

Le monoxyde de carbone, communément désigné sous le nom d’oxyde de carbone (CO), est un gaz inodore et incolore, qui réduit l’aptitude de l’hémoglobine à transporter et à fournir de l’oxygène.
Présence. La formation d’oxyde de carbone résulte de la combustion incomplète, en présence d’air ou d’oxygène en quantité limitée, de matières organiques telles que le charbon, le bois, le papier, les huiles, l’essence, le gaz, les explosifs ou toute autre matière carbonée. Lorsque la combustion a lieu en présence d’une quantité abondante d’air sans que la flamme entre en contact avec une surface, un dégagement d’oxyde de carbone a peu de chance de se produire. Le CO se forme lorsque la flamme entre en contact avec une surface dont la température est inférieure à la température d’ignition de la partie gazeuse de la flamme. Le CO atmosphérique est à 90% d’origine naturelle, l’activité humaine produisant les 10% restants. Les véhicules à moteur sont responsables de 55 à 60% de la quantité totale de CO résultant de l’activité humaine. Les gaz d’échappement des moteurs à essence (allumage à étincelle) sont une source courante de CO atmosphérique. Les gaz d’échappement des moteurs diesel (allumage par compression) contiennent environ 0,1% de CO lorsque le moteur fonctionne correctement, mais les moteurs diesel mal réglés, en surcharge ou mal entretenus peuvent émettre des quantités considérables de CO. Les brûleurs thermiques ou catalytiques placés dans les pots d’échappement réduisent considérablement la quantité de CO émise. Les autres sources importantes de CO sont constituées par des installations telles que les cubilots des fonderies, les unités de craquage catalytique des raffineries de pétrole, les unités de distillation de la houille et du bois, les fours à chaux et les fours de récupération du papier kraft des fabriques de papier kraft, les cokeries, les usines à gaz et les usines d’incinération d’ordures, ou par des opérations telles que la synthèse du méthanol et d’autres composés organiques à partir d’oxyde de carbone, le frittage de la charge des hauts-fourneaux, la fabrication des carbures, la synthèse du formaldéhyde et la fabrication du noir de carbone.
Toute opération dans laquelle se produit une combustion incomplète de matières organiques peut constituer une source potentielle d’émission d’oxyde de carbone.
On produit le monoxyde de carbone à l’échelle industrielle par oxydation partielle d’hydrocarbures gazeux provenant du gaz naturel ou par la gazéification de la houille ou du coke. Il sert d’agent réducteur en métallurgie et on l’emploie également en synthèse organique et pour la préparation des métaux-carbonyles. Plusieurs gaz industriels que l’on utilise pour chauffer des chaudières et des fours et faire fonctionner des moteurs à gaz contiennent de l’oxyde de carbone.
Le monoxyde de carbone est considéré comme la cause la plus fréquente d’intoxications en milieu industriel ou domestique. Chaque année, des milliers de personnes succombent à une intoxication par le CO. On estime que le nombre des victimes d’intoxications dont l’issue n’a pas été fatale, mais qui souffrent de lésions permanentes du système nerveux central (SNC) est encore plus important. L’exposition au monoxyde de carbone, que l’issue en soit fatale ou non, représente un risque sanitaire considérable, et les intoxications sont probablement plus fréquentes qu’on veut bien généralement le reconnaître.
Une proportion notable de la population active d’un pays court un important risque professionnel d’exposition au CO. Ce risque est toujours présent dans l’industrie automobile, les garages et les stations-service. Les routiers peuvent également être en danger si, à l’occasion d’une fuite, des gaz d’échappement s’infiltrent dans la cabine du conducteur. Les activités qui peuvent exposer au CO sont nombreuses — par exemple, la mécanique automobile, la préparation du charbon de bois, le travail auprès des fours à coke, des cubilots, des hauts-fourneaux, dans les forges, les mines, les tunnels ou les installations utilisant le procédé Mond d’affinage, dans les usines à gaz, les chaufferies, auprès des fours à poterie, dans les unités de distillation du bois, les cuisines de restaurants, les boulangeries, le service du feu, les unités de production de formaldéhyde, etc. Les opérations de soudage dans des cuves, réservoirs ou autres récipients peuvent produire des quantités dangereuses de CO si la ventilation n’est pas efficace. Les explosions de méthane et les coups de poussière dans les mines de charbon produisent de la «mofette» qui emmagasine des quantités considérables de monoxyde et de dioxyde de carbone. Si la ventilation diminue ou que l’émission de CO augmente par suite de fuites ou de problèmes dans une opération industrielle, des intoxications peuvent se produire inopinément alors qu’il n’y a normalement pas de risque lié au CO dans ces circonstances.
Dans l’organisme humain, le catabolisme des hèmes contenus dans l’hémoglobine et autres pigments produit de faibles quantités de CO, ce qui entraîne une saturation endogène de l’hémoglobine en carboxyhémoglobine (COHb) d’environ 0,3 à 0,8%. La concentration de COHb endogène augmente dans les anémies hémolytiques ou à la suite de contusions et d’hématomes importants, entraînant une augmentation du catabolisme de l’hémoglobine.
Le CO pénètre facilement dans le sang au niveau des poumons. L’effet biologique le mieux connu du CO est sa combinaison avec l’hémoglobine pour former la COHb. Le monoxyde de carbone entre en compétition avec l’oxygène pour les sites de liaison des molécules d’hémoglobine. L’affinité de l’hémoglobine humaine pour le CO est environ 240 fois supérieure à son affinité pour l’oxygène. La formation de COHb produit deux effets indésirables: elle bloque le transport d’oxygène en inactivant l’hémoglobine et sa présence dans le sang déplace la courbe de dissociation de l’oxyhémoglobine (O2Hb) vers la gauche, d’où un mauvais relargage tissulaire de l’oxygène par l’O2Hb restante. En raison de ce dernier effet, la présence de COHb dans le sang réduit bien davantage l’oxygénation tissulaire qu’une diminution équivalente de la concentration d’hémoglobine, par exemple à la suite d’une hémorragie. Le monoxyde de carbone se fixe également sur la myoglobine pour former la carboxymyoglobine, qui peut perturber le métabolisme musculaire, en particulier au niveau du myocarde.
Le rapport approximatif de la COHb à l’O2Hb dans le sang peut être calculé à l’aide de l’équation de Haldane. Ce rapport est proportionnel au rapport des pressions partielles du CO et de l’oxygène dans l’air alvéolaire:
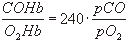
L’équation est applicable dans la plupart des cas se présentant dans la pratique pour calculer la valeur approximative du rapport à l’équilibre. Pour une concentration donnée de CO dans l’air ambiant, la concentration de COHb augmente ou diminue pour tendre vers l’équilibre, conformément à l’équation. Le sens de la variation de la COHb dépend de sa valeur initiale. A titre d’exemple, l’exposition continue à une atmosphère contenant 35 ppm de CO entraînerait un état d’équilibre correspondant à environ 5% de COHb dans le sang, après quoi, si la concentration atmosphérique reste inchangée, le taux de COHb ne varie plus. Si la concentration atmosphérique augmente ou diminue, le taux de COHb varie également pour tendre vers un nouvel équilibre. Un gros fumeur peut présenter une concentration sanguine de COHb de 8% au début d’un poste de travail. S’il est exposé en continu à une concentration de 35 ppm de CO pendant le poste, mais qu’il lui est interdit de fumer, son taux de COHb va diminuer progressivement pour atteindre un nouvel état d’équilibre à 5% de COHb. Par contre, le taux de COHb des travailleurs non fumeurs va augmenter progressivement à partir d’une valeur initiale d’environ 0,8% de COHb endogène pour tendre vers le taux de 5%. Ainsi donc, l’absorption de CO et la formation de COHb sont déterminées par la loi des gaz parfaits, et la résolution de l’équation de Haldane permet d’obtenir la valeur maximale approximative de COHb pour une concentration atmosphérique donnée de CO. Toutefois, il faut noter que, chez l’être humain, le temps nécessaire pour atteindre l’équilibre est de plusieurs heures pour des concentrations atmosphériques de CO généralement présentes sur les lieux de travail. Par conséquent, lorsqu’on évalue le risque sanitaire potentiel que comporte l’exposition au CO, il faut prendre en compte la durée de l’exposition en plus de la concentration atmosphérique de CO. La ventilation alvéolaire influe également fortement sur la vitesse d’absorption du CO. Lorsque la ventilation alvéolaire augmente — lors d’un effort physique important, par exemple —, l’équilibre est atteint plus rapidement que dans une situation où la ventilation est normale.
La demi-vie biologique de la COHb dans le sang d’un adulte sédentaire est d’environ 3 à 4 heures. L’élimination du CO ralentit avec le temps et plus la concentration initiale de COHb est faible, plus la vitesse d’élimination est lente.
L’apparition des symptômes est fonction de la concentration de CO dans l’air, de la durée de l’exposition, de l’importance de l’effort physique et de la sensibilité individuelle. Si l’exposition est massive, le sujet peut perdre conscience presque instantanément, les prodromes étant peu nombreux sinon absents. L’exposition à des concentrations de 10 000 à 40 000 ppm entraîne la mort en quelques minutes. Entre 1 000 et 10 000 ppm, des céphalées, des étourdissements et des nausées apparaissent en 13 à 15 minutes, suivis d’une perte de conscience et de la mort si l’exposition se poursuit pendant 10 à 45 minutes, la rapidité de l’effet variant avec la concentration. Au-dessous de ces valeurs, le temps de latence des symptômes est allongé: une concentration de 500 ppm cause des céphalées au bout de 20 minutes et une concentration de 200 ppm, au bout de 50 minutes. La relation entre la concentration de COHb et la symptomatologie est explicitée au tableau 104.125.
|
Concentration de carboxyhémoglobine (COHb) (%) |
Principaux signes et symptômes |
|
0,3-0,7 |
Asymptomatique. Taux endogène normal |
|
2,5-5 |
Asymptomatique. Augmentation compensatoire du flux sanguin vers certains organes vitaux. Il peut y avoir décompensation en cas de maladie cardio-vasculaire grave. Chez l’angineux, la douleur thoracique apparaît plus rapidement à l’effort |
|
5-10 |
Légère élévation du seuil de perception lumineuse |
|
10-20 |
Constriction frontale. Légères céphalées. Anomalies de la réponse visuelle évoquée. Possibilité de léger essoufflement à l’effort. Peut être mortelle pour le fœtus ou pour des malades souffrant d’affections cardio-vasculaires graves |
|
20-30 |
Céphalées de légères à modérées et battements dans les tempes. Rougeur de la face. Nausées. Perte de la dextérité manuelle fine |
|
30-40 |
Violentes céphalées, vertiges, nausées et vomissements. Faiblesse. Irritabilité et altération du jugement. Syncope à l’effort |
|
40-50 |
Comme ci-dessus, mais plus intenses, avec risque accru de collapsus et de syncope |
|
50-60 |
Risque de coma avec convulsions intermittentes et respiration de Cheyne-Stokes |
|
60-70 |
Coma avec convulsions intermittentes. Respiration et activité cardiaque réduites. Risque d’issue fatale |
|
70-80 |
Pouls faible et respiration lente. Dépression du centre respiratoire aboutissant à la mort |
1 Les symptômes varient considérablement d’un sujet à l’autre.
La description classique de l’intoxication oxycarbonée évoque généralement la teinte cochenille des téguments. Aux stades précoces de l’intoxication, on constate plutôt une pâleur. Ultérieurement, la peau, le lit unguéal et les muqueuses peuvent prendre la teinte cochenille en raison de la concentration élevée de COHb et de la faible concentration d’hémoglobine dans le sang. Ce signe peut être reconnaissable à partir d’une concentration de COHb de 30%, mais il n’est ni fiable ni invariable dans l’intoxication oxycarbonée. Le pouls du patient est rapide et bondissant. L’hyperpnée est faible ou absente, sauf si le taux de COHb est très élevé.
Lorsque les symptômes ci-dessus se produisent chez une personne potentiellement exposée au CO de par son travail, il y a lieu de suspecter immédiatement une intoxication oxycarbonée. Par rapport à une intoxication médicamenteuse, un éthylisme aigu, un accident vasculaire cérébral ou cardiaque, un coma diabétique ou urémique, le diagnostic différentiel peut être difficile et il arrive souvent que la possibilité d’une exposition au monoxyde de carbone ne soit pas reconnue ou soit simplement négligée. Le diagnostic d’une intoxication oxycarbonée ne doit pas être considéré comme posé aussi longtemps que l’on n’a pas établi avec certitude la présence dans l’organisme de quantités anormales de CO. Le monoxyde de carbone est facilement décelable dans un échantillon de sang et, si les poumons du sujet sont en bon état, il est possible de déterminer rapidement le taux sanguin de COHb sur un échantillon d’air alvéolaire exhalé en équilibre avec la concentration de COHb dans le sang.
Les organes cibles du CO sont le cerveau et le cœur qui exigent tous les deux un apport ininterrompu d’oxygène. Le monoxyde de carbone affecte le cœur de deux manières — le travail du cœur augmente pour assurer la demande périphérique d’oxygène, tandis que sa propre alimentation en oxygène est réduite par le CO. Une exposition au monoxyde de carbone peut précipiter un infarctus du myocarde.
L’intoxication aiguë peut entraîner une atteinte neurologique ou cardio-vasculaire, qui est manifeste à la sortie du premier coma. Dans le cas d’une intoxication grave, un œdème pulmonaire (quantité excessive de liquide dans les tissus pulmonaires) peut apparaître. Une pneumonie, due parfois à l’aspiration, peut se manifester après quelques heures ou quelques jours. Une glycosurie ou une albuminurie temporaires peuvent aussi se produire. Dans de rares cas, l’insuffisance rénale aiguë complique le rétablissement. Diverses manifestations cutanées peuvent également s’observer.
Après une grave intoxication oxycarbonée, le patient peut souffrir d’un œdème cérébral accompagné de lésions irréversibles plus ou moins étendues. Un premier rétablissement peut être suivi d’une rechute neuropsychiatrique, des jours ou même des semaines après l’intoxication. L’étude anatomopathologique des cas mortels indique que les lésions cérébrales concernent principalement la substance blanche plutôt que les neurones chez les victimes qui survivent quelques jours à l’intoxication. La gravité de l’atteinte cérébrale dépend de l’intensité et de la durée de l’exposition. Lorsque les victimes d’une intoxication oxycarbonée aiguë reprennent conscience, 50% d’entre elles présentent un état mental anormal qui se manifeste par de l’irritabilité, de l’agitation, un délire prolongé, une dépression ou de l’anxiété. Le suivi de ces patients pendant 3 ans a révélé que 33% présentaient une altération de la personnalité et 43% des troubles mnésiques permanents.
Expositions répétées. Le monoxyde de carbone ne s’accumule pas dans l’organisme. Il est complètement éliminé après chaque exposition, à condition que le patient reste suffisamment longtemps à l’air frais. Néanmoins, il peut arriver que des intoxications répétées, même faibles à modérées, et qui n’ont pas entraîné de perte de conscience, provoquent la mort des cellules cerébrales et finissent par déterminer des lésions centrales dont les symptômes peuvent être nombreux: céphalées, étourdissements, irritabilité, perte de mémoire, altération de la personnalité et faiblesse des membres.
Une exposition répétée à des concentrations modérées de CO pourrait entraîner une certaine adaptation à l’action du CO. On suppose que ce mécanisme d’adaptation est semblable à celui de la tolérance vis-à-vis de l’hypoxie en altitude. On a constaté une augmentation de la concentration d’hémoglobine et de l’hématocrite chez des animaux exposés, mais ni le déroulement, ni le seuil d’apparition de ces effets n’ont été déterminés avec précision chez des sujets humains exposés.
Effets de l’altitude. A une altitude élevée, la combustion a plus de chances d’être incomplète et de dégager davantage de CO, car la teneur de l’air en oxygène est moindre qu’au niveau de la mer. L’organisme réagit également moins favorablement, en raison de la baisse de la pression partielle d’oxygène dans l’air inspiré. Il semble que, à une altitude élevée, les effets du CO et ceux du manque d’oxygène s’additionnent.
Parmi les hydrocarbures halogénés dérivés du méthane, le dichlorométhane (chlorure de méthylène), qui est l’un des principaux constituants de nombreux décapants pour peintures et d’autres solvants de ce type, est métabolisé dans le foie avec production de CO. Il en résulte une augmentation de la concentration de COHb jusqu’à produire une intoxication modérée.
Effets d’une exposition oxycarbonée à faible dose. Ces dernières années, on a déployé des efforts de recherche considérables pour déterminer les effets biologiques de concentrations de COHb inférieures à 10% chez des sujets sains et des patients souffrant d’affections cardio-vasculaires. Un patient souffrant d’une affection cardio-vasculaire grave peut se révéler incapable de compenser le déficit d’oxygénation lorsque le taux sanguin de COHb atteint environ 3%, de sorte qu’une douleur angineuse peut être réveillée plus rapidement par l’effort. Le CO traverse facilement la barrière placentaire, exposant ainsi le fœtus, dont la sensibilité à toute charge hypoxique supplémentaire risque de compromettre le développement normal.
Groupes sensibles. Les personnes dont la capacité de transport de l’oxygène est réduite en raison d’une anémie ou d’une hémoglobinopathie sont particulièrement sensibles à l’action du CO; il en va de même pour celles dont les besoins en oxygène sont accrus par suite de fièvre, d’hyperthyroïdie ou de grossesse, pour les malades souffrant d’hypoxie systémique par insuffisance respiratoire ou encore de cardiopathie ischémique ou d’artériosclérose cérébrale ou généralisée. Chez les enfants et les jeunes dont la ventilation est plus rapide que chez l’adulte, la concentration toxique de COHb est plus rapidement atteinte que chez ce dernier. De même, un fumeur exposé à une forte dose et dont le taux initial de COHb est supérieur à celui d’un non-fumeur atteindra plus rapidement une concentration dangereuse de COHb.