

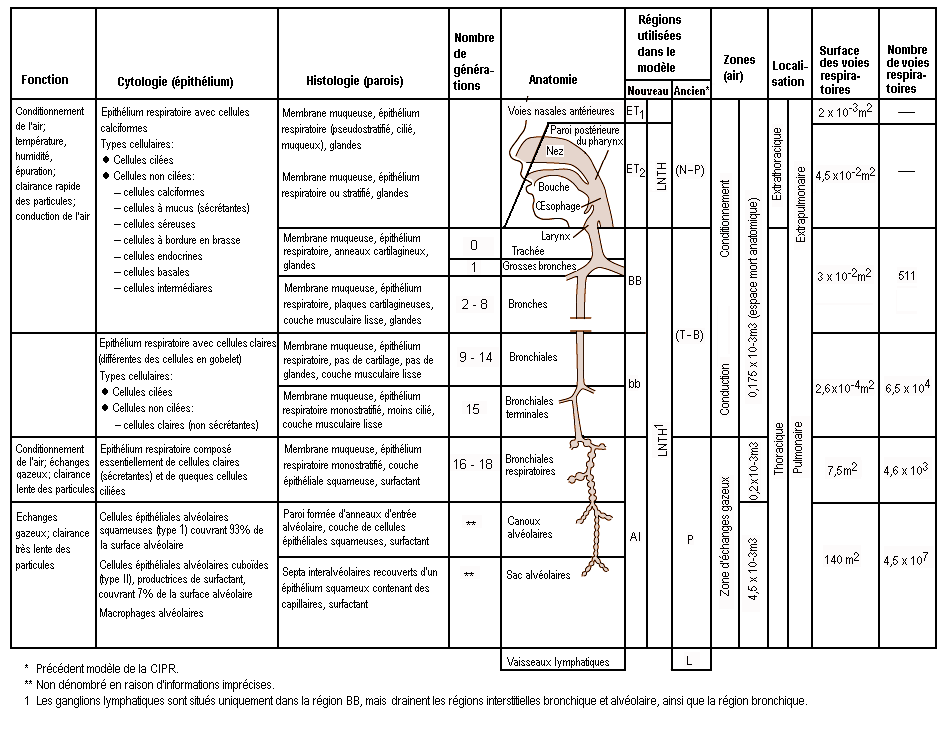
L’appareil respiratoire commence au nez et à la bouche, se poursuit par les voies aériennes au niveau du cou et du thorax et se termine par les alvéoles pulmonaires où s’effectuent les échanges gazeux avec les capillaires sanguins périalvéolaires. Cet appareil a pour principale fonction d’apporter l’oxygène (O2) dans la zone d’échanges gazeux des poumons où il peut diffuser à travers la paroi alvéolaire pour oxygéner le sang circulant dans les capillaires alvéolaires, en fonction des besoins engendrés par les divers types de travaux ou d’activités. L’appareil respiratoire doit également: 1) éliminer un volume égal de gaz carbonique amené aux poumons par les capillaires alvéolaires; 2) maintenir la température corporelle et l’état de saturation de la vapeur d’eau dans les voies aériennes (pour assurer la viabilité et les capacités fonctionnelles des liquides de surface et des cellules); 3) rester stérile (pour prévenir les infections et leurs conséquences indésirables); 4) éliminer les liquides superficiels excédentaires et les débris tels que les particules inhalées et les cellules phagocytaires et épithéliales sénescentes. Il doit accomplir l’ensemble de ces fonctions exigeantes en permanence, tout au long de la vie, en faisant preuve d’une efficacité élevée quant à sa performance et à sa consommation énergétique. L’appareil respiratoire peut être victime d’agressions sévères résultant, par exemple, d’un tabagisme prononcé, de concentrations élevées de poussières industrielles ou de faibles concentrations d’agents pathogènes spécifiques qui perturbent ou détruisent ses mécanismes de défense ou en altèrent le bon fonctionnement. Son aptitude à maîtriser ces agressions ou à les neutraliser comme il le fait généralement témoigne de l’heureuse combinaison de ses propriétés structurales et fonctionnelles.
La structure complexe et les multiples fonctions de l’appareil respiratoire humain ont été exposées sous une forme condensée par un Groupe de travail de la Commission internationale de protection radiologique (CIPR, 1994), comme le montre la figure 10.1. Les voies aériennes de conduction, également appelées espace mort respiratoire, ont un volume d’environ 0,2 litre. Elles conditionnent l’air inhalé et le distribuent par convection (globalement) aux quelque 65 000 acini auxquels aboutissent les bronchioles terminales. Plus le volume inspiré augmente et plus les échanges gazeux s’opèrent profondément dans les bronchioles. Dans tous les cas, au niveau de l’acinus respiratoire, la distance séparant le front de convection de la surface alvéolaire est suffisamment courte pour permettre des échanges CO2-O2 efficaces par diffusion moléculaire. En revanche, les particules en suspension dans l’air, dont le coefficient de diffusion est inférieur de plusieurs ordres de grandeur à celui des gaz, ont tendance à rester en suspension dans l’air inspiré et peuvent être exhalées sans s’être déposées.
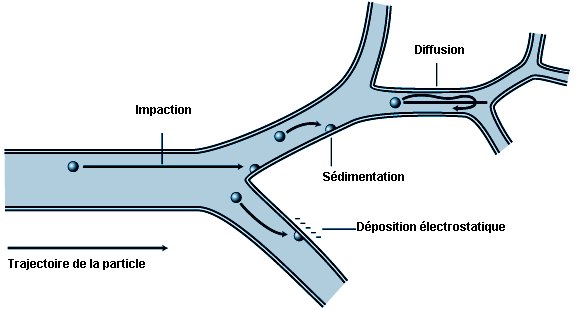
Une fraction élevée des particules inhalées se dépose dans les voies respiratoires. Les mécanismes expliquant la déposition des particules au cours de la phase inspiratoire d’un cycle ventilatoire sont résumés à la figure 10.2. Les particules de plus de 2 µm de diamètre aérodynamique (diamètre d’une sphère de densité unitaire ayant la même vitesse terminale de sédimentation (Stokes)) peuvent être dotées d’une énergie cinétique importante et se déposer par impaction aux vitesses relativement élevées observées dans les voies respiratoires de plus gros calibre. Les particules de plus de 1 µm se déposent par sédimentation dans les voies respiratoires de plus petit calibre où la vitesse de l’air est nettement moins élevée. Enfin, les particules de diamètre compris entre 0,1 et 1 µm, qui ont très peu de chances de se déposer au cours d’un cycle ventilatoire, peuvent demeurer dans les 15% environ d’air inspiré qui sont échangés avec l’air résiduel des poumons au cours de chaque cycle. Cet échange volumétrique est le fait des débits d’air variables dans les différentes régions du poumon. Du fait de l’allongement de la durée de séjour de l’air résiduel dans les poumons, le mouvement brownien des particules de 0,1 à 1 µm présentes dans ce volume d’air inhalé piégé devient suffisant pour permettre leur déposition par sédimentation ou leur diffusion au cours de plusieurs cycles ventilatoires successifs.
L’air résiduel pulmonaire, pratiquement exempt de particules, représente 15% environ de l’air expiratoire courant et a tendance à se comporter comme une gaine d’air propre entourant une colonne centrale d’air se déplaçant vers l’extérieur, de sorte que dans l’acinus respiratoire, les particules se déposent essentiellement sur les parois intérieures telles que les bifurcations des voies respiratoires, alors que la déposition est minime au niveau des parois des voies respiratoires situées entre les points de bifurcation.
Le nombre de particules déposées et leur distribution le long des parois des voies respiratoires sont, avec les propriétés toxiques du matériau déposé, les principaux déterminants du pouvoir pathogène. Les particules déposées peuvent léser les cellules épithéliales ou les phagocytes mobiles au niveau des sites de dépôt ou à leur voisinage; elles peuvent aussi stimuler la sécrétion de liquides et de médiateurs d’origine cellulaire exerçant des effets secondaires sur l’appareil. Les substances solubles déposées sur les particules ou à l’intérieur de celles-ci peuvent gagner par diffusion les liquides de surface et les cellules et être rapidement transportées par la circulation sanguine dans l’ensemble de l’organisme.
La solubilité dans l’eau des substances brutes reflète mal celle des particules de ces mêmes substances dans l’appareil respiratoire. D’une manière générale, la solubilité est considérablement accrue par la valeur très élevée du rapport surface/volume des particules de taille suffisamment petite pour pénétrer dans les poumons. De plus, la teneur en ions et en lipides des liquides de surface présents dans les voies respiratoires est complexe et extrêmement variable et peut entraîner une augmentation de la solubilité ou une précipitation rapide des solutés aqueux. En outre, les voies de clairance et les temps de séjour des particules déposées à la surface des voies respiratoires sont très différents dans les divers segments fonctionnels de l’appareil respiratoire.
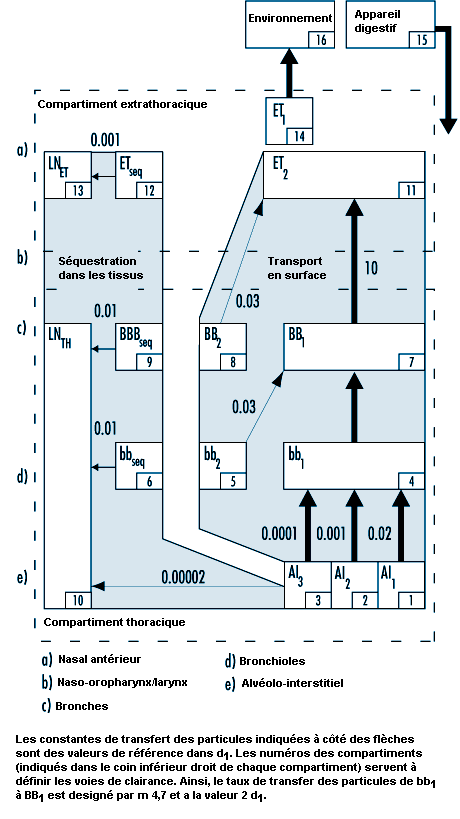
Le modèle révisé de clairance élaboré par le Groupe de travail de la CIPR décrit les principales voies d’élimination respiratoire qui interviennent dans la détermination de la rétention de diverses substances radioactives et, par conséquent, des doses de rayonnements reçues par les tissus respiratoires et d’autres organes après translocation. Le modèle de déposition de la CIPR permet d’évaluer la quantité de substance inhalée qui pénètre dans chacune des voies de clairance. Ces voies discrètes sont représentées par le modèle de la figure 10.3. Elles correspondent aux compartiments anatomiques de la figure 10.1 et sont résumées dans le tableau 10.1, avec celles déterminées par d’autres groupes d’experts en matière de dosimétrie des particules inhalées.
|
Structures anatomiques incluses |
Région définie par le modèle de l�ACGIH |
Régions définies par l�ISO et le CEN |
Région définie par le Groupe de travail de la CIPR (1996) |
Région définie par le Groupe de travail de la CIPR (1994) |
|
Nez, nasopharynx |
Voies respiratoires céphaliques (HAR) |
Voies respiratoires extrathoraciques (E) |
Nasopharynx (NP) |
Voies nasales antérieures (ET1) |
|
Trachée, bronches |
Trachéo-bronchique (TBR) |
Trachéo-bronchique (B) |
Trachéo-bronchique (TB) |
Trachée et grosses bronches (BB) |
|
Bronchioles (jusqu�aux bronchioles terminales) |
— |
— |
— |
Bronchioles (bb) |
|
Bronchioles respiratoires, canaux alvéolaires, sacs alvéolaires, alvéoles |
Echanges gazeux (GER) |
Alvéolaire (A) |
Pulmonaire (P) |
Voies alvéolo-interstitielles (AI) |
Comme le montre la figure 10.1, la CIPR (1994) divise les voies respiratoires extrathoraciques en deux zones distinctes sur le plan de la clairance et de la dosimétrie: la filière nasale antérieure (ET1) et l’ensemble des autres voies respiratoires extrathoraciques (ET2) — à savoir la filière nasale postérieure, le nasopharynx, l’oropharynx et le larynx. Les particules déposées à la surface de la peau tapissant la filière nasale antérieure (ET1) sont censées n’être soumises qu’à des moyens d’élimination extrinsèques (mouchage, essuyage, etc.). La majeure partie de la matière déposée dans le nasopharynx et l’oropharynx (ET2) fait l’objet d’une élimination rapide avec le liquide tapissant ces voies respiratoires. A la différence des modèles précédents, le nouveau modèle reconnaît que la déposition des particules ultrafines par diffusion dans les voies respiratoires extrathoraciques peut être importante.
La matière radioactive déposée à l’intérieur du thorax se répartit généralement entre la région trachéo-bronchique (TB), où les particules déposées sont soumises à une clairance mucociliaire relativement rapide, et la région alvéolo-interstitielle (AI), où la clairance des particules est beaucoup plus lente.
Pour la dosimétrie, la CIPR (1994) a réparti la déposition des substances inhalées dans la région TB entre la trachée et les bronches (BB) et les petites voies aériennes plus distales, les bronchioles (bb). L’efficacité avec laquelle les cils de ces deux types de voies respiratoires sont capables d’éliminer les particules déposées est toutefois sujette à controverse. Pour être certain de ne pas sous-estimer les doses appliquées aux épithéliums bronchique et bronchiolaire, le Groupe de travail de la CIPR a présumé que la moitié des particules déposées dans ces voies respiratoires était soumise à une clairance mucociliaire relativement «lente». La probabilité de l’élimination assez lente d’une particule par le système mucociliaire semble dépendre du calibre de celle-ci.
La substance déposée dans la région AI se répartit entre trois compartiments (AI1, AI2 et AI3), chacun d’eux étant nettoyé plus lentement que la région TB, le nettoyage des subdivisions s’effectuant à des vitesses caractéristiques différentes.
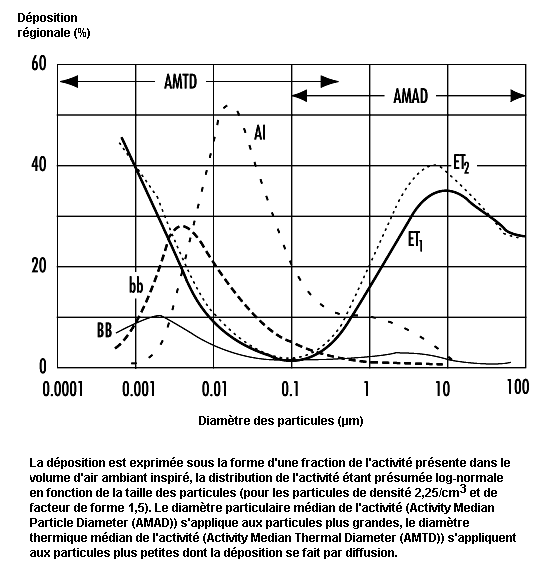
La figure 10.4 illustre les prédictions du modèle de la CIPR (1994) relatives aux fractions déposées dans chaque région en fonction de la taille des particules inhalées. Elle montre que le dépôt pulmonaire est minime pour les particules de 0,1 à 1 µm, ce dépôt étant largement déterminé par les échanges entre l’air courant et l’air résiduel dans la profondeur des poumons. Le dépôt augmente au-dessous de 0,1 µm, car la diffusion s’accroît avec la diminution de la taille des particules. Il s’accentue également lorsque les particules ont plus de 1 µm, la sédimentation et l’impaction devenant de plus en plus efficaces.
Des modèles moins complexes du phénomène de déposition en fonction de la taille ont été adoptés par les spécialistes et les organismes publics chargés de la pollution de l’air et de la médecine du travail et ont été utilisés pour déterminer des limites d’exposition par inhalation pour certaines tailles de particules. On établit une distinction entre:
Au début des années quatre-vingt-dix, on a procédé à une harmonisation internationale des définitions quantitatives de la MPI, de la MPT et de la MPR. Le tableau 10.2 résume les spécifications de l’orifice d’admission des particules en fonction de leur calibre dans les échantillonneurs d’air satisfaisant aux critères de la Conférence américaine des hygiénistes industriels gouvernementaux (American Conference of Governmental Industrial Hygienists (ACGIH)) (ACGIH, 1993), de l’Organisation internationale de normalisation (ISO, 1995) et du Comité européen de normalisation (CEN, 1993). Elles diffèrent des fractions de dépôt de la CIPR (1994), en particulier pour les particules de grande taille, car elles sont fondées sur le principe prudent qu’une protection est nécessaire contre les particules inhalées par voie buccale qui ont contourné le filtre très efficace constitué par les fosses nasales.
|
Fraction inhalable |
Fraction thoracique |
Fraction respirable ou alvéolaire |
PM10 |
||||
|
Diamètre aéro-dynamique des particules (µm) |
Masse particulaire inhalable (MPI) (%) |
Diamètre aéro-dynamique des particules (µm) |
Masse particulaire thoracique (MPT) (%) |
Diamètre aéro-dynamique des particules (µm) |
Masse particulaire respirable (MPR) (%) |
Diamètre aéro-dynamique des particules (µm) |
Masse particulaire thoracique (MPT) (%) |
|
0 |
100 |
0 |
100 |
0 |
100 |
0 |
100 |
|
1 |
97 |
2 |
94 |
1 |
97 |
2 |
94 |
|
2 |
94 |
4 |
89 |
2 |
91 |
4 |
89 |
|
5 |
87 |
6 |
80,5 |
3 |
74 |
6 |
81,2 |
|
10 |
77 |
8 |
67 |
4 |
50 |
8 |
69,7 |
|
20 |
65 |
10 |
50 |
5 |
30 |
10 |
55,1 |
|
30 |
58 |
12 |
35 |
6 |
17 |
12 |
37,1 |
|
40 |
54,5 |
14 |
23 |
7 |
9 |
14 |
15,9 |
|
50 |
52,5 |
16 |
15 |
8 |
5 |
16 |
0 |
|
100 |
50 |
18 |
9,5 |
10 |
1 |
— |
— |
|
— |
— |
20 |
6 |
— |
— |
— |
— |
|
— |
— |
25 |
2 |
— |
— |
— |
— |
La norme choisie par l’Agence américaine de protection de l’environnement (Environmental Protection Agency (EPA)) (EPA, 1987) pour le taux des particules dans l’air ambiant est le PM10, c’est-à-dire la matière particulaire de moins de 10 µm de diamètre aérodynamique. Les valeurs retenues pour l’orifice d’admission des échantillonneurs sont fonctionnellement équivalentes à celles de la MPT, mais les spécifications sont numériquement un peu différentes, comme le montre le tableau 10.2.
Dans des conditions normales de température et de pression ambiantes, les polluants peuvent être dispersés dans l’air sous forme gazeuse, liquide ou solide. Les deux dernières formes constituent des suspensions de particules dans l’air et Gibbs (1924) leur a donné le nom générique d’aérosols, par analogie avec le terme hydrosols, utilisé pour décrire les systèmes dispersés dans l’eau. Les gaz et vapeurs, présents sous la forme de molécules discrètes, forment de véritables solutions dans l’air. Les particules de substances à pression de vapeur élevée ou modérée ont tendance à s’évaporer rapidement, car celles qui sont suffisamment petites pour rester en suspension dans l’air plus de quelques minutes (c’est-à-dire celles de moins de 10 µm environ) sont caractérisées par une valeur élevée du rapport surface/volume. Certaines substances ayant une pression de vapeur relativement basse peuvent être présentes simultanément sous forme de vapeurs et d’aérosols, et, cela, en pourcentages notables.
Une fois dispersés dans l’air, les gaz et les vapeurs forment des mélanges tellement dilués que leurs propriétés physiques (masse volumique, viscosité, enthalpie, etc.) sont indiscernables de celles de l’air propre. On peut considérer que ces mélanges satisfont aux lois des gaz parfaits. En pratique, il n’y a aucune différence entre un gaz et une vapeur, sauf que celle-ci est généralement assimilée à la phase gazeuse d’une substance qui peut exister sous forme solide ou liquide à la température ambiante. Une fois dispersées dans l’air, toutes les molécules d’une substance donnée sont analogues pour l’essentiel quant à leur dimension et à leurs probabilités de capture par les surfaces proches, les parois de l’arbre respiratoire et les collecteurs ou échantillonneurs de polluants.
Les aérosols sont des dispersions de particules solides ou liquides dans l’air; ils se caractérisent également par une variable très importante, à savoir la taille des particules. Celle-ci influe sur les mouvements des particules et, par conséquent, sur la probabilité d’apparition de phénomènes physiques tels que la coagulation, la dispersion, la sédimentation, l’impaction, l’interfaçage et les propriétés de diffusion de la lumière. Il n’est pas possible de caractériser une particule donnée par sa seule taille. A titre d’exemple, on relèvera que les propriétés aérodynamiques d’une particule dépendent de sa masse volumique et de sa forme, ainsi que de ses dimensions linéaires, tandis que la taille effective permettant la dispersion des rayons lumineux dépend de l’indice de réfraction et de la forme.
Dans certains cas particuliers, toutes les particules d’un aérosol ont essentiellement la même taille: on parle alors d’un aérosol monodispersé. C’est le cas, par exemple, des pollens naturels et de certains aérosols produits en laboratoire. En général, cependant, les aérosols sont composés de particules de calibres différents et sont donc dits hétérodispersés ou polydispersés. Des aérosols différents ont des degrés différents de dispersion de taille. Il est donc nécessaire de spécifier au moins deux paramètres pour caractériser la taille de l’aérosol: une mesure de la tendance centrale (moyenne ou médiane) et une mesure de la dispersion (écart-type arithmétique ou géométrique).
Les diamètres des particules générées par une source ou un processus unique obéissent généralement à une distribution log-normale, c’est-à-dire que les logarithmes de ces diamètres ont une distribution gaussienne. Dans ce cas, la dispersion est caractérisée par l’écart-type géométrique, qui correspond au rapport de la taille au 84,1e centile à la taille au 50e centile. Lorsqu’il existe plusieurs sources importantes de particules, l’aérosol mixte qui en résulte ne suivra généralement pas une seule distribution log-normale et il pourra être nécessaire de le caractériser par la somme de plusieurs distributions.
Les particules possèdent, outre leur taille linéaire, de nombreuses caractéristiques susceptibles d’exercer une grande influence sur leur comportement dans l’air et leurs effets sur l’environnement et la santé. Ce sont notamment:
La surface. Pour les particules sphériques, la surface varie selon le carré de leur diamètre. Cependant, pour les aérosols de concentration massique donnée, plus la taille des particules diminue et plus la surface totale augmente. Pour les particules non sphériques ou les agrégats, de même que pour les particules fissurées ou poreuses, le rapport surface/volume peut être beaucoup plus élevé que dans le cas des particules sphériques.
Le volume. Le volume d’une particule varie selon le cube de son diamètre. Il s’ensuit que les quelques particules les plus grandes d’un aérosol ont un rôle dominant dans sa concentration volumique (ou massique).
La forme. La forme d’une particule influe sur son comportement aérodynamique (coefficient de traînée), de même que sur sa surface et, par conséquent, sur ses probabilités de déplacement et de déposition.
La masse volumique. La vitesse d’une particule, sous l’effet de la pesanteur ou de la force d’inertie, varie selon la racine carrée de sa masse volumique.
Le diamètre aérodynamique. Le diamètre aérodynamique d’une particule est égal au diamètre d’une sphère de masse volumique égale à 1 g/3 possédant la même vitesse terminale de chute que la particule considérée. La vitesse terminale de chute est la vitesse d’équilibre d’une particule tombant sous l’influence de la pesanteur et soumise à la résistance du fluide qui l’entoure. Le diamètre aérodynamique est déterminé par la taille réelle de la particule, sa masse volumique et un coefficient de forme aérodynamique.
Les aérosols sont généralement classés en fonction de leurs modes de formation. Bien que la classification ci-après ne soit ni rigoureuse ni complète, elle est couramment utilisée et agréée dans les domaines de l’hygiène industrielle et de la pollution atmosphérique.
Le terme poussière désigne un aérosol formé par subdivision mécanique d’un matériau mère à l’état solide en petits fragments aéroportés ayant la même composition chimique. Les particules de poussière sont généralement solides et de forme irrégulière et leur diamètre dépasse 1 µm.
Le terme fumées (au pluriel) désigne un aérosol composé de particules solides formées par condensation de vapeurs produites par combustion ou sublimation d’un corps solide à des températures élevées. Les particules primaires sont généralement très petites (moins de 0,1 µm) et ont une forme sphérique ou cristalline caractéristique. Elles peuvent être chimiquement identiques à la substance mère ou peuvent être composées d’un produit d’oxydation, un oxyde métallique par exemple. Comme elles peuvent être formées en très grand nombre, elles s’agrègent souvent rapidement et forment des amas de faible densité globale.
Le terme fumée (au singulier) désigne un aérosol formé par condensation de produits de combustion, généralement de matières organiques. Les particules sont généralement des gouttelettes liquides de diamètre inférieur à 0,5 µm.
Le terme brouillard peut désigner soit un aérosol aqueux constitué par condensation de vapeur d’eau sur des noyaux atmosphériques dans des conditions d’humidité relative élevée (la taille des gouttelettes est généralement supérieure à 1 µm), soit un aérosol formé de gouttelettes obtenues par cisaillement mécanique d’un liquide par atomisation, nébulisation, bullage ou vaporisation (dans ce cas, la taille des gouttelettes peut varier considérablement, généralement entre 2 µm et plus de 50 µm). On parle parfois aussi de nuage (acides, encres).
Le terme smog est un terme populaire désignant un brouillard épais formé d’aérosols polluants résultant d’une combinaison de particules de fumée et de gouttes d’eau. On l’utilise couramment pour désigner les pollutions atmosphériques mixtes dans les régions industrielles et humides.
L’expression noyaux de condensation (NC) ou d’Aitken désigne des particules atmosphériques très petites (généralement inférieures à 0,1 µm) formées par des processus de combustion et par conversion chimique de précurseurs gazeux.
L’expression mode d’accumulation s’applique aux particules de l’atmosphère ambiante dont le diamètre est compris entre 0,1 et 1 µm environ. Ces particules sont généralement sphériques (leur surface étant liquide) et sont formées par coagulation et condensation de particules plus petites provenant de précurseurs gazeux. Trop grandes pour permettre une coagulation rapide et trop petites pour une sédimentation efficace, elles ont tendance à s’accumuler dans l’air ambiant.
L’expression mode particulaire grossier s’applique aux particules en suspension dans l’air ayant un diamètre aérodynamique supérieur à 2,5 µm; elles sont généralement formées par des processus mécaniques avant d’être remises en suspension après s’être déposées.
Les réponses aux polluants atmosphériques vont de simples nuisances à la nécrose tissulaire et à la mort, d’effets systémiques généralisés à des agressions spécifiques touchant tel ou tel tissu. Des facteurs liés à l’hôte et à l’environnement permettent de modifier les effets des substances chimiques inhalées, la réponse finale étant le résultat de leur interaction. Les principaux facteurs liés à l’hôte sont:
Les facteurs environnementaux sont la concentration, la stabilité et les propriétés physico-chimiques de l’agent dans l’environnement, outre la durée et la fréquence de l’exposition, ainsi que la voie de pénétration de l’agent. Les expositions aiguës et chroniques à une substance chimique peuvent entraîner des manifestations pathologiques différentes.
Chaque organe ne peut répondre que d’un nombre restreint de façons, mais les étiquettes diagnostiques pour les maladies qui en résultent sont nombreuses. Les paragraphes qui suivent décrivent les grands types de réponses de l’appareil respiratoire succédant à une exposition à des polluants environnementaux.
Les agents irritants provoquent une inflammation tissulaire généralisée, non spécifique, qui peut aboutir à la destruction de la zone en contact avec l’agent contaminant. Certains agents irritants ne génèrent pas d’effets systémiques du fait que la réponse qu’ils provoquent prédomine nettement sur les effets systémiques, alors que d’autres ont également des effets systémiques marqués après leur absorption — c’est le cas, par exemple, de l’hydrogène sulfuré absorbé par les poumons.
A des degrés de concentration élevés, les agents irritants peuvent entraîner une sensation de brûlure du nez et de la gorge (et généralement aussi des yeux), des douleurs thoraciques et une toux provoquant une inflammation des muqueuses (trachéite, bronchite). Parmi les principaux agents irritants, on peut citer des gaz comme le chlore, le fluor, le dioxyde de soufre, le phosgène et les oxydes d’azote; les brouillards d’acides ou de bases; les fumées de cadmium; les poussières de chlorure de zinc et de pentoxyde de vanadium. Des concentrations élevées de substances chimiques irritantes peuvent également pénétrer profondément dans les poumons et provoquer un œdème pulmonaire (les alvéoles se remplissent de liquide) ou une inflammation (pneumopathie chimique).
Des concentrations très élevées de poussières dénuées de propriétés chimiques irritantes peuvent toutefois causer une irritation purement mécanique des bronches et, après leur passage dans l’appareil digestif, contribuer au développement d’un cancer de l’estomac ou du côlon.
L’exposition à des agents irritants peut entraîner la mort en cas d’atteinte sévère d’organes vitaux. Dans certains cas, les lésions peuvent être réversibles ou induire une altération fonctionnelle permanente, telle qu’une altération des échanges gazeux.
Un certain nombre de types de poussières sont la cause de diverses affections pulmonaires appelées pneumoconioses. Ce terme général englobe de nombreux états de fibrose pulmonaire, c’est-à-dire de maladies caractérisées par la formation de cicatrices dans le tissu conjonctif interstitiel. Les pneumoconioses sont dues à l’inhalation et à la rétention sélective de certaines poussières dans les alvéoles, au niveau desquelles elles sont soumises à un processus de séquestration interstitielle.
Les pneumoconioses se caractérisent par des lésions fibreuses spécifiques dont le type et les modalités évolutives diffèrent selon le genre de poussière en cause. Par exemple, la silicose due à la déposition de silice non cristalline se caractérise par une fibrose de type nodulaire, alors que dans le cas de l’asbestose, due à l’exposition aux fibres d’amiante, il s’agit d’une fibrose diffuse. Certaines poussières, telles que l’oxyde de fer, ne provoquent que des anomalies radiologiques (sidérose), sans troubles fonctionnels, tandis que les effets de certaines autres vont de l’incapacité légère à la mort.
Les réponses allergiques font intervenir le phénomène dit de sensibilisation. L’exposition initiale à un allergène entraîne l’induction de la formation d’anticorps; les expositions ultérieures du sujet désormais «sensibilisé» déclenchent une réaction immunitaire — c’est-à-dire une réaction antigène-anticorps (l’antigène est l’allergène combiné avec une protéine endogène). Cette réaction immunitaire peut se produire immédiatement après l’exposition à l’allergène ou peut être retardée.
Les réactions allergiques respiratoires primaires sont l’asthme bronchique, les réactions des voies respiratoires supérieures impliquant une libération de médiateurs du genre histamine à la suite de réactions immunitaires de la muqueuse, et un type de pneumopathie (inflammation pulmonaire) connu sous le nom d’alvéolite allergique extrinsèque. Outre ces réactions locales, une réaction allergique systémique (choc anaphylactique) peut succéder à une exposition à certains allergènes chimiques.
Des agents infectieux peuvent entraîner des cas de tuberculose, d’infection charbonneuse, d’ornithose, de brucellose, d’histoplasmose, de maladie des légionnaires (légionnellose), etc.
Le cancer est un terme général désignant une série de maladies apparentées caractérisées par la croissance désordonnée de certains tissus. Son développement est dû à un processus complexe faisant intervenir de multiples facteurs chez l’hôte et dans l’environnement.
L’une des principales difficultés rencontrées lorsqu’on essaie d’établir un lien entre l’exposition à un agent spécifique et le développement d’un cancer chez l’humain est la durée de la période de latence, qui est généralement de quinze à quarante ans; c’est la période qui s’écoule entre le début de l’exposition et les premières manifestations de la maladie.
Parmi les polluants atmosphériques capables d’induire un cancer, il faut citer l’arsenic et ses dérivés, les chromates, la silice, les particules contenant des hydrocarbures aromatiques polycycliques et certaines poussières contenant du nickel. Les fibres d’amiante peuvent induire un cancer bronchique et un mésothéliome pleural ou péritonéal. Enfin, des particules radioactives déposées peuvent exposer le tissu pulmonaire à des doses locales élevées de rayonnements ionisants et être à l’origine d’un cancer.
De nombreuses substances chimiques présentes dans l’environnement peuvent entraîner une maladie systémique généralisée par leurs effets sur un certain nombre d’organes. Les poumons ne sont pas seulement l’organe cible de nombreux agents nocifs, ils sont aussi la porte d’entrée de substances toxiques qui les traversent et pénètrent dans la circulation sanguine sans occasionner de lésions pulmonaires. Néanmoins, quand ces substances en circulation atteignent certains organes, elles peuvent les léser ou provoquer une infection générale qui sera à son tour responsable d’effets systémiques. Ce rôle des poumons dans la pathologie professionnelle sort du cadre du présent article. Il convient cependant de mentionner l’effet de particules finement dispersées (fumées) de plusieurs oxydes métalliques souvent associés à un syndrome systémique aigu connu sous le nom de fièvre des métaux ou fièvre des fondeurs.
La fonction respiratoire peut être mesurée de multiples façons. Il convient cependant de bien définir le but des mesures avant tout examen si l’on veut pouvoir interpréter correctement les résultats. Dans le présent article, nous allons évoquer l’étude de la fonction respiratoire en mettant l’accent sur l’aspect professionnel. Il est important de se souvenir des limites des différentes mesures de la fonction considérée. Les effets transitoires aigus sur la fonction respiratoire peuvent passer inaperçus en cas d’exposition à des poussières fibrogènes comme le quartz et l’amiante, ce qui n’est pas le cas des effets chroniques résultant d’une exposition prolongée (> 20 ans). Ce phénomène est dû au fait que les effets chroniques apparaissent plusieurs années après l’inhalation des poussières et leur dépôt dans les poumons. Par contre, les effets transitoires aigus des poussières organiques et inorganiques — ainsi que ceux des moisissures, des fumées de soudage et des gaz d’échappement des moteurs — se prêtent parfaitement à l’étude, du fait que l’effet irritant de ces poussières apparaît déjà au bout de quelques heures d’exposition. Il est également possible de déceler des effets aigus ou chroniques sur la fonction respiratoire en cas d’exposition à des concentrations de certains gaz irritants (dioxyde d’azote, aldéhydes, acides et chlorures d’acides) proches des limites d’exposition, en particulier si leurs effets sont potentialisés par une contamination de l’air par des particules.
Les examens de la fonction respiratoire doivent être sans danger pour les sujets examinés et le matériel utilisé doit être sûr pour l’examinateur. Les spécifications propres aux différents types de matériel de mesure de la fonction respiratoire ont été citées brièvement dans certaines études (par exemple, Quanjer et coll., 1993). Bien entendu, les appareils doivent être calibrés conformément à des étalons indépendants, ce qui n’est pas toujours facile, surtout lorsqu’il s’agit de matériel informatisé. Les résultats des épreuves fonctionnelles respiratoires dépendent à la fois du sujet et de l’examinateur. Pour que l’examen donne des résultats satisfaisants, les techniciens doivent avoir été dûment formés et être capables de fournir des instructions claires au sujet et de l’inciter à subir correctement les épreuves. L’investigateur doit par ailleurs avoir une bonne connaissance des voies respiratoires et des poumons afin d’interpréter correctement les résultats obtenus. Il est recommandé d’utiliser des méthodes ayant un taux de reproductibilité inter- et intra-individuelle assez élevé. La reproductibilité peut se refléter dans le coefficient de variation, c’est-à-dire l’écart-type multiplié par 100 et divisé par la valeur moyenne. Des valeurs inférieures à 10% sont considérées comme acceptables dans le cas de plusieurs mesures effectuées sur un même sujet.
Pour savoir si les valeurs obtenues sont pathologiques ou non, il faut les comparer à des valeurs théoriques. Les équations prédictives concernant les variables spirométriques reposent généralement sur l’âge et la taille, avec une répartition en fonction du sexe. Les valeurs moyennes caractérisant la fonction respiratoire sont plus élevées chez les hommes que chez les femmes de même âge et de même taille. Cette fonction se dégrade avec l’âge et augmente avec la taille. Un sujet de grande taille aura donc un volume pulmonaire supérieur à celui d’un sujet de petite taille ayant le même âge. Le résultat des équations prédictives peut varier considérablement d’une population repère à l’autre. Les variations d’âge et de taille dans la population repère influeront également sur les valeurs attendues. Cela signifie, par exemple, qu’il ne faut pas utiliser une équation prédictive si l’âge ou la taille du sujet se situent hors de l’intervalle fixé pour la population ayant servi à définir l’équation prédictive.
Le tabagisme altère aussi la fonction pulmonaire et cette altération peut être potentialisée chez les sujets professionnellement exposés à des substances irritantes. On conclut généralement au caractère non pathologique des épreuves fonctionnelles respiratoires si les valeurs obtenues ne s’écartent pas de plus de 80% de la valeur théorique fournie par une équation prédictive.
Les épreuves fonctionnelles respiratoires ont pour but d’évaluer l’état des poumons. Les mesures peuvent porter sur un seul ou plusieurs paramètres ventilatoires, ou sur les propriétés dynamiques des voies respiratoires et des poumons. Dans ce dernier cas, ces propriétés sont généralement évaluées au cours d’épreuves d’effort. L’état pulmonaire peut également être évalué à partir de ses fonctions physiologiques, à savoir la capacité de diffusion, la résistance des voies respiratoires et la compliance (voir ci-après).
Les mesures relatives à la capacité respiratoire sont obtenues par spirométrie. La manœuvre ventilatoire consiste généralement en une inspiration forcée suivie d’une expiration forcée; elle fournit la capacité vitale (CV, mesurée en litres). Il convient d’effectuer au moins trois enregistrements corrects (c’est-à-dire inspiration complète et une expiration d’effort sans pertes observables), en retenant la valeur la plus élevée. Le volume peut être mesuré de façon directe, à l’aide d’une cloche à eau ou de faible résistance, ou de façon indirecte avec un pneumotachographe (intégration d’un signal de débit en fonction du temps). Il convient de rappeler que tous les volumes pulmonaires mesurés doivent être exprimés dans les conditions BTPS, c’est-à-dire température corporelle et pression ambiante saturée en vapeur d’eau.
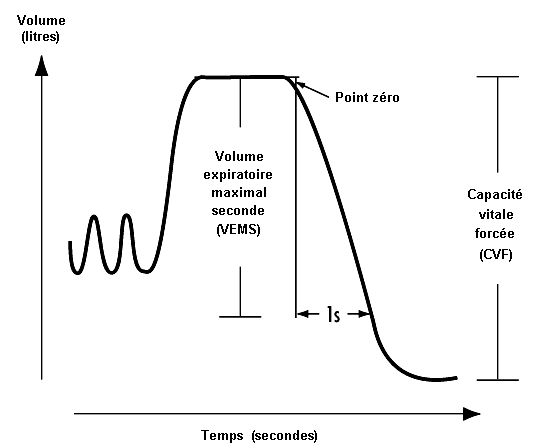
La capacité vitale expiratoire forcée (CVF, en litres) correspond au volume d’air expiré avec un effort expiratoire maximal. En raison de la simplicité de l’épreuve et du coût relativement faible du matériel utilisé, le spirogramme expiratoire forcé est devenu un élément majeur de la surveillance de la fonction respiratoire. Il a cependant donné lieu à de nombreux tracés de qualité médiocre et d’un intérêt douteux. Pour obtenir des résultats satisfaisants, on peut s’appuyer sur la directive concernant l’enregistrement et l’interprétation du tracé d’expiration forcée remise à jour et publiée par la Société américaine de chirurgie thoracique (American Thoracic Society) en 1987 (ATS, 1987).
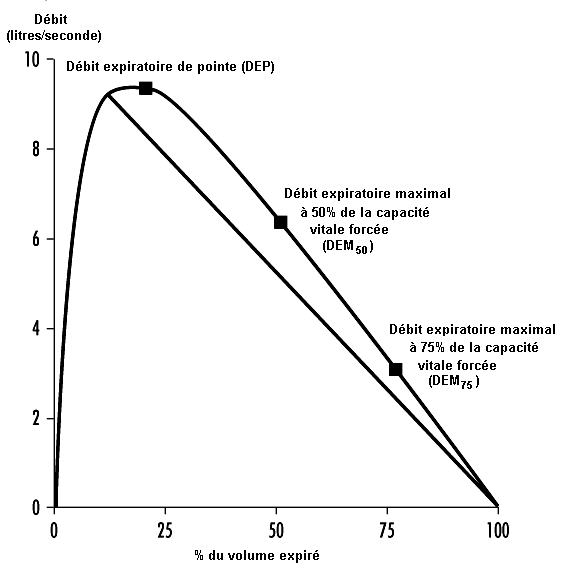
Il est possible de mesurer des débits instantanés à l’aide de courbes débit-volume ou débit-temps, en prélevant les valeurs moyennes du débit en fonction du temps sur le spirogramme. Les variables associées qu’il est possible de calculer à partir du spirogramme expiratoire forcé sont le volume expiratoire maximal seconde (VEMS, en litres par seconde) — ou en pourcentage de la CVF (VEMS%) — , le débit expiratoire de pointe (DEP, l/s), les débits expiratoires maximaux à 50% et 75% de la CVF (DEM50 et DEM75 respectivement). La figure10.5 illustre la détermination du VEMS à partir du spirogramme. Chez des sujets sains, les débits maximaux mesurés pour d’importants volumes pulmonaires (c’est-à-dire en début d’expiration) reflètent essentiellement les caractéristiques de l’écoulement dans les voies respiratoires de gros calibre, alors que ceux mesurés pour de petits volumes pulmonaires (c’est-à-dire en fin d’expiration) sont généralement considérés comme un reflet des caractéristiques des bronchioles (voir figure 10.6). Dans celles-ci, l’écoulement est laminaire, alors que dans les grosses voies respiratoires, il peut être de type turbulent.
Le DEP peut également être mesuré à l’aide d’un petit appareil portable comme celui qui a été mis au point par Wright en 1959. Cet appareil a l’avantage de permettre au patient d’effectuer des mesures en série, notamment à son poste de travail. Cependant, pour que les tracés soient interprétables, les patients doivent recevoir une formation appropriée. Il faut également se rappeler que les mesures du DEP effectuées par exemple avec l’appareil de Wright et celles obtenues par la méthode classique, c’est-à-dire par spirométrie, ne peuvent être comparées du fait que les techniques ventilatoires sont différentes.
Certaines variables spirométriques (CV, CVF et VEMS) varient légèrement d’un sujet à l’autre, 60 à 70% de cette variation s’expliquant par l’âge, la taille et le sexe. Les troubles restrictifs respiratoires donneront des valeurs plus basses de la CV, de la CVF et du VEMS. Les mesures des débits expiratoires présentent d’importants écarts individuels, les débits mesurés dépendant à la fois de l’effort et du temps. Cela signifie, par exemple, qu’un sujet aura un débit très élevé en cas de réduction du volume pulmonaire. En revanche, le débit pourra être extrêmement faible en cas de volume pulmonaire très important. En règle générale, cependant, le débit sera généralement réduit en présence de maladies obstructives chroniques (asthme, bronchite chronique).
Le volume résiduel (VR), c’est-à-dire le volume d’air demeurant dans les poumons après une expiration maximale, peut être déterminé par dilution gazeuse ou par pléthysmographie. La technique de dilution gazeuse nécessite un matériel plus simple et est donc plus facile à utiliser dans les études réalisées sur le terrain. La figure 10.7 expose le principe de cette technique, qui repose sur la dilution d’un gaz indicateur dans un circuit fermé. Le gaz en question doit être faiblement soluble dans les tissus biologiques de façon à ne pas être capté par les tissus et le sang pulmonaires. On avait recours au début à de l’hydrogène, mais, en raison du risque de formation de mélanges explosifs avec l’air, il a été remplacé par l’hélium, facilement détecté par le principe de la conductivité thermique.
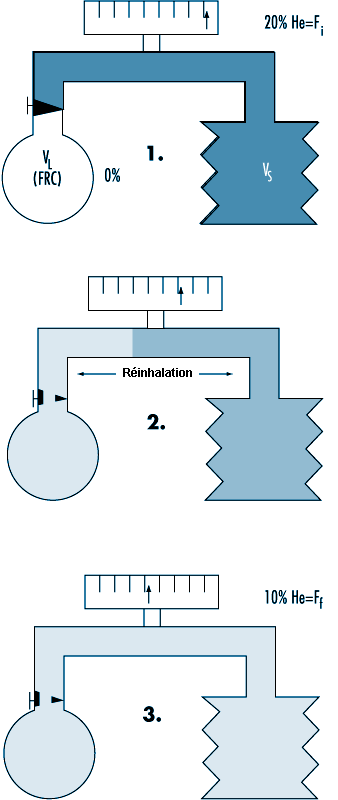
Le sujet et l’appareil forment un système clos; la concentration initiale du gaz diminue donc au fur et à mesure de sa dilution dans le volume gazeux pulmonaire. A l’état d’équilibre, la concentration du gaz indicateur est la même dans les poumons et dans l’appareil et la capacité résiduelle fonctionnelle (CRF) peut être calculée à partir de l’équation:
CRF = VL = [(VS × Fi) / Ff] – VS
où VS est le volume du spiromètre (y compris le mélange gazeux ajouté dans l’appareil), VL le volume pulmonaire, Fi la concentration initiale du gaz et Ff sa concentration finale.
Deux ou trois mesures de la CV permettent d’obtenir une valeur fiable de la capacité pulmonaire totale (la CPT, en litres). Les différents volumes pulmonaires sont indiqués dans la figure 10.8.
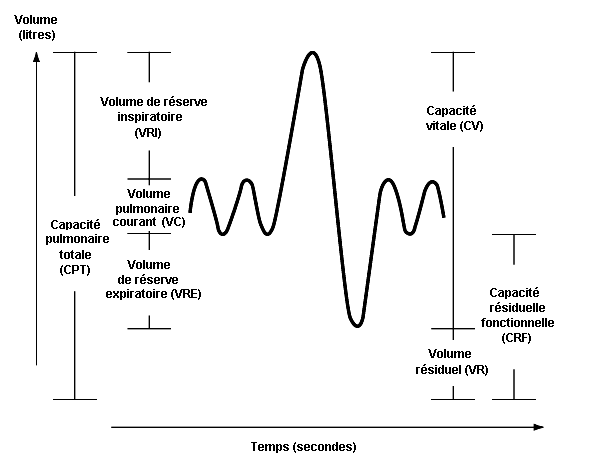
Le VR et la CRF augmentent avec l’âge, à la suite des modifications des propriétés élastiques des voies respiratoires. Dans le cas des maladies obstructives chroniques, on observe généralement des valeurs accrues du VR et de la CRF, tandis que la CV est diminuée. Cependant, chez les sujets dont certaines régions pulmonaires sont mal ventilées — par exemple les emphysémateux —, la technique de la dilution gazeuse peut sous-estimer le VR, la CRF et la CPT, car le gaz indicateur ne peut communiquer avec les voies collapsées, si bien que la diminution de sa concentration sera exagérée.
Il est possible d’obtenir une mesure de l’occlusion des voies aériennes et de la distribution des gaz dans les poumons en une seule et même manœuvre par l’étude des variations de la concentration d’un gaz marqueur au cours d’un cycle ventilatoire unique (voir figure 10.9). Le matériel comporte un spiromètre relié à un ballonnet placé dans une enceinte et un enregistreur continu de la concentration d’azote. La manœuvre consiste en une inspiration forcée d’oxygène pur provenant du ballonnet. Au début de l’expiration, la concentration d’azote augmente par suite de la vidange de l’espace mort du sujet qui contient de l’oxygène pur. L’expiration se poursuit avec l’air provenant des voies respiratoires et des alvéoles. Enfin, l’air alvéolaire, qui contient de 20 à 40% d’azote, est expiré. Quand l’expiration de l’air provenant de la base des poumons augmente, la concentration d’azote augmente brusquement s’il y a occlusion des voies respiratoires dans les régions pulmonaires concernées (voir figure 10.9). Le volume au-delà du VR, pour lequel les voies respiratoires se ferment au cours de l’expiration, est le volume de fermeture (VF), que l’on exprime généralement en pourcentage de la CV (VF%). La distribution de l’air inspiré dans les poumons est exprimée par la pente du plateau alvéolaire (%N2 ou phase III, %N2/l). On l’obtient en divisant la différence de concentration de l’azote entre le point correspondant à 30% du volume d’air expiré et le point où se produit l’occlusion des voies respiratoires par le volume correspondant.
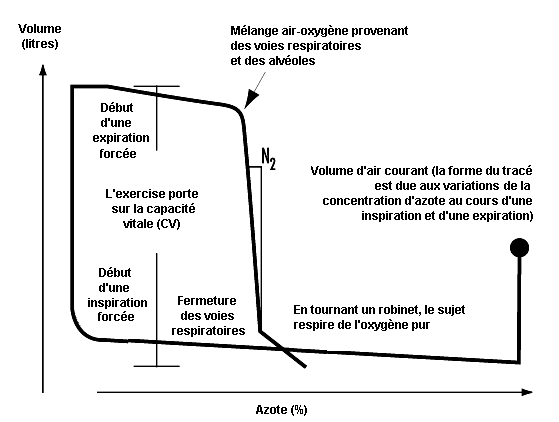
Le vieillissement de même que les troubles obstructifs chroniques entraînent une augmentation des valeurs du VF% et de la phase III. Cependant, même les sujets sains n’ont pas une distribution homogène des gaz dans les poumons, ce qui se traduit par des valeurs légèrement élevées en phase III, c’est-à-dire de 1 à 2% N2/l. On considère que les variables VF% et phase III reflètent les conditions régnant dans les voies respiratoires périphériques de petit calibre, d’un diamètre interne inférieur à 2 mm environ. Normalement, les voies respiratoires périphériques contribuent pour une petite partie (10 à 20%) à la résistance totale des voies aériennes. Des anomalies extrêmement importantes, qui ne sont pas décelables par les épreuves fonctionnelles respiratoires classiques, telles que la spirométrie dynamique, peuvent s’installer, par exemple à la suite d’une exposition à des substances irritantes de l’air présent dans les voies respiratoires périphériques. Cela semble indiquer que l’obstruction des voies respiratoires commence au niveau des voies aériennes de petit calibre. Les résultats de certaines études ont également signalé l’existence d’anomalies dans VF% et la phase III avant toute modification de la spirométrie statique ou dynamique. Ces anomalies précoces peuvent régresser en cas d’arrêt de l’exposition aux agents dangereux.
Le facteur de transfert pulmonaire (mmol/min; kPa) est une expression de la capacité de diffusion du transport de l’oxygène dans les capillaires pulmonaires. Ce facteur peut être déterminé à l’aide de techniques utilisant des cycles respiratoires uniques ou multiples; on estime que c’est la technique du cycle ventilatoire unique qui convient le mieux aux études menées sur le terrain. On se sert du monoxyde de carbone (CO), car la pression de retour du CO est très basse dans le sang périphérique, à la différence de celle de l’oxygène. La fixation du CO est censée suivre un modèle exponentiel, et cette hypothèse peut être utilisée pour déterminer le facteur de transfert des poumons.
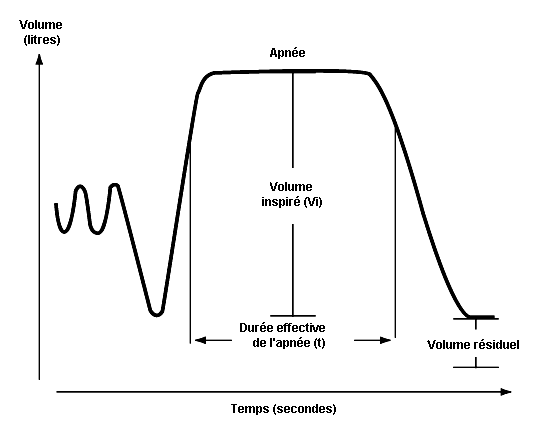
La détermination de TLCO (facteur de transfert du CO) est réalisée grâce à une manœuvre ventilatoire comportant une expiration forcée, suivie d’une inspiration forcée d’un mélange gazeux formé de monoxyde de carbone, d’hélium, d’oxygène et d’azote. A une phase d’apnée succède une expiration forcée qui reflète le contenu de l’air alvéolaire (voir figure 10.10). L’hélium est utilisé pour déterminer le volume alvéolaire (VA). En supposant que l’hélium et le CO ont la même dilution, il est possible de calculer la concentration initiale du CO avant le début de la diffusion. TLCO se calcule grâce à l’équation ci-dessous, dans laquelle k dépend de la dimension des éléments, t est la durée effective d’apnée et log est le logarithme de base 10. Le volume inspiré est Vi et les fractions F du CO et de l’hélium (He) sont désignées par i et a, respectivement pour l’air inspiré et l’air alvéolaire.
TLCO = k Vi (Fa,He / Fi,He) log (Fi,CO Fa,He / Fa,CO Fi,He) (t)-1
La valeur de TLCO dépendra d’un certain nombre de conditions — par exemple, la quantité d’hémoglobine disponible, le volume des alvéoles ventilées et des capillaires pulmonaires perfusés et le rapport ventilation/perfusion. Les valeurs de TLCO s’abaissent avec l’âge et s’élèvent avec l’activité physique et quand les volumes pulmonaires sont augmentés. On observe une diminution de TLCO en présence de syndromes restrictifs ou obstructifs.
La compliance (l/kPa) est une fonction, entre autres, de la propriété élastique des poumons. Les poumons ont une tendance intrinsèque à se rétracter, c’est-à-dire à collaber. La force nécessaire au maintien de l’expansion pulmonaire dépend de l’élasticité du tissu pulmonaire, de la tension superficielle au niveau des alvéoles et de la musculature bronchique. Par ailleurs, la paroi thoracique a tendance à se dilater jusqu’à des volumes pulmonaires dépassant la CRF de 1 à 2 litres. Pour les volumes pulmonaires supérieurs, une force doit être appliquée pour permettre une nouvelle expansion de la paroi thoracique. A la valeur de la CRF, la tendance des poumons à se rétracter est contrebalancée par la tendance du thorax à se dilater. C’est pourquoi on considère que la CRF correspond à la position de repos du poumon.
La compliance pulmonaire est définie par le quotient de la variation du volume et de la pression transpulmonaire (c’est-à-dire la différence entre les pressions mesurées au niveau de la bouche — pression atmosphérique — et des poumons à la suite d’une manœuvre respiratoire). La mesure des pressions intrapulmonaires est délicate; on la remplace par la mesure de la pression intra-œsophagienne. Celle-ci est pratiquement la même que la pression intrapulmonaire; on la mesure à l’aide d’une fine sonde en polyéthylène munie d’un ballonnet couvrant les 10 derniers centimètres. Au cours des manœuvres inspiratoires et expiratoires, les variations de volume et de pression sont enregistrées respectivement au moyen d’un spiromètre et d’un manomètre. Lorsque les mesures sont effectuées pendant un cycle respiratoire normal, la compliance dynamique peut être mesurée. On obtient la compliance statique au cours d’une manœuvre de CV lente. Dans ce dernier cas, les mesures sont effectuées à l’aide d’un pléthysmographe et l’expiration est interrompue par intermittence au moyen d’un obturateur. Les mesures de la compliance sont cependant difficiles à effectuer lorsqu’on étudie les effets d’une exposition donnée sur la fonction respiratoire sur le terrain; c’est une technique qui convient mieux au laboratoire.
On observe une diminution de la compliance (c’est-à-dire une augmentation de l’élasticité) dans la fibrose. Les variations de pression nécessaires pour induire des variations de volume doivent alors être plus importantes. Par ailleurs, on observe une compliance élevée, par exemple dans l’emphysème, à la suite d’une disparition de tissu élastique et, par conséquent, d’une diminution de l’élasticité pulmonaire.
La résistance des voies respiratoires dépend essentiellement du rayon et de la longueur des voies aériennes, mais aussi de la viscosité de l’air. Cette résistance (RL en (kPa/l)/s) peut être déterminée à l’aide d’un spiromètre, d’un manomètre et d’un pneumotachographe (pour mesurer le débit). Les mesures peuvent également s’effectuer à l’aide d’un pléthysmographe qui permet d’enregistrer les variations de débit et de pression au cours des épreuves de respiration rapide. L’administration d’un médicament destiné à provoquer une bronchoconstriction permet d’identifier les sujets sensibles grâce à l’hyperréactivité de leurs voies respiratoires. Les asthmatiques présentent généralement des valeurs de RL plus élevées.
La mesure de la fonction respiratoire permet de déceler l’effet d’une exposition professionnelle sur les poumons. Les examens effectués lors de l’embauche ne devraient pas être utilisés pour exclure des candidats à un emploi; en effet, la fonction pulmonaire de sujets sains varie énormément et il est difficile de fixer une limite en deçà de laquelle il est admis avec certitude que le poumon est malade. Une autre raison est que l’environnement professionnel devrait être d’une qualité suffisante pour permettre même aux sujets présentant de légers troubles fonctionnels respiratoires de travailler dans de bonnes conditions.
Les troubles pulmonaires chroniques chez des sujets professionnellement exposés peuvent être décelés de différentes façons. Les techniques d’exploration pulmonaire sont conçues pour déterminer les effets antérieurs à la mesure et les résultats ne peuvent guère servir à déterminer comment empêcher une dégradation fonctionnelle ultérieure. C’est pourquoi on procède volontiers à une comparaison des valeurs réellement mesurées chez les sujets exposés avec les valeurs de la fonction respiratoire obtenues dans une population de référence exempte de toute exposition professionnelle. Les sujets témoins peuvent être recrutés dans les mêmes entreprises, à proximité de celles-ci ou dans la même ville.
On a eu recours également à l’analyse multidimensionnelle dans certaines études pour évaluer les écarts entre les sujets exposés et des témoins non exposés ayant des caractéristiques similaires. Les valeurs de la fonction respiratoire chez les sujets exposés peuvent aussi être normalisées grâce à une équation de référence basée sur les valeurs de cette fonction chez les sujets non exposés.
Une autre méthode consiste à étudier la différence entre les valeurs de la fonction respiratoire chez des travailleurs exposés et non exposés après ajustement en fonction de l’âge et de la taille à l’aide de valeurs de référence externes, déterminées au moyen d’une équation prédictive basée sur des sujets sains. On peut aussi apparier la population de référence aux sujets exposés selon l’appartenance ethnique, le sexe, l’âge, la taille et le tabagisme afin d’atténuer l’effet des divers facteurs susceptibles d’agir sur la fonction pulmonaire.
Le problème demeure cependant de décider si une diminution de la fonction respiratoire est suffisamment importante pour être jugée pathologique quand on utilise des valeurs de référence externes. Bien que les instruments employés soient portables et relativement simples, il convient de prêter attention à la sensibilité des méthodes choisies pour déceler de petites anomalies des voies respiratoires et des poumons, ainsi qu’à la possibilité de combiner différentes techniques. Certaines observations indiquent que les sujets ayant des troubles respiratoires tels qu’une dyspnée d’effort présentent davantage de risques de déclin rapide de leur fonction pulmonaire. La présence de symptômes respiratoires est donc importante et ne devrait pas être négligée.
Le sujet peut également être suivi à l’aide d’examens spirométriques réalisés par exemple annuellement pendant un certain nombre d’années. Les résultats serviront d’avertissement quant à l’évolution de la maladie. Cette méthode a cependant des limites, car elle demande beaucoup de temps et la fonction pulmonaire pouvait être déjà altérée de manière définitive au moment où une anomalie a été constatée. Son application ne doit donc pas décourager la mise en place de moyens techniques destinés à réduire les concentrations dangereuses de polluants atmosphériques.
Enfin, les effets chroniques sur la fonction respiratoire peuvent aussi être étudiés en analysant pendant un certain nombre d’années les variations individuelles de cette fonction respiratoire chez des sujets exposés et non exposés. Cette conception d’étude longitudinale offre l’avantage d’éliminer la variabilité d’un sujet à l’autre, mais son application est coûteuse en temps et en argent.
Les sujets sensibles peuvent également être recherchés en comparant leur fonction respiratoire avec et sans exposition au cours de leur travail. Pour réduire autant que possible les éventuels effets des variations circadiennes, on procède aux mesures à la même heure de la journée pendant une exposition et à un moment sans exposition. L’absence d’exposition peut être réalisée, par exemple, en transférant de temps en temps le sujet dans une zone non contaminée ou en lui faisant porter un appareil de protection respiratoire pendant toute la durée de son poste de travail; dans certains cas, on peut procéder aux mesures de la fonction respiratoire dans l’après-midi d’un jour de repos du travailleur.
Les effets transitoires, mais répétés, posent un problème particulier, car ils peuvent aboutir à des effets chroniques. Une altération transitoire aiguë de la fonction respiratoire peut non seulement être un indice d’exposition biologique, mais aussi un facteur pronostique d’une altération fonctionnelle respiratoire chronique. L’exposition à des polluants atmosphériques peut entraîner des effets aigus détectables sur la fonction respiratoire, même si les concentrations moyennes des polluants en question sont inférieures aux limites admissibles. Il faut alors se demander si ces effets sont réellement néfastes à long terme. Il est difficile de répondre directement à cette question, en particulier parce que la pollution atmosphérique dans les lieux de travail a une composition souvent complexe et parce que l’exposition ne peut être définie par la concentration moyenne de chaque substance. L’effet d’une exposition professionnelle tient également en partie à la sensibilité du sujet. Ainsi, certains sujets réagiront plus tôt ou davantage que d’autres. On ne connaît cependant pas bien les mécanismes physiopathologiques sous-tendant les altérations transitoires aiguës de la fonction respiratoire. Il n’en reste pas moins que les réactions indésirables à l’exposition à un polluant atmosphérique irritant constituent une mesure objective, contrairement aux manifestations subjectives que sont les symptômes de diverses origines.
L’avantage d’une détection des anomalies précoces des voies respiratoires et des poumons provoquées par les polluants atmosphériques dangereux est évident: l’exposition prédominante peut être réduite afin de prévenir des affections plus graves. Dans ce contexte, un objectif important est donc d’utiliser la mesure des effets aigus transitoires sur la fonction respiratoire comme un système d’alarme sensible et précoce, quand on étudie des groupes de travailleurs sains.
Les signes d’irritation sont l’un des principaux critères utilisés pour établir les limites d’exposition. Il n’est cependant pas certain que le respect d’une limite d’exposition basée sur l’irritation puisse protéger efficacement contre l’apparition d’effets irritants. Il faut tenir compte du fait qu’une limite d’exposition à un polluant atmosphérique comporte généralement deux volets au moins: une valeur moyenne pondérée dans le temps (TWAL) et une limite d’exposition à court terme (STEL), ou tout au moins des règles en cas de dépassement de la valeur moyenne d’exposition, à savoir des «limites d’excursion». Dans le cas de substances fortement irritantes telles que le dioxyde de soufre, l’acroléine ou le phosgène, il est important de limiter la concentration, même pendant de très courtes périodes; on fixe donc généralement des limites d’exposition professionnelle sous la forme de valeurs plafonds, avec une période d’échantillonnage aussi brève que le permettent les dispositifs de mesure.
Des limites moyennes d’exposition pondérées dans le temps et valables pour une journée de travail de huit heures, combinées à des règles en cas de dépassement de ces moyennes, sont, pour la plupart des substances, fournies dans la liste des valeurs seuils (TLV) de la Conférence américaine des hygiénistes industriels gouvernementaux (American Conference of Governmental Industrial Hygienists (ACGIH)). La liste des TLV de 1993-94 renferme le texte suivant relatif aux fluctuations (limites d’excursion) admissibles au-delà des valeurs limites:
Pour l’immense majorité des substances ayant une TLV-TWA, on ne dispose d’aucune donnée toxicologique suffisante pour garantir une limite d’exposition à court terme. Néanmoins, les dépassements de la TLV-TWA doivent être contrôlés, même si la TWA pour un poste de huit heures reste dans les limites recommandées.
Les mesures de l’exposition à des polluants atmosphériques connus et leur comparaison avec des limites d’exposition bien documentées devraient être effectuées systématiquement. Il existe cependant de nombreuses situations dans lesquelles la détermination du respect des limites d’exposition ne suffit pas, notamment dans les circonstances suivantes:
Comme nous l’avons mentionné plus haut, la mesure des effets aigus transitoires sur la fonction respiratoire peut servir dans ces cas d’avertissement d’un risque de surexposition à des agents irritants.
Dans les cas 2) et 3), les effets aigus transitoires sur la fonction respiratoire peuvent également servir à tester l’efficacité des mesures de prévention visant à réduire l’exposition à la pollution de l’air ou dans des études scientifiques, par exemple pour rattacher des effets biologiques à des composants de polluants atmosphériques. Un certain nombre d’exemples suivent, dans lesquels les effets aigus transitoires sur la fonction respiratoire ont été étudiés avec succès en médecine du travail.
On a signalé, vers la fin de 1950, une altération transitoire de la fonction respiratoire, d’origine professionnelle, au cours d’un poste de travail chez des travailleurs de l’industrie du coton. Par la suite, plusieurs auteurs ont décrit des altérations aiguës transitoires d’origine professionnelle parmi les travailleurs du chanvre et du textile, les mineurs de charbon, les travailleurs exposés au diisocyanate de toluylène, les sapeurs-pompiers, les travailleurs de l’industrie du caoutchouc, les mouleurs et les noyauteurs, les soudeurs, les farteurs de skis, les travailleurs exposés aux poussières organiques et aux agents irritants des peintures à l’eau.
Dans plusieurs cas, cependant, les mesures effectuées avant et après l’exposition — généralement pendant un poste de travail — n’ont pas permis de déceler d’effets aigus, malgré l’intensité de l’exposition. Cela est dû probablement à l’effet des variations circadiennes normales, surtout en ce qui concerne les variables de la fonction respiratoire dépendant du calibre des voies aériennes. La diminution transitoire de ces variables doit donc être supérieure à la variation circadienne normale pour pouvoir être décelée. Toutefois, il est possible de contourner la difficulté en mesurant chaque fois la fonction respiratoire au même moment de la journée. En employant le sujet exposé comme son propre témoin, il est possible de réduire encore la variation interindividuelle. Cette formule a été appliquée à des soudeurs et, bien que l’écart moyen entre les valeurs de la CVF chez les sujets exposés et non exposés ait été inférieur à 3% chez 15 soudeurs, cet écart a été significatif dans l’intervalle de confiance à 95% avec une puissance supérieure à 99%.
Les effets transitoires réversibles sur les poumons peuvent servir d’indice d’exposition à des polluants irritants complexes. Dans l’étude citée plus haut, les particules présentes dans l’environnement professionnel ont joué un rôle majeur dans les effets irritants sur les voies respiratoires et les poumons. Ces particules ont été captées grâce à un appareil de protection respiratoire à filtre monté sur le casque de soudage. Les résultats ont montré que les effets sur les poumons étaient dus aux particules présentes dans les fumées de soudage et que le problème pouvait être résolu au moyen d’un filtre particulaire.
L’exposition aux gaz d’échappement des moteurs diesel entraîne également des effets irritants mesurables sur les poumons, qui se traduisent par une altération transitoire aiguë de la fonction respiratoire. Le montage de filtres mécaniques sur les tuyaux d’échappement des camions utilisés par des dockers pour des opérations de transbordement a permis d’atténuer les troubles subjectifs et de réduire l’altération transitoire aiguë de la fonction respiratoire observée en l’absence de filtration. Cela confirme que la présence de particules dans l’environnement professionnel joue un rôle primordial dans l’irritation des voies respiratoires et des poumons et qu’il est possible d’évaluer cet effet irritant en mesurant les brusques variations des paramètres de la fonction respiratoire.
La multiplicité des expositions professionnelles et les modifications continuelles du milieu de travail peuvent rendre difficile l’identification d’une relation causale avec les différents agents présents dans ce milieu. Le scénario de l’exposition dans les scieries illustre parfaitement cette difficulté. On ne peut (notamment pour des raisons économiques) mesurer l’exposition à tous les agents possibles (terpènes, poussière, moisissures, bactéries, endotoxines, mycotoxines, etc.) dans cet environnement. Une méthode envisageable consiste à suivre longitudinalement l’évolution de la fonction respiratoire. Dans le cadre d’une étude portant sur des travailleurs occupés dans des scieries, faisant l’éboutage du bois, la fonction respiratoire a été étudiée au début et à la fin d’une semaine de travail, et aucune anomalie statistiquement significative n’a été mise en évidence. Cependant, une étude de suivi réalisée quelques années plus tard a révélé que les travailleurs chez lesquels on avait observé une altération quantitative de la fonction respiratoire au cours de la semaine de travail considérée étaient également atteints à long terme de troubles fonctionnels respiratoires. C’est peut-être un signe qu’il est possible d’identifier les sujets vulnérables en mesurant les variations des paramètres fonctionnels respiratoires tout au long d’une semaine de travail.
La présence d’agents irritants sur les lieux de travail peut être désagréable ou gênante; elle peut aussi être à l’origine d’une atteinte au moral ou d’une baisse de productivité. Certaines expositions sont franchement dangereuses, voire mortelles. Dans tous les cas, les troubles causés au niveau des voies respiratoires par les agents irritants et les substances toxiques inhalées ne sont pas rares et de nombreux travailleurs sont confrontés quotidiennement au risque d’expositions de cette nature. Ces agents et ces substances peuvent être nocifs de très nombreuses façons, et l’importance des lésions qu’ils provoquent est extrêmement variable en fonction du degré d’exposition et des propriétés biochimiques de l’agent inhalé. Ils se caractérisent cependant tous par l’absence de spécificité, c’est-à-dire qu’à partir d’un certain niveau d’exposition ils constituent une menace pour la santé de pratiquement toutes les personnes exposées.
D’autres substances inhalées peuvent n’entraîner des troubles respiratoires que chez des sujets sensibles; la meilleure technique consiste à les traiter comme des affections d’origine allergique ou immunologique. Certains composés, comme les isocyanates, les anhydrides d’acides et les résines époxy, peuvent se comporter en fortes concentrations non seulement comme des agents irritants non spécifiques, mais ils peuvent aussi prédisposer certains sujets à une sensibilisation allergique. A très faible concentration, cependant, ces mêmes composés provoquent l’apparition de symptômes respiratoires chez les sujets sensibilisés.
Les agents irritants pour les voies respiratoires comprennent des substances qui, après avoir été inhalées, provoquent une inflammation desdites voies. Les lésions peuvent affecter les voies respiratoires supérieures et inférieures. L’inflammation aiguë du parenchyme pulmonaire, qui se manifeste notamment dans le cas de la pneumopathie chimique ou de l’œdème pulmonaire non cardiogénique, est plus dangereuse. Les substances susceptibles d’induire des lésions parenchymateuses sont considérées comme toxiques. De nombreuses substances chimiques toxiques inhalées peuvent, elles aussi, irriter les voies respiratoires; elles se signalent à l’attention par leur odeur désagréable, une irritation nasopharyngée et de la toux. La plupart des agents irritants pour les voies respiratoires sont également toxiques pour le parenchyme pulmonaire quand ils sont inhalés à fortes doses. Après avoir été inhalées, de nombreuses substances peuvent passer dans le sang et avoir ainsi des effets systémiques toxiques, sans léser nécessairement les poumons; c’est le cas, par exemple, du plomb, du monoxyde de carbone et de l’acide cyanhydrique. On observe normalement une légère inflammation pulmonaire dans les fièvres d’inhalation (syndrome toxique des poussières organiques, fièvre des métaux, fièvre des polymères, etc.). Des lésions graves des poumons surviennent en cas d’exposition importante à des substances toxiques comme le cadmium et le mercure.
Les propriétés physiques des substances inhalées permettent de prévoir leur site de déposition, c’est-à-dire le niveau auquel les substances irritantes causeront des troubles. Les particules de grande taille (10 à 20 µm) se déposent dans le nez et les voies respiratoires supérieures, les particules plus petites (5 à 10 µm) dans la trachée et les bronches, tandis que les particules inférieures à 5 µm peuvent parvenir jusqu’aux alvéoles. Celles de moins de 0,5 µm sont si petites qu’elles se comportent comme des gaz. La déposition des gaz toxiques dépend de leur solubilité: un gaz hydrosoluble sera adsorbé par la muqueuse humide des voies respiratoires supérieures, tandis que les gaz moins solubles se déposeront, de façon plus erratique, dans n’importe quelle partie de l’arbre respiratoire.
Ces agents, après avoir été inhalés, entraînent une inflammation non spécifique des poumons. Leur appellation chimique, leurs sources d’exposition, leurs principales propriétés physiques et autres, ainsi que les lésions qu’ils provoquent, sont récapitulées au tableau 10.3. Les gaz irritants ont tendance à être plus solubles dans l’eau que les gaz plus toxiques pour le parenchyme pulmonaire. Les fumées toxiques dont le seuil d’irritation est élevé sont particulièrement dangereuses, car on les respire sans éprouver les sensations désagréables qui servent généralement de signal d’alarme.
|
Substance chimique |
Sources d�exposition |
Principales propriétés |
Lésions produites |
Limite d�exposition à court terme; 15 minutes maximum (ppm) |
|
Acétaldéhyde |
Plastiques, industrie du caoutchouc synthétique; produits de combustion |
Pression de vapeur élevée; grande hydrosolubilité |
Lésions des voies aériennes supérieures; rares cas d�œdème pulmonaire retardé |
|
|
Acide acétique, acides organiques |
Industries chimique et électronique; produits de combustion |
Solubilité dans l�eau |
Lésions des yeux et des voies aériennes supérieures |
|
|
Acide chlorhydrique |
Affinage des métaux, fabrication de caoutchouc et de composés organiques, produits photographiques |
Très grande solubilité dans l�eau |
Inflammation des yeux et des voies aériennes supérieures, inflammation des voies aériennes inférieures uniquement en cas d�exposition massive |
100 |
|
Acide chromique (Cr(VI)) |
Soudage, galvanoplastie |
Irritant hydrosoluble; sensibilisant allergique |
Inflammation et ulcération nasale, rhinite, pneumopathie en cas d�exposition massive |
|
|
Acide fluorhydrique |
Catalyseur chimique, pesticides, blanchiment, soudage, gravure |
Oxydant très hydrosoluble, puissant et rapide; abaisse la calcémie en cas d�exposition massive |
Inflammation des yeux et des voies aériennes supérieures, trachéo-bronchite et pneumonie en cas d�exposition massive |
20 |
|
Acide sélénhydrique |
Affinage du cuivre, production d�acide sulfurique |
Soluble dans l�eau; l�exposition aux composés séléniés provoque une haleine alliacée |
Inflammation des yeux et des voies aériennes supérieures, œdème pulmonaire retardé |
|
|
Acroléine |
Fabrication des plastiques, des textiles et des produits pharmaceutiques; produits de combustion |
Pression de vapeur élevée, hydrosolubilité moyenne, irritant puissant |
Lésions diffuses des voies aériennes et du parenchyme pulmonaire |
|
|
Ammoniac |
Fabrication des engrais, des aliments pour animaux, des produits chimiques et pharmaceutiques |
Gaz alcalin, très grande hydrosolubilité |
Essentiellement brûlures des yeux et des voies aériennes supérieures; l�exposition massive peut entraîner une bronchectasie |
500 |
|
Anhydrides d�acides |
Industries chimique, des peintures et des plastiques; composants des résines époxydes |
Hydrosolubilité, réactivité élevée; peuvent provoquer une sensibilisation allergique |
Lésions des yeux et des voies aériennes supérieures, bronchospasme, hémorragies pulmonaires après une exposition massive |
|
|
Béryllium |
Alliages (avec le cuivre), produits céramiques; électronique; industrie aérospatiale et pièces de réacteurs nucléaires |
Métal irritant; se comporte aussi comme un antigène pour favoriser une réponse granulomateuse à long terme |
Lésions aiguës des voies aériennes supérieures, trachéo-bronchite, pneumonie chimique |
25 µg/m3 |
|
Boranes (diborane) |
Carburants pour avions; fabrication de fongicides |
Gaz hydrosoluble |
Lésions des voies aériennes supérieures, pneumonie en cas d�exposition massive |
|
|
Bromure d�hydrogène |
Raffinage du pétrole |
|
Lésions des voies aériennes supérieures, pneumonie en cas d�exposition massive |
|
|
Bromure de méthyle |
Réfrigération; fumigants |
Gaz moyennement soluble |
Lésions des voies aériennes supérieures et inférieures, pneumonie, dépression du SNC et convulsions |
|
|
Cadmium |
Alliages avec le zinc et le plomb, galvanoplastie, accumulateurs, insecticides |
Effets aériennes aigus et chroniques |
Trachéo-bronchite, œdème pulmonaire (apparition souvent retardée de 24-48 heures); l�exposition chronique induit des lésions inflammatoires et un emphysème |
100 |
|
Chlore |
Blanchiment, production de composés chlorés, nettoyants domestiques |
Hydrosolubilité moyenne |
Inflammation des voies aériennes supérieures et inférieures, pneumonie et œdème pulmonaire non cardiogénique |
5-10 |
|
Chloro-acétophénone |
Gaz lacrymogène |
Les propriétés irritantes sont utilisées pour la neutralisation de manifestations; agent alkylant |
Inflammation des yeux et des voies aériennes supérieures; lésions des voies aériennes inférieures et du parenchyme pulmonaire en cas d�exposition massive |
1-10 |
|
o-Chlorobenzylidène-malononitrile |
Gaz lacrymogène |
Les propriétés irritantes sont utilisées pour la neutralisation de manifestations |
Inflammation des yeux et des voies aériennes supérieures; lésions des voies aériennes inférieures en cas d�exposition massive |
|
|
Chlorométhyl-éthers |
Solvants, utilisés pour la fabrication d�autres composés organiques |
|
Irritation des voies aériennes supérieures et inférieures; également cancérogène pour l�appareil respiratoire |
|
|
Chloropicrine |
Fabrication de produits chimiques, notamment de fumigènes |
Gaz de combat au cours de la première guerre mondiale |
Inflammation des voies aériennes supérieures et inférieures |
15 |
|
Chlorure de zinc |
Grenades fumigènes, obus d�artillerie |
Plus toxique que l�oxyde de zinc |
Irritation des voies aériennes supérieures et inférieures, fièvre, pneumonie d�apparition retardée |
200 |
|
Chlorures phosphoriques |
Fabrication de composés organiques chlorés, de colorants et d�additifs pour l�essence |
Forment de l�acide phosphorique et de l�acide chlorhydrique au contact des surfaces muqueuses |
Inflammation des yeux et des voies aériennes supérieures |
10 mg/m3 |
|
Cobalt |
Alliages à haute température, aimants permanents, outils en métal dur (avec le carbure de tungstène) |
Agent irritant non spécifique; sensibilisant allergique |
Bronchospasme aigu ou pneumonie; l�exposition chronique peut induire une fibrose pulmonaire |
|
|
Dioxyde d�azote |
Silos de stockage de céréales, fabrication d�engrais, soudage à l�arc, produits de combustion |
Très peu soluble dans l�eau; gaz brun en concentration élevée |
Inflammation des yeux et des voies aériennes supérieures et inférieures, œdème pulmonaire non cardiogénique, bronchiolite d�apparition retardée |
50 |
|
Dioxyde de sélénium |
Affinage du cuivre et du nickel, chauffage d�alliages au sélénium |
Vésicant puissant; forme de l�acide sélénieux (H2SeO3) sur les surfaces muqueuses |
Inflammation des yeux et des voies aériennes supérieures, œdème pulmonaire en cas d�exposition massive |
|
|
Dioxyde de soufre |
Raffinage du pétrole, production de pâte à papier, installations réfrigérées, fabrication de sulfite de sodium |
Gaz fortement soluble dans l�eau |
Inflammation des voies aériennes supérieures, bronchoconstriction, pneumonie en cas d�exposition massive |
100 |
|
Formaldéhyde |
Fabrication de mousses isolantes, contreplaqués, textiles, papier, engrais, résines; embaumement; produits de combustion |
Très grande hydrosolubilité, métabolisme rapide; agit essentiellement en stimulant les nerfs sensitifs; sensibilisation possible |
Irritation des yeux et des voies aériennes supérieures; bronchospasme en cas de forte exposition; dermatite de contact en cas de sensibilisation |
3 |
|
Hexafluorure d�uranium |
Décapage de revêtements métalliques, étanchéité de planchers, peintures en spray |
Toxicité probablement due aux ions chlorure |
Inflammation des voies aériennes supérieures et inférieures, bronchospasme, pneumonie |
|
|
Hydrure de lithium |
Alliages, céramiques, électronique, catalyseurs chimiques |
Faible solubilité, réactivité élevée |
Pneumonie, œdème pulmonaire non cardiogénique |
|
|
Isocyanates |
Production de polyuréthanes; peintures; herbicides et insecticides; meubles stratifiés, émaillage, application d�élastomères |
Composés organiques de faible masse moléculaire, irritants; provoquent une sensibilisation chez les sujets sensibles |
Inflammation des yeux et des voies aériennes supérieures et inférieures; asthme; pneumonie par hypersensibilité chez les sujets déjà sensibilisés |
0,1 |
|
Mercure |
Electrolyse, extraction des minerais et des amalgames, fabrication de composants électroniques |
Pas de symptômes respiratoires en cas d�exposition chronique à de faibles concentrations |
Inflammation des yeux et de l�appareil respiratoire, pneumonie, effets sur le SNC et le rein et effets systémiques |
1,1 mg/m3 |
|
Moutardes à l�azote; moutardes au soufre |
Gaz de combat vésicants |
Provoquent des lésions graves; propriétés vésicantes |
Inflammation des yeux et de l�ensemble des voies aériennes, pneumonie |
20 mg/m3 (N) |
|
Nickel-carbonyle |
Affinage du nickel, galvanoplastie, réactifs chimiques |
Toxique puissant |
Irritation des voies aériennes inférieures, pneumonie, effets toxiques systémiques retardés |
8 µg/m3 |
|
Oxyde de calcium, hydroxyde de calcium |
Chaux, photographie, tannage, insecticides |
Causticité modérée; toxicité à très hautes doses seulement |
Inflammation des voies aériennes supérieures et inférieures, pneumonie |
|
|
Ozone |
Soudage à l�arc, photocopieuses, blanchiment du papier |
Gaz d�odeur sucrée, solubilité modérée dans l�eau |
Inflammation des voies aériennes supérieures et inférieures; les asthmatiques sont plus sensibles |
1 |
|
Pentoxyde de vanadium |
Nettoyage de citernes de fuel, métallurgie |
|
Symptômes affectant les yeux et les voies aériennes supérieures et inférieures |
70 |
|
Phosgène |
Fabrication de pesticides et d�autres produits chimiques, soudage à l�arc, décapage des peintures |
Faiblement soluble dans l�eau; à faibles concentrations, n�irrite pas les voies aériennes |
Inflammation des voies aériennes supérieures et pneumonie; à faibles concentrations, œdème pulmonaire retardé |
2 |
|
Styrène |
Fabrication de polystyrène et de résines, polymères |
Irritant puissant |
Inflammation des yeux, des voies aériennes supérieures et inférieures, troubles neurologiques |
600 |
|
Sulfures phosphoriques |
Production d�insecticides, agents d�ignition, allumettes |
|
Inflammation des yeux et des voies aériennes supérieures |
|
|
Tétrachlorure de titane |
Colorants, pigments, fumigènes |
Les ions chlorure forment du HCl sur les muqueuses |
Lésions des voies aériennes supérieures |
|
|
Tétrachlorure de zirconium |
Pigments, catalyseurs |
Toxicité liée aux ions chlorure |
Irritation des voies aériennes supérieures et inférieures, pneumonie |
|
|
Tétroxyde d�osmium |
Affinage du cuivre, alliages avec l�iridium, catalyseur de la synthèse des stéroïdes et synthèse de l�ammoniac |
L�osmium métallique est inerte; le tétroxyde apparaît par chauffage dans l�air |
Irritation grave des yeux et des voies aériennes supérieures; lésions rénales transitoires |
1 mg/m3 |
|
Trichlorure d�antimoine, pentachlorure d�antimoine |
Alliages, catalyseurs organiques |
Faible solubilité; lésions probablement dues à l�ion halogénure |
Pneumonie; œdème pulmonaire non cardiogénique |
|
D�après Sheppard, 1988; Graham, 1994; Rom, 1992; Blanc et Schwartz, 1994; Nemery, 1990; Skornik, 1988.
La nature et l’intensité de la réaction à un agent irritant dépendent des propriétés physiques du gaz ou de l’aérosol, de sa concentration, de la durée d’exposition et d’autres variables encore telles que la température ou l’humidité ambiantes et la présence d’agents pathogènes ou d’autres gaz (Man et Hulbert, 1988). Des facteurs propres à l’hôte, tels que l’âge (Cabral-Anderson, Evans et Freeman, 1977; Evans, Cabral-Anderson et Freeman, 1977), l’exposition antérieure (Tyler, Tyler et Last, 1988), la concentration en antioxydants (McMillan et Boyd, 1982) et la présence d’une infection, peuvent avoir une influence sur les anomalies pathologiques constatées. Cette multiplicité de facteurs rend difficile l’étude systématique des effets pathogènes des irritants respiratoires.
Les substances irritantes les mieux connues sont celles qui provoquent des lésions par oxydation. C’est le cas de la plupart des agents irritants inhalés (dont les principaux polluants) qui agissent individuellement par oxydation ou donnent naissance à des composés qui exercent une action du même type. La plupart des fumées de métaux sont en fait des oxydes du métal chauffé; ces oxydes provoquent des lésions oxydatives. Les agents oxydants lèsent essentiellement les cellules en induisant une peroxydation des lipides, mais d’autres mécanismes peuvent être impliqués. Au niveau cellulaire, on observe d’abord une disparition relativement spécifique des cellules ciliées de l’épithélium respiratoire et des cellules épithéliales alvéolaires de type I, avec rupture ultérieure des ponts unissant les cellules épithéliales (Man et Hulbert, 1988; Gordon, Salano et Kleinerman, 1986; Stephens et coll., 1974). Il en résulte des lésions sous-épithéliales et sous-muqueuses, accompagnées d’une stimulation des fibres musculaires lisses et des terminaisons nerveuses sensitives afférentes parasympathiques qui provoquent une bronchoconstriction (Holgate, Beasley et Twentyman, 1987; Boucher, 1981) entraînant une réponse inflammatoire (Hogg, 1981) et la libération, par les polynucléaires neutrophiles et éosinophiles, de médiateurs qui causent d’autres lésions oxydatives (Castleman et coll., 1980). Les pneumocytes de type II et les cellules cuboïdes servent de cellules-souches pour la réparation (Keenan, Combs et McDowell, 1982; Keenan, Wilson et McDowell, 1983).
D’autres mécanismes de formation de lésions pulmonaires par oxydation peuvent également intervenir, surtout à la suite d’une lésion affectant la couche épithéliale protectrice et provoquant une réponse inflammatoire. Les mécanismes les plus courants sont indiqués au tableau 10.4.
|
Mécanisme lésionnel |
Exemples de substances |
Lésions |
|
Oxydation |
Ozone, dioxyde d�azote, dioxyde de soufre, chlore, oxydes |
Lésions dispersées des voies aériennes, avec augmentation de la perméabilité et exposition des terminaisons nerveuses; disparition des cils des cellules ciliées; nécrose des pneumocytes de type I; formation de radicaux libres, puis liaison protéique et peroxydation des lipides |
|
Formation d�acides |
Dioxyde de soufre, chlore, halogénures |
Le gaz se dissout dans l�eau pour former un acide qui altère les cellules épithéliales par un mécanisme d�oxydation; action prédominant au niveau des voies aériennes supérieures |
|
Formation de bases |
Ammoniac, oxyde de calcium, hydroxydes |
Le gaz se dissout dans l�eau en formant une solution alcaline susceptible d�entraîner une liquéfaction tissulaire; lésions prédominant au niveau des voies aériennes supérieures; atteinte des voies aériennes inférieures en cas d�exposition massive |
|
Liaison avec les protéines |
Formaldéhyde |
Les réactions avec les acides aminés génèrent des produits intermédiaires toxiques et des lésions des cellules épithéliales |
|
Stimulation des nerfs afférents |
Ammoniac, formaldéhyde |
La stimulation directe des terminaisons nerveuses provoque des symptômes |
|
Antigénicité |
Platine, anhydrides d�acides |
Les molécules de faible masse moléculaire se comportent comme des haptènes chez les sujets sensibilisés |
|
Stimulation des réponses immunitaires de l�hôte |
Oxydes de cuivre et de zinc, lipoprotéines |
Stimulation de la libération de cytokines et de médiateurs de l�inflammation, sans lésion cellulaire directe apparente |
|
Formation de radicaux libres |
Paraquat |
Formation stimulée de radicaux peroxyde ou retard dans leur élimination, aboutissant à une peroxydation des lipides et à des lésions par oxydation |
|
Clairance retardée des particules |
Toute inhalation prolongée de poussières minérales |
Escaliers mucociliaires et macrophages alvéolaires submergés par les particules, entraînant une réponse inflammatoire non spécifique |
Les travailleurs exposés à de faibles concentrations d’irritants respiratoires peuvent présenter des symptômes infracliniques, à savoir des irritations des muqueuses qui provoquent larmoiement, mal de gorge, rhinorrhée et toux. En cas d’exposition plus sévère, la sensation d’essoufflement qui s’ajoute à ces divers symptômes incite généralement l’intéressé à consulter un médecin. Il est important de bien interroger le patient sur ses antécédents médicaux pour déterminer la nature probable de l’exposition, son degré et sa durée. Les signes d’œdème laryngé, raucité de la voix et stridor, entre autres, doivent être recherchés, et l’examen des poumons doit porter sur les signes d’atteinte des voies respiratoires inférieures et du parenchyme. Il est important pour la conduite à tenir à court terme de disposer d’une évaluation de l’état des voies respiratoires et de la fonction pulmonaire, ainsi que d’une radiographie thoracique. Il peut être indiqué d’effectuer une laryngoscopie dans le cadre du bilan respiratoire.
En cas de menace pour les voies respiratoires, le patient devrait être intubé et placé sous assistance ventilatoire. Les patients présentant des signes d’œdème laryngé devraient être gardés en observation pendant douze heures au moins jusqu’à ce que l’on soit sûr que ces signes ont disparu d’eux-mêmes. Le bronchospasme doit être traité avec des alpha-agonistes et, en cas d’échec, avec des corticoïdes intraveineux. La muqueuse buccale ou oculaire irritée doit être soigneusement irriguée. Les patients présentant des râles sous-crépitants à l’auscultation ou des anomalies radiologiques devraient être hospitalisés pour surveillance en raison du risque de pneumopathie ou d’œdème pulmonaire. Il existe un risque de surinfection bactérienne chez ces patients, mais l’antibioprophylaxie n’a pas fait la preuve de son efficacité.
Presque tous les patients ayant survécu à l’agression initiale guérissent complètement après une exposition aux agents irritants. Les risques de séquelles à long terme sont plus probables en cas de lésion initiale grave. On parle de syndrome de dysfonction réactive des voies aériennes ou asthme induit par les irritants (Reactive Airways Dysfunction Syndrome (RADS)) lorsque les symptômes asthmatiformes persistent après une exposition aiguë à des agents irritants respiratoires (Brooks, Weiss et Bernstein, 1985).
On pense que cet état est la conséquence d’une persistance de l’inflammation, avec diminution de la perméabilité des cellules épithéliales ou diminution du seuil de conductance des terminaisons nerveuses sous-épithéliales.
L’exposition à des concentrations élevées de bases ou d’acides est susceptible de provoquer des brûlures des voies respiratoires supérieures et inférieures qui peuvent devenir chroniques. On sait que l’ammoniac provoque des bronchectasies (Kass et coll., 1972); le chlore (qui se transforme en HCl dans la muqueuse) provoque une maladie respiratoire obstructive (Donelly et Fitzgerald, 1990; Das et Blanc, 1993). L’exposition chronique à de faibles concentrations de substances irritantes peut entraîner des symptômes permanents au niveau des yeux et des voies respiratoires supérieures (Korn, Dockery et Speizer, 1987), mais la détérioration permanente de la fonction pulmonaire n’a pas été démontrée. Les études consacrées aux effets de l’exposition chronique à de faibles concentrations d’agents irritants sur la fonction des voies respiratoires ne sont pas concluantes; elles sont obérées par l’absence de suivi à long terme et perturbées par des facteurs de confusion tels que le tabagisme, l’«effet du travailleur en bonne santé», sans compter que les manifestations cliniques peuvent être minimes, voire nulles (Brooks et Kalica, 1987).
Dès que la lésion initiale est guérie, il est indispensable d’assurer un suivi médical régulier. Il faut aussi examiner le lieu de travail du patient et envisager des précautions respiratoires, une ventilation appropriée et le confinement des agents irritants en cause.
Les substances chimiques toxiques pour les poumons comprennent la plupart des agents irritants respiratoires, pour autant que l’exposition soit suffisamment importante; toutefois, de nombreuses substances chimiques peuvent provoquer de sévères lésions parenchymateuses en dépit de leurs propriétés irritantes faibles ou modérées. Ces substances exercent leurs effets par les mécanismes mentionnés au tableau 10.3 et traités plus haut. Les agents toxiques pour les poumons ont tendance à être moins hydrosolubles que les substances irritantes pour les voies respiratoires supérieures. Le tableau 10.5 fournit des exemples d’agents toxiques pour les poumons et indique leurs sources d’exposition ainsi que leurs effets.
|
Substance chimique |
Sources d�exposition |
Toxicité |
|
Acroléine |
Fabrication des plastiques, des textiles et des produits pharmaceutiques; produits de combustion |
Lésions diffuses des voies aériennes et du parenchyme pulmonaire |
|
Cadmium |
Alliages avec le zinc et le plomb, galvanoplastie, accumulateurs, insecticides |
Trachéo-bronchite, œdème pulmonaire (apparition souvent retardée de 24-48 heures), lésions rénales: protéinurie tubulaire |
|
Chlore |
Blanchiment, production de composés chlorés, nettoyants domestiques |
Inflammation des voies aériennes supérieures et inférieures, pneumonie et œdème pulmonaire non cardiogénique |
|
Chloropicrine |
Fabrication de produits chimiques; composants de fumigènes |
Inflammation des voies aériennes supérieures et inférieures |
|
Chlorure de zinc |
Grenades fumigènes, obus d�artillerie |
Irritation des voies aériennes supérieures et inférieures, fièvre, pneumonie d�apparition retardée |
|
Dioxyde d�azote |
Silos de stockage de céréales, fabrication d�engrais, soudage à l�arc; produits de combustion |
Inflammation des yeux et des voies aériennes supérieures et inférieures, œdème pulmonaire non cardiogénique, bronchiolite d�apparition retardée |
|
Hydrure de lithium |
Alliages, céramiques, électronique, catalyseurs chimiques |
Pneumonie, œdème pulmonaire non cardiogénique |
|
Mercure |
Electrolyse, extraction des minerais et des amalgames, fabrication de composants électroniques |
Inflammation des yeux et de l�appareil respiratoire, pneumonie, effets sur le SNC et le rein et effets systémiques |
|
Méthylisocyanate |
Synthèse de pesticides |
Irritation des voies aériennes supérieures et inférieures, œdème pulmonaire |
|
Moutardes à l�azote, moutardes au soufre |
Gaz de combat, vésicants |
Inflammation des yeux et de l�appareil respiratoire, pneumonie |
|
Nickel-carbonyle |
Affinage du nickel, galvanoplastie, réactifs chimiques |
Irritation des voies aériennes inférieures, pneumonie, effets toxiques systémiques retardés |
|
Paraquat |
Herbicides (ingestion) |
Lésions sélectives des pneumocytes de type 2 entraînant un RADS, une fibrose pulmonaire, insuffisance rénale, irritation digestive |
|
Phosgène |
Fabrication de pesticides et d�autres produits chimiques, soudage à l�arc; décapage des peintures |
Inflammation des voies aériennes supérieures et pneumopathie; œdème pulmonaire retardé à dose faible |
|
Sulfure d�hydrogène |
Puits de gaz naturel, mines, engrais |
Irritation des yeux et des voies aériennes supérieures et inférieures, œdème pulmonaire retardé, asphyxie par hypoxie tissulaire systémique |
|
Trichlorure d�antimoine; pentachlorure d�antimoine |
Alliages, catalyseurs organiques |
Pneumonie, œdème pulmonaire non cardiogénique |
Une classe d’agents toxiques respirables est celle des asphyxiants. Présents en concentration suffisamment élevée, certains agents asphyxiants tels que le gaz carbonique, le méthane et l’azote, déplacent l’oxygène et finissent par causer la suffocation de la victime. L’acide cyanhydrique, le monoxyde de carbone et l’hydrogène sulfuré agissent en inhibant la respiration cellulaire malgré un apport suffisant d’oxygène aux poumons. Quant aux agents toxiques inhalés non asphyxiants, ils lèsent les organes cibles, causant un grand nombre de problèmes de santé et une mortalité non négligeable.
Le traitement médical en cas d’inhalation d’agents toxiques pulmonaires est le même que pour les agents irritants respiratoires. Souvent, le maximum d’intensité des effets cliniques de ces agents toxiques n’est pas atteint au cours des heures qui suivent l’exposition et une surveillance pendant la nuit peut être nécessaire lorsqu’il s’agit de substances susceptibles de provoquer un œdème pulmonaire retardé. Le traitement des atteintes toxiques systémiques sortant du cadre du présent chapitre, le lecteur est prié de consulter les chapitres de l’Encyclopédie où il est question des divers toxiques, ainsi que la documentation consacrée à ce sujet (Goldfrank et coll., 1990; Ellenhorn et Barceloux, 1988).
Certaines expositions par inhalation se produisant dans divers environnements professionnels peuvent induire des syndromes pseudo-grippaux d’une durée de quelques heures, appelés fièvres d’inhalation. Malgré la gravité des symptômes, il semble que la toxicité soit autolimitée dans la plupart des cas, et peu de séquelles à long terme ont été signalées. L’exposition massive à des substances irritantes peut cependant entraîner une réaction plus forte provoquant une pneumopathie et un œdème pulmonaire; ces cas peu fréquents sont jugés plus complexes qu’une simple fièvre d’inhalation.
Les fièvres d’inhalation ont pour caractéristique commune l’absence de spécificité; le syndrome peut apparaître chez pratiquement n’importe quel individu pourvu que l’exposition à l’agent irritant soit assez forte. Une sensibilisation n’est pas indispensable; il en va de même pour une exposition antérieure. Certains des syndromes s’accompagnent d’un phénomène de tolérance, c’est-à-dire qu’aucun symptôme n’apparaît en cas d’exposition répétée régulière. On pense que ce phénomène est dû à une activité accrue des mécanismes de clairance, mais il n’a pas encore été suffisamment étudié.
Le syndrome toxique des poussières organiques (Organic Dust Toxic Syndrome (ODTS)) est une expression qui désigne les symptômes pseudo-grippaux autolimités consécutifs à une exposition importante à des poussières organiques. Ce syndrome englobe un grand nombre de maladies fébriles aiguës désignées en fonction des activités professionnelles qui sont à l’origine de l’exposition aux poussières. Les symptômes n’apparaissent qu’après une exposition massive et la plupart des sujets exposés en sont atteints.
Le syndrome toxique des poussières organiques était appelé auparavant mycotoxicose pulmonaire en raison de son étiologie présumée qui impliquait des spores de moisissures et des actinomycètes. Chez certains patients, on peut obtenir des cultures de différentes espèces: Aspergillus, Penicillium et des actinomycètes mésophiles et thermophiles (Emanuel, Wenzel et Lawton, 1975; Emanuel, Marx et Ault, 1989). Plus récemment, on a attribué un rôle au moins aussi important à des endotoxines bactériennes. Le syndrome a été provoqué expérimentalement par l’inhalation d’une endotoxine sécrétée par Enterobacter agglomerans, élément majeur des poussières organiques (Rylander, Bake et Fischer, 1989). En milieu agricole, on a mis en évidence des concentrations d’endotoxines bactériennes comprises entre 0,01 et 100 mg/m3. Dans de nombreux échantillons, la concentration dépassait 0,2 mg/m3, taux à partir duquel on sait qu’apparaissent des troubles cliniques (May, Stallones et Darrow, 1989). On présume que les cytokines telles que l’IL-1 peuvent assurer la médiation des effets systémiques, compte tenu de ce que l’on sait déjà sur la libération de l’IL-1 par les macrophages alvéolaires en présence d’endotoxines (Richerson, 1990). Un mécanisme allergique est peu probable, étant donné que le phénomène peut se produire sans sensibilisation et qu’une exposition massive à la poussière est nécessaire.
Sur le plan clinique, le patient présente habituellement des symptômes deux à huit heures après l’exposition à des céréales (généralement moisies) ou à du foin, du coton, du lin, du chanvre ou des copeaux de bois, ou encore après s’être occupé de cochons (do Pico, 1992). Les symptômes débutent souvent par une irritation des yeux et des muqueuses, accompagnée d’une toux sèche; ils évoluent vers une hyperthermie associée à des malaises, une oppression thoracique, des myalgies et des céphalées. Le patient a l’air malade, mais l’examen clinique est normal par ailleurs. On note souvent une hyperleucocytose qui peut atteindre 25 000 leucocytes/mm3. La radiographie pulmonaire est presque toujours normale. L’examen spirométrique peut mettre en évidence un léger syndrome obstructif. Lorsque des bronchoscopies ont été réalisées avec lavage broncho-alvéolaire, on a observé une augmentation des leucocytes dans le liquide de lavage. Le pourcentage de polynucléaires neutrophiles était nettement supérieur à la normale (Emanuel, Marx et Ault, 1989; Lecours, Laviolette et Cormier, 1986). La bronchoscopie pratiquée de une à quatre semaines après l’accident initial indique une hypercellularité persistante, avec prédominance des lymphocytes.
Selon la nature de l’exposition, le diagnostic différentiel peut mettre en évidence une exposition à un gaz toxique (dioxyde d’azote ou ammoniac), en particulier si l’accident est survenu dans un silo. Il est possible d’envisager une pneumopathie d’hypersensibilité, surtout en cas d’anomalies significatives de la radiographie thoracique ou des épreuves fonctionnelles respiratoires. La distinction entre la pneumopathie d’hypersensibilité (PH) et le STPO est importante: la PH exige le strict retrait de l’exposition et a un moins bon pronostic, alors que le STPO a une évolution bénigne et autolimitée. Le STPO se distingue également de la PH par sa plus grande fréquence, par le fait qu’il exige une exposition à des concentrations plus élevées de poussières, par son absence d’induction d’une libération d’anticorps précipitants sériques et, au début, par l’absence d’alvéolite lymphocytaire caractéristique de la PH.
Les troubles sont traités avec des antipyrétiques. On ne recommande pas l’usage de corticoïdes puisque la guérison est spontanée. Il faut conseiller aux patients d’éviter toute exposition importante. L’effet à long terme des accidents répétés est jugé négligeable, mais la question n’a pas encore été suffisamment étudiée.
La fièvre des métaux (FM) est une autre maladie à guérison spontanée, d’allure pseudo-grippale, qui apparaît après l’inhalation de fumées de métaux. Ce syndrome survient souvent après inhalation d’oxyde de zinc comme il s’en produit dans les fonderies de cuivre au cours des opérations de fusion ou de soudage de métaux galvanisés. Les oxydes de cuivre et de fer peuvent également induire une FM; les fumées ou vapeurs d’aluminium, d’arsenic, de cadmium, de mercure, de cobalt, de chrome, d’argent, de manganèse, de sélénium et d’étain ont été parfois incriminées elles aussi (Rose, 1992). Les travailleurs développent une tachyphylaxie, c’est-à-dire que les symptômes n’apparaissent qu’après une exposition succédant à plusieurs jours sans exposition et non à la suite d’expositions répétées régulières. L’Administration de la sécurité et de la santé au travail (Occupational Safety and Health Administration (OSHA)) aux Etats-Unis a fixé à 5 mg/m3 la TLV sur huit heures de l’oxyde de zinc, mais des symptômes ont été provoqués expérimentalement après deux heures d’exposition à cette concentration (Gordon et coll., 1992).
La pathogenèse de la FM reste mal connue. Le fait que la fièvre puisse réapparaître chez n’importe quel individu, pour autant qu’il soit exposé, va à l’encontre de l’hypothèse d’une sensibilisation spécifique, immune ou allergique. L’absence de symptômes associés à une libération d’histamine (bouffées vasomotrices, prurit, wheezing, urticaire) contredit également l’hypothèse d’un mécanisme allergique. Paul Blanc et ses collaborateurs ont mis au point un modèle faisant intervenir une libération de cytokines (Blanc et coll., 1991; Blanc et coll., 1993). Ils ont mesuré le facteur nécrosant des tumeurs (Tumour Necrosis Factor (TNF)) et les niveaux de diverses interleukines (IL-1, IL-4, IL-6 et IL-8) dans le liquide de lavage de poumons de vingt-trois volontaires exposés expérimentalement à des fumées d’oxyde de zinc (Blanc et coll., 1993). Le liquide de lavage broncho-alvéolaire (Bronchoalveolar Lavage (BAL)) des volontaires présentait des valeurs élevées de TNF trois heures après l’exposition. Vingt heures plus tard, ces mêmes auteurs ont observé un niveau élevé d’IL-8 (un puissant agent attractif des polynucléaires neutrophiles) dans le BAL, ainsi qu’une alvéolite neutrophile sévère. Ils ont pu montrer que le TNF, cytokine pyrogène capable de stimuler les cellules immunitaires, est libéré par des monocytes en culture qui ont été exposés à du zinc (Scuderi, 1990). Il s’ensuit que la présence de TNF en quantité accrue dans les poumons concorde avec l’apparition des symptômes observés dans la FM. On sait que le TNF stimule la libération de l’IL-6 et de l’IL-8 pendant une période qui coïncide avec les pics de concentrations des cytokines dans le BAL des sujets. Le recrutement de ces cytokines peut expliquer l’alvéolite neutrophile consécutive et les symptômes pseudo-grippaux qui caractérisent la FM. La raison pour laquelle l’alvéolite disparaît aussi rapidement reste un mystère.
Les symptômes commencent de trois à dix heures après l’exposition. Au début, il peut s’agir d’un goût métallique sucré dans la bouche, accompagné d’une toux sèche qui s’aggrave et d’un essoufflement. Une hyperthermie et des frissons apparaissent souvent et le travailleur se sent malade; à part cela, l’examen somatique ne révèle aucune modification particulière. Le bilan biologique signale une hyperleucocytose et la radiographie pulmonaire est normale. Les épreuves fonctionnelles respiratoires peuvent mettre en évidence une légère diminution du DEM25-75 et de la DLCO (Nemery, 1990; Rose, 1992).
Une anamnèse bien conduite permet de poser un diagnostic aisé et le travailleur peut être traité symptomatiquement aux antipyrétiques. Les symptômes et les anomalies cliniques disparaissent vingt-quatre à quarante-huit heures plus tard. Dans le cas contraire, il convient d’envisager une étiologie bactérienne ou virale des symptômes. En cas d’exposition extrême ou d’exposition impliquant une contamination par des toxiques tels que le chlorure de zinc, le cadmium ou le mercure, la FM peut être le signe avant-coureur d’une pneumopathie chimique qui apparaîtra cliniquement au cours des deux jours suivants (Blount, 1990). Chez ces patients, on peut observer des infiltrats diffus sur les radiographies pulmonaires et des signes d’œdème du poumon et d’insuffisance respiratoire. Alors que cette éventualité devrait être envisagée dans l’évaluation initiale d’un patient exposé, cette évolution fulminante est inhabituelle et n’est pas caractéristique de la FM non compliquée.
Pour qu’un cas de FM survienne, il n’est pas nécessaire que le sujet soit particulièrement sensible aux fumées de métaux; il s’agit plutôt de carences en matière d’hygiène industrielle. Le problème de l’exposition doit être réglé si l’on veut empêcher les récidives. Quoique le syndrome en question soit considéré comme bénin, les effets à long terme d’accès répétés de FM n’ont pas encore été suffisamment étudiés pour être bien connus.
La fièvre des polymères est une maladie fébrile autolimitée, comparable à la FM, mais provoquée par l’inhalation des produits de pyrolyse de fluoropolymères, et notamment du polytétrafluoroéthylène (PTFE; noms commerciaux Teflon, Fluon). Du fait de ses propriétés, le PTFE est largement utilisé comme lubrifiant et comme isolant thermique et électrique. Il est inoffensif tant qu’il n’est pas chauffé à plus de 300 °C, température à laquelle il commence à libérer des produits de décomposition (Shusterman, 1993), par exemple lorsqu’on soude des matériaux revêtus de PTFE, lorsqu’on chauffe du PTFE au cours d’une opération d’usinage à grande vitesse ou lorsqu’on travaille à des machines à mouler ou à extruder (Rose, 1992) et, dans de rares cas, au cours d’interventions de chirurgie endotrachéale au laser (Rom, 1992a).
Une cause fréquente de fièvre des polymères a été découverte après une enquête de santé publique classique menée au début des années soixante-dix (Wegman et Peters, 1974; Kuntz et McCord, 1974). Des ouvriers du textile présentaient des troubles fébriles autolimités après exposition au formaldéhyde, à l’ammoniac et aux fibres de nylon; ils n’étaient pas exposés aux fumées de fluoropolymères, mais manipulaient des polymères broyés. Après avoir constaté que l’exposition aux autres agents étiologiques possibles n’excédait pas les limites admissibles, on a étudié plus attentivement les opérations impliquant les fluoropolymères. Il est apparu que seuls les fumeurs de cigarette travaillant avec ces polymères présentaient des symptômes. On a supposé que les cigarettes étaient contaminées par les fluoropolymères présents sur les mains des ouvriers et que ceux-ci étaient absorbés quand une cigarette était fumée, exposant ainsi l’ouvrier aux fumées toxiques. Après l’interdiction de la cigarette sur le lieu de travail et l’établissement de règles strictes de lavage des mains, aucun autre cas n’a été rapporté (Wegman et Peters, 1974). Depuis lors, le même phénomène a été observé lors de la manipulation de composés hydrofuges, de lubrifiants de démoulage (Albrecht et Bryant, 1987) et de certains types de farts pour skis (Ström et Alexandersen, 1990).
La pathogenèse de la fièvre des polymères est inconnue. On pense qu’elle est identique à celle des autres fièvres d’inhalation du fait de la similitude de leurs aspects cliniques et de leurs réponses immunitaires apparemment aspécifiques. Aucune étude expérimentale n’a porté sur l’humain; en revanche, les rats et les oiseaux présentent tous deux des lésions épithéliales alvéolaires sévères en cas d’exposition aux produits de pyrolyse du PTFE (Wells, Slocombe et Trapp, 1982; Blandford et coll., 1975). Aucune mesure précise de la fonction pulmonaire ou des modifications du liquide de lavage broncho-alvéolaire n’a été effectuée.
Les symptômes apparaissent plusieurs heures après l’exposition et, à la différence de la FM, on ne note aucun phénomène de tolérance ou de tachyphylaxie. Une sensation de faiblesse et des myalgies sont suivies d’une hyperthermie et de frissons. On observe souvent une oppression thoracique et de la toux. L’examen clinique est généralement normal par ailleurs. Une hyperleucocytose est fréquente. La radiographie pulmonaire est généralement normale. Les symptômes disparaissent spontanément en douze à quarante-huit heures. On a rapporté quelques cas de patients faisant un œdème pulmonaire après exposition au PTFE; en règle générale, on pense que les fumées de ce composé sont plus toxiques que celles du zinc ou du cuivre induisant une FM (Shusterman, 1993; Brubaker, 1977). On a signalé un dysfonctionnement chronique des voies respiratoires chez des sujets ayant présenté de nombreux accès de fièvre des polymères (Williams, Atkinson et Patchefsky, 1974).
Le diagnostic de la fièvre des polymères exige une anamnèse approfondie, associée à une forte suspicion clinique. Lorsque la responsabilité des produits de pyrolyse du PTFE est confirmée, il faut s’efforcer d’éviter toute nouvelle exposition. L’obligation du lavage des mains et l’interdiction du tabagisme sur le lieu de travail ont fait disparaître complètement les cas liés à la contamination des cigarettes. Les travailleurs ayant fait de nombreux accès de fièvre des polymères ou un œdème du poumon associé devraient faire l’objet d’un suivi médical prolongé.
L’asthme est une maladie respiratoire caractérisée par une obstruction des voies aériennes partiellement ou complètement réversible (spontanément ou après traitement), une inflammation des voies respiratoires et une augmentation de la réactivité des voies respiratoires à un grand nombre de stimuli (NAEP, 1991). L’asthme professionnel (AP) est lié à des activités se déroulant sur les lieux de travail. Plusieurs centaines d’agents ont été accusés d’induire un AP. L’asthme préexistant ou l’hyperréactivité des voies respiratoires — dont les symptômes sont aggravés par une exposition professionnelle à des agents irritants ou à des stimuli physiques — sont généralement classés comme asthme aggravé par le travail (AAT). On s’accorde généralement à dire que l’AP est devenu la maladie respiratoire professionnelle la plus fréquente dans les pays développés, bien que les estimations de sa prévalence et de son incidence réelles soient extrêmement variables. Il n’en demeure pas moins que dans de nombreux pays, l’asthme d’origine professionnelle constitue une charge largement méconnue en raison de ses effets invalidants et des coûts qui en résultent tant sur le plan économique que sur d’autres plans. Ce fardeau pour la santé publique et l’économie pourrait être considérablement allégé par la détection et par la réduction ou l’élimination des expositions professionnelles induisant ce type d’affection. Le présent article donne un bref aperçu des méthodes actuelles de dépistage, de traitement et de prévention de l’AP. Plusieurs publications récentes traitent ce sujet de façon plus détaillée (Chan-Yeung, 1995; Bernstein et coll., 1993).
La prévalence de l’asthme chez l’adulte varie entre 3 et 5%, selon la définition et selon certains facteurs géographiques; elle peut être beaucoup plus forte dans certaines populations urbaines à faible revenu. Quant au pourcentage de cas d’asthme professionnel au sein de la population adulte, il varie entre 2 et 23%; selon les estimations les plus récentes, il approche toutefois la limite supérieure. La prévalence de l’asthme et de l’AP a été estimée dans des études portant sur de petites cohortes et dans des études transversales de groupes professionnels à haut risque. L’examen des résultats de vingt-deux études portant sur des milieux où les travailleurs sont exposés à des substances spécifiques indique que la prévalence de l’asthme et de l’AP, définie de différentes façons, oscillait entre 3 et 54%, et que dans douze cas elle était supérieure à 15% (Becklake, 1993). Cette plage importante reflète la variation réelle de la prévalence effective (due aux différences de nature et de degré de l’exposition), mais elle reflète aussi les différences des critères diagnostiques, de même que l’importance plus ou moins grande des facteurs de biais tels que l’«effet du travailleur survivant bien portant» qui peut résulter du fait que les travailleurs malades ont quitté leur poste avant que le début de l’étude ne commence. Les estimations de l’incidence à l’échelle de la population entière vont de 14 sujets actifs par million et par an aux Etats-Unis à 140 par million et par an en Finlande (Meredith et Nordman, 1996) où le dépistage des cas était plus efficace et les méthodes diagnostiques généralement plus rigoureuses. Il ressort de ces différentes études que l’AP est souvent sous-estimé ou sous-déclaré et qu’il représente un problème de santé publique beaucoup plus grave qu’on ne le pense habituellement.
Des études épidémiologiques et cliniques ont montré que plus de 200 agents (substances, professions ou processus industriels spécifiques) ont été incriminés dans l’étiologie de l’AP. Dans cette affection, l’inflammation des voies respiratoires et la bronchoconstriction peuvent être provoquées par une réponse immunologique à des agents sensibilisants, par des effets irritants directs ou par d’autres mécanismes non immunologiques. Certains agents (les insecticides organophosphorés, par exemple) peuvent également provoquer une bronchoconstriction par effet pharmacologique direct. On pense que la plupart des agents mis en cause entraînent une réaction de sensibilisation. Les agents irritants respiratoires aggravent souvent les symptômes présentés par les travailleurs déjà asthmatiques (AAT); en cas d’exposition importante, ils peuvent faire apparaître une nouvelle attaque d’asthme (appelée syndrome de dysfonction réactive des voies aériennes (Reactive Airways Dysfunction Syndrome (RADS)), ou encore asthme irritatif) (Brooks, Weiss et Bernstein, 1985; Alberts et do Pico, 1996).
Un AP peut survenir avec ou sans période de latence. Par période ou temps de latence, on entend le temps écoulé entre l’exposition initiale et l’apparition des symptômes. Cette période peut être extrêmement variable; elle est souvent inférieure à deux ans, mais dans 20% des cas environ, elle atteint ou dépasse dix ans. L’AP avec période de latence est généralement dû à une sensibilisation à une ou plusieurs substances. Le RADS, de son côté, est un type d’AP qui n’a pas de période de latence.
Les agents sensibilisants de masse moléculaire relative élevée (égale ou supérieure à 5 000 daltons) agissent souvent selon un mécanisme IgE-dépendant. Les agents sensibilisants de faible masse moléculaire relative (inférieure à 5 000 daltons ) — qui regroupent des substances chimiques hautement réactives comme les isocyanates — peuvent agir par des mécanismes IgE-indépendants ou peuvent se comporter comme des haptènes qui se combinent avec des protéines de l’organisme. Dès qu’un travailleur est sensibilisé, toute réexposition aux mêmes agents (fréquemment à des niveaux nettement inférieurs à celui responsable de la sensibilisation) entraîne une réponse inflammatoire des voies respiratoires, souvent accompagnée d’une augmentation de la limitation du débit respiratoire et de la réactivité bronchique non spécifique (RBNS).
Dans les études épidémiologiques de l’AP, l’exposition professionnelle demeure le principal facteur de la prévalence de l’asthme; par ailleurs, le risque de développement d’un AP après une certaine période de latence a tendance à augmenter avec l’intensité estimée de l’exposition. L’atopie est un facteur étiologique important; le tabac l’est un peu moins si l’on considère les agents agissant par l’entremise d’un mécanisme IgE-dépendant. Ni l’atopie, ni le tabagisme ne jouent un rôle majeur pour ce qui est des agents qui fonctionnent par un mécanisme IgE-indépendant.
Le tableau symptomatique de l’AP est comparable à celui de l’asthme non professionnel: râles, toux, oppression thoracique et dyspnée. Les patients présentent parfois une variante de la toux ou un asthme nocturne. L’AP peut être sévère et invalidant; des cas de décès ont même été signalés. La survenue de l’AP résulte d’un environnement professionnel spécifique, de sorte que l’identification des expositions présentes au moment du déclenchement de la crise d’asthme est indispensable à un diagnostic précis. Les expositions auxquelles sont soumis les travailleurs AAT sur le lieu de travail entraînent une augmentation significative de la fréquence ou de la gravité des symptômes de l’asthme préexistant (ou des deux à la fois).
Plusieurs caractères des antécédents cliniques peuvent suggérer une étiologie professionnelle (Chan-Yeung, 1995). Les symptômes, qui s’aggravent fréquemment au travail ou durant la nuit, s’améliorent pendant les arrêts de travail et réapparaissent lors de la reprise du travail. Ils peuvent s’aggraver progressivement vers la fin de la semaine de travail. Le patient peut noter les activités ou les agents spécifiques qui déclenchent à chaque fois les symptômes d’AP sur le lieu de travail. Une irritation oculaire ou une rhinite d’origine professionnelle peuvent s’associer aux symptômes asthmatiques. Ces tableaux cliniques caractéristiques peuvent être présents seulement aux stades initiaux de l’AP. Il est courant d’observer, au début de l’évolution de l’AP, une disparition partielle ou complète des symptômes pendant les fins de semaine ou les vacances; à la suite d’expositions répétées, cependant, le temps nécessaire à la récupération peut passer à une ou deux semaines, quand celle-ci ne s’avère pas impossible. La majorité des patients atteints d’AP qui ne sont plus soumis à une exposition dangereuse continuent à présenter un asthme symptomatique, et, cela, plusieurs années même après la fin de l’exposition, avec des troubles permanents et invalidants. La persistance de l’exposition entraîne une nouvelle aggravation de l’asthme. Par contre, si les symptômes sont de courte durée ou peu prononcés après cessation de l’exposition, le pronostic est favorable et les risques de troubles permanents sont faibles.
On a rapporté dans l’AP plusieurs schémas de succession des symptômes dans le temps. Des réactions asthmatiques précoces se produisent généralement peu de temps (moins d’une heure) après le début du travail ou de l’exposition professionnelle responsable de l’asthme. Les réactions asthmatiques tardives commencent quatre à six heures après le début de l’exposition et peuvent durer de vingt-quatre à quarante-huit heures. Des réactions asthmatiques combinées peuvent se produire, caractérisées par une sédation spontanée des symptômes entre la réaction précoce et la réaction tardive, ou par des réactions asthmatiques continues sans intervalle libre entre les différentes phases. A quelques exceptions près, les réactions précoces sont plutôt médiées IgE-dépendantes, tandis que les réactions tardives sont IgE-indépendantes.
Une RBNS accrue, généralement mise en évidence par le test à la méthacholine ou à l’histamine, est en principe considérée comme un symptôme majeur de l’AP professionnel. Le temps d’évolution et l’intensité de la RBNS peuvent être utiles au diagnostic et à la surveillance. La RBNS peut s’atténuer en plusieurs semaines après l’arrêt de l’exposition, quoiqu’une RBNS anormale persiste souvent encore plusieurs mois, voire plusieurs années. Chez les sujets atteints d’AP induit par des agents irritants, la RBNS ne devrait pas varier avec l’exposition ou les symptômes.
Il est important de poser le diagnostic précis d’un AP en raison des importantes conséquences négatives de sa sous- ou sa surestimation. Chez les travailleurs atteints d’AP ou présentant un risque d’apparition d’AP, la détection en temps opportun, de même que l’identification et le contrôle des expositions professionnelles déclenchant l’asthme améliorent les chances de prévention ou de guérison complète. Cette prévention primaire peut grandement réduire le coût financier et humain de l’asthme invalidant chronique. En revanche, comme le diagnostic d’AP peut nécessiter une reconversion professionnelle complète ou des interventions coûteuses sur le lieu de travail, la distinction entre l’AP et l’asthme non professionnel peut permettre d’éviter, à l’employeur comme au travailleur, des charges financières et sociales inutiles.
Plusieurs définitions de l’AP ont été proposées, adaptées à des circonstances différentes. Il est possible que des définitions valables pour le dépistage ou la surveillance des travailleurs (Hoffman et coll., 1990) ne conviennent pas parfaitement à des objectifs cliniques ou à des fins de réparation. Des chercheurs se sont mis d’accord pour définir l’AP comme une «maladie caractérisée par une limitation variable du débit ventilatoire ou une hyperréactivité des voies respiratoires, due à des causes et conditions imputables à un environnement professionnel particulier et non à des stimuli rencontrés en dehors du lieu de travail» (Bernstein et coll., 1993). Cette description a été adoptée en tant que définition nosologique et est résumée au tableau 10.6 (Chan-Yeung, 1995).
|
Critères diagnostiques de l�asthme professionnel (les quatre sont obligatoires, A-D):
Critères diagnostiques de RADS (les sept sont obligatoires):
Critères diagnostiques de l�asthme aggravé par le travail (AAT):
|
1 Une définition médicale exigeant A, C et l�un quelconque des critères D1 à D5 peut être utile dans la surveillance de l�AP, de l�AAT et du RADS.
Source: Chan-Yeung, 1995.
Le bilan clinique complet d’un AP peut être long, coûteux et difficile. Il peut exiger des tests diagnostiques d’arrêt et de reprise du travail et contraint souvent le patient à effectuer des mesures en série du débit expiratoire de pointe (DEP). Les médecins peuvent avoir des difficultés à faire pratiquer certains éléments du bilan clinique (par exemple, des tests bronchiques spécifiques ou des tests quantitatifs en série pour déterminer la RBNS). D’autres éléments peuvent tout simplement être irréalisables (patient qui ne travaille plus, moyens diagnostiques non disponibles, mesures en série du DEP incorrectes). Le soin apporté à l’examen clinique devrait permettre d’améliorer la précision diagnostique. Pour chaque patient, les décisions concernant l’importance du bilan médical à envisager devront mettre en balance le coût de ce bilan et les conséquences cliniques, sociales, financières et sanitaires d’un diagnostic confirmant ou excluant à tort un cas d’AP.
Compte tenu de ces difficultés, une approche progressive du diagnostic de l’AP est décrite au tableau 10.7. Il s’agit d’un guide général destiné à faciliter la réalisation d’un bilan diagnostique précis, pratique et efficace, sachant que certaines des procédures suggérées sont irréalisables dans certains établissements. Le diagnostic de l’AP passe par le diagnostic de l’asthme et l’établissement de la relation entre l’asthme et la ou les expositions professionnelles. Après chaque étape et pour chaque patient, le médecin devra déterminer si le niveau diagnostique atteint avec certitude permet de prendre les décisions adéquates ou s’il faut passer à l’étape suivante. Si l’on dispose des installations et des moyens nécessaires, le temps et le coût de la poursuite du bilan clinique sont généralement justifiés par l’importance de l’établissement exact de la relation entre l’asthme et le travail. Les principaux aspects des procédures diagnostiques de l’AP sont résumés et des renseignements précis figurent dans plusieurs des études citées (Chan-Yeung 1995; Bernstein et coll., 1993). La consultation d’un médecin spécialiste de l’AP peut être utile, car le processus diagnostique peut être difficile.
|
Etape 1 |
Interrogatoire approfondi portant sur les antécédents médicaux et professionnels et examen clinique orienté |
|
Etape 2 |
Etude physiologique de l�obstruction réversible des voies aériennes ou de l�hyperréactivité bronchique non spécifique |
|
Etape 3 |
Bilan immunologique si nécessaire |
|
Evaluation de la situation professionnelle: |
|
|
Travaille actuellement: dans ce cas, passer d�abord à l�étape 4 |
|
|
Etape 4 |
Evaluation clinique de l�asthme au travail ou essai diagnostique de reprise du travail |
|
Etape 5 |
Evaluation clinique de l�asthme en dehors du travail ou essai diagnostique d�arrêt du travail |
|
Etape 6 |
Test de provocation bronchique spécifique ou test de provocation sur le lieu de travail. Si elle est réalisable pour les expositions présumées responsables, cette étape peut être effectuée avant l�étape 4 |
Ce tableau est destiné à servir de guide général pour faciliter un bilan diagnostique pratique et efficace. Il est recommandé aux médecins chargés du diagnostic et du traitement de l�AP de consulter également la documentation clinique récente.
Le RADS secondaire à une exposition professionnelle est généralement considéré comme une sous-classe de l’AP. On en fait cliniquement le diagnostic en se fondant sur les critères énoncés au tableau 10.6. Les patients qui ont subi une agression respiratoire significative suite à l’inhalation d’agents irritants en forte concentration devraient être examinés pour détecter des symptômes persistants et la présence d’une obstruction ventilatoire peu après l’événement. Si les circonstances cliniques sont compatibles avec un RADS, la suite du bilan doit, en l’absence de contre-indication, comporter une détermination quantitative de la RBNS. Un asthme préexistant peut être fréquent et entraîner une lourde invalidité qui peut être évitée, mais les études scientifiques sur le diagnostic, le traitement et le pronostic sont peu nombreuses. Comme le résume le tableau 10.6, on admet qu’il y a asthme préexistant quand des symptômes asthmatiques ont précédé l’exposition causale suspectée et sont nettement aggravés par l’environnement professionnel. Cette aggravation peut être prouvée par des réactions physiologiques ou par un examen attentif des dossiers médicaux et des traitements prescrits. En définitive, c’est sur le jugement clinique que repose le diagnostic d’AP ou d’asthme préexistant chez les patients ayant des antécédents d’asthme en rémission qui font des récidives de symptômes asthmatiques et qui satisfont, par ailleurs, aux critères du diagnostic d’AP. On a estimé qu’une période asymptomatique d’une année était suffisamment longue pour que l’apparition de nouveaux symptômes indique qu’il peut s’agir d’AP dû à une exposition professionnelle; les avis ne sont toutefois pas unanimes.
Les premiers soupçons éveillés par le tableau clinique et les conditions de travail sont d’une importance primordiale étant donné qu’un diagnostic et un traitement rapides augmentent les chances de guérison. Le diagnostic d’AP ou d’AAT devrait être envisagé dans tous les cas d’asthme qui se déclarent chez un sujet adulte actif (surtout s’il s’agit de cas récents) ou quand l’asthme s’est fortement aggravé. Un AP devrait également être envisagé chez tous les autres sujets présentant des troubles asthmatiformes qui exercent des professions les exposant à des agents provoquant des crises d’asthme ou qui pensent que leurs symptômes sont liés à leur travail.
Il convient de procéder à un interrogatoire attentif des patients susceptibles d’avoir un AP afin de connaître leurs antécédents médicaux et professionnels ou environnementaux, en mettant l’accent sur la nature et la date d’apparition des symptômes et du diagnostic de l’asthme et sur toute exposition potentiellement suspecte à cette époque. Il convient d’évaluer la compatibilité des antécédents médicaux avec le tableau clinique de l’AP décrit ci-dessus, en particulier la succession dans le temps des symptômes par rapport au travail effectué et aux changements survenus dans les expositions liées au travail. Les modalités d’utilisation des traitements antiasthmatiques et leurs modifications, de même que la durée minimale d’arrêt de travail permettant l’amélioration des symptômes devraient être notées. Parmi les questions qui ont de l’importance, mentionnons les antécédents de maladie respiratoire, les manifestations allergiques/atopiques, le tabagisme et les autres expositions toxiques, ainsi que les antécédents familiaux d’allergie.
Les expositions professionnelles et environnementales à des agents ou à des procédés asthmogènes devraient être soigneusement examinées, avec preuves à l’appui si possible. En cas de suspicion, il est recommandé d’examiner la situation par rapport à une liste exhaustive d’agents accusés d’induire un AP (Harber, Schenker et Balmes, 1996; Chan-Yeung et Malo, 1994; Bernstein et coll., 1993; Rom, 1992b), bien qu’il soit relativement fréquent de ne pas parvenir à identifier les agents spécifiques et que l’induction d’un asthme par des agents non encore répertoriés soit possible. Le tableau 10.8 en fournit quelques illustrations. Les antécédents professionnels devraient inclure une description de la profession actuelle et des emplois antérieurs, avec les dates, le nom de la ou des professions, les tâches et les expositions, en insistant sur l’emploi actuel et l’emploi occupé au moment de l’apparition des symptômes. Les autres antécédents environnementaux devraient comporter une revue des expositions domestiques ou communautaires susceptibles d’induire un asthme. Il est utile de débuter l’historique des expositions de manière ouverte, en utilisant de grandes catégories d’agents aéroportés: les poussières (en particulier les poussières organiques d’origine animale, végétale ou microbienne), les substances chimiques, les produits pharmaceutiques et les fumées et les gaz irritants ou visibles. Le patient peut identifier des agents spécifiques, des processus de travail ou des catégories génériques d’agents qui ont déclenché des troubles. Il peut être utile de lui demander de décrire, dans l’ordre chronologique, les diverses activités menées au cours de la dernière journée de travail où des symptômes se sont manifestés, ainsi que les expositions incriminées. Il peut aussi être important de connaître la nature des matières utilisées par les collègues de travail ou libérées en grande quantité de façon accidentelle ou de quelque autre façon. Des informations supplémentaires peuvent souvent être obtenues sur le nom des produits et leurs composants, ainsi que le nom, l’adresse et le numéro de téléphone du fabricant. Des agents spécifiques peuvent être identifiés en appelant le fabricant ou à partir de nombreuses autres sources: manuels, bases de données sur CD-ROM ou centres antipoison. L’AP étant fréquemment dû à de faibles concentrations d’aéroallergènes, les évaluations qualitatives des expositions faites dans le cadre d’inspections des lieux et les mesures de contrôle sont souvent plus utiles que les mesures quantitatives des polluants atmosphériques.
|
Classification |
Sous-groupes |
Exemples de substances |
Exemples de professions et de branches |
|
Protéines antigéniques de masse moléculaire élevée |
Substances d�origine animale |
Animaux de laboratoire, crabes, fruits de mer et poissons, acariens, insectes |
Gardiens d�animaux, agriculteurs. Transformation des produits alimentaires |
|
|
Substances d�origine végétale |
Poussières de farines et de céréales, gants en latex, enzymes bactériennes, poussières de graines de ricin, gommes végétales |
Boulangeries, personnels de santé, fabrication de détergents, industries alimentaires |
|
Agents sensibilisants chimiques de faible masse moléculaire |
Plastifiants, peintures bicomposées, adhésifs, mousses |
Isocyanates, anhydrides d�acides, amines |
Peinture par pulvérisation, vernissage, travail du bois |
|
|
Métaux |
Sels de platine, cobalt |
Affinage du platine, meulage des métaux |
|
|
Poussières de bois |
Cèdre (acide plicatique), chêne |
Scieries, menuiseries |
|
|
Produits pharmaceutiques |
Psyllium, antibiotiques |
Fabrication et emballage des produits pharmaceutiques |
|
Autres substances chimiques |
|
Chloramine T, fumées de poly(chlorure de vinyle), insecticides organophosphorés |
Travaux de conciergerie, conditionnement de la viande |
Les antécédents cliniques servent davantage à exclure qu’à confirmer un diagnostic d’AP; des antécédents librement rapportés au médecin valent mieux qu’un questionnaire fermé. Une étude a comparé les résultats de témoignages sur les antécédents cliniques faits en présence de spécialistes de l’AP à un «étalon or» de tests de stimulation bronchique spécifique réalisés auprès de 162 patients susceptibles d’être atteints d’AP. Les investigateurs ont rapporté que, d’après l’examen d’antécédents cliniques portant à croire que le sujet était atteint d’AP, la sensibilité était de 87%, la spécificité de 55%, la valeur pronostique positive de 63% et la valeur pronostique négative de 83% (Malo et coll., 1991). Dans ce groupe de patients, la prévalence de l’asthme était de 80% et celle de l’AP de 46%. Dans d’autres groupes de patients, les valeurs pronostiques positives tirées d’un questionnaire fermé variaient entre 8 et 52% pour un grand nombre d’expositions professionnelles (Bernstein et coll., 1993). L’extrapolation de ces résultats à d’autres situations nécessite une évaluation médicale.
Un examen médical est parfois utile et il convient de noter les observations relatives à l’asthme (râles, polypes nasaux, dermatite eczémateuse), à une irritation ou à une allergie respiratoire (rhinite, conjonctivite) ou à d’autres causes potentielles de troubles.
Il est possible de sauter l’étape 2 s’il existe déjà suffisamment d’arguments physiologiques en faveur du diagnostic d’asthme (NAEP, 1991). Dans le cas contraire, il faut faire pratiquer des tests spirométriques par un technicien, de préférence après une journée de travail, un jour où le patient présente des symptômes asthmatiques. Si la spirométrie met en évidence une obstruction des voies respiratoires levée par un bronchodilatateur, le diagnostic d’asthme est confirmé. Chez les patients sans signes spirométriques nets de limitation ventilatoire, il faut pratiquer une étude quantitative de la RBNS avec administration de méthacholine ou d’histamine, autant que possible le même jour. Dans ce cas, l’étude quantitative de la RBNS est un examen clé pour deux raisons. Premièrement, elle permet souvent d’identifier les patients atteints d’un AP léger ou au stade initial, c’est-à-dire ceux qui ont le plus de chances de guérison, alors que la détection de ces cas serait impossible si l’on ne poussait pas les tests plus loin que la spirométrie normale. Deuxièmement, si la RBNS est normale chez un travailleur actuellement soumis à une exposition professionnelle associée à ses symptômes, l’AP peut généralement être éliminé sans autre examen. En cas d’anomalie, on peut passer aux étapes 3 ou 4 et il peut être utile d’attribuer une valeur à la RBNS afin de vérifier si l’état du patient s’est amélioré après le test diagnostique de cessation de l’exposition présumée responsable (étape 5). Si la spirométrie met en évidence une limitation ventilatoire importante qui ne s’améliore pas après l’inhalation d’un bronchodilatateur, il faut envisager un nouveau bilan après un essai thérapeutique de plus longue durée, avec administration de corticoïdes (ATS, 1995; NAEP, 1991).
Des tests cutanés ou sérologiques (le test RAST, par exemple) peuvent révéler une sensibilisation immunologique à un agent spécifique du lieu de travail. Ces tests immunologiques ont été utilisés pour confirmer le lien entre l’asthme et le travail et, dans certains cas, se dispenser de faire des tests de provocation utilisant des substances inhalées spécifiques. Par exemple, les tests bronchiques spécifiques ultérieurs ont permis de confirmer l’AP chez environ 80% des patients exposés au psyllium dont l’histoire clinique était compatible avec un AP, avec un asthme confirmé ou avec une hyperréactivité bronchique et qui présentaient des signes de sensibilisation immunologique à cette espèce (Malo et coll., 1990). Dans la plupart des cas, la signification diagnostique des tests immunologiques négatifs est moins claire. La sensibilité diagnostique de ces tests dépend essentiellement de l’inclusion dans l’épreuve de tous les antigènes présumés responsables présents sur le lieu de travail ou de complexes haptène-protéine. Bien que la conséquence d’une sensibilisation d’un travailleur asymptomatique soit mal connue, l’analyse des résultats groupés peut contribuer à l’évaluation des contrôles environnementaux. L’évaluation immunologique est surtout intéressante dans le cas des agents pour lesquels on dispose de tests in vitro standardisés ou de cuti-réactions, tels que les sels de platine et les enzymes détergentes. Malheureusement, la plupart des allergènes professionnels qui seraient intéressants ne sont pas disponibles actuellement sur le marché. L’utilisation de solutions non commercialisées pour les cuti-réactions a parfois entraîné des réactions graves, notamment des réactions anaphylactiques, de sorte que la prudence s’impose.
Si les résultats des étapes 1 et 2 sont compatibles avec un AP, il faut poursuivre le bilan lorsqu’on le peut. L’ordre et l’importance des autres examens dépendent des moyens diagnostiques disponibles, de la situation professionnelle du patient et de la faisabilité d’essais diagnostiques d’arrêt et de reprise du travail, comme l’indique le tableau 10.7. S’il est impossible de procéder à d’autres examens, le diagnostic doit reposer sur les informations disponibles à ce moment.
En règle générale, l’épreuve physiologique d’obstruction des voies respiratoires la plus accessible est la spirométrie. Pour améliorer la reproductibilité, la spirométrie devrait être effectuée par un technicien compétent. Malheureusement, la spirométrie réalisée sur une seule journée en alternant les postes de travail, avant et après chaque changement de poste, n’est pas une méthode efficace ou précise de détection des obstructions des voies respiratoires d’origine professionnelle. Il devrait être possible d’améliorer le diagnostic en faisant chaque jour de nombreuses épreuves spirométriques, pendant et après plusieurs journées de travail, mais l’efficacité de cette méthode n’a pas encore été évaluée de façon satisfaisante.
En raison des lacunes de la spirométrie avec alternance des postes de travail, les mesures en série du débit expiratoire de pointe (DEP) sont devenues un élément important du diagnostic de l’AP. A l’aide d’un appareil de mesure portable peu coûteux, les mesures du DEP sont enregistrées toutes les deux heures pendant le temps de veille. Pour améliorer la sensibilité, les mesures doivent avoir lieu au cours d’une période où le travailleur est exposé aux agents présumés responsables et alors qu’il présente une série de symptômes liés au travail. Trois mesures sont effectuées à chaque fois et tous les jours, au travail et pendant les périodes de repos. Les mesures devraient se poursuivre pendant seize jours consécutifs au moins (par exemple, deux semaines de cinq jours ouvrables plus trois fins de semaine de repos) si le patient peut continuer à travailler en toute sécurité. Les mesures du DEP sont notées dans un protocole, ainsi que les heures de travail, les symptômes, l’utilisation de bronchodilatateurs et les expositions importantes. L’interprétation est facilitée en présentant les résultats sous forme graphique. Certaines observations sont évocatrices d’un AP, mais aucune n’est pathognomonique et il est souvent utile d’en confier l’interprétation à un spécialiste. Les mesures en série du DEP ont l’avantage d’être peu coûteuses et d’offrir une corrélation satisfaisante avec les résultats des tests de provocation bronchique; la méthode a toutefois plusieurs inconvénients. Elle exige notamment une coopération étroite du patient et les résultats ne sont pas nécessairement précis; en outre, il n’existe pas de méthode normalisée pour l’interprétation des données; certains patients sont obligés de prendre une ou deux semaines consécutives de repos pour que les mesures confirment que leur état s’améliore sensiblement. Les spiromètres enregistreurs électroniques portables, conçus pour l’autocontrôle des patients, permettent de remédier à certains inconvénients des mesures en série du DEP; encore faut-il en avoir à disposition.
Les médicaments antiasthmatiques ont tendance à réduire l’effet des expositions professionnelles sur les mesures d’exploration ventilatoire. Il n’est toutefois pas recommandé d’interrompre les traitements au cours de la surveillance des débits respiratoires au travail. Au contraire, le patient devrait rester sous médication (à dose faible, mais constante, d’anti-inflammatoires) pendant toute la période d’établissement du diagnostic; il faut également surveiller de près les symptômes et le débit respiratoire et noter dans le protocole si l’on a utilisé des bronchodilatateurs à courte durée d’action pour enrayer les symptômes.
L’absence de variation du DEP pendant les heures de travail régulières du patient n’exclut pas le diagnostic d’AP; dans de nombreux cas, en effet, il faudra plus que les deux jours d’une fin de semaine pour qu’une amélioration considérable du DEP se manifeste. Dans ce cas, un essai diagnostique d’arrêt de travail prolongé (étape 5) devrait être envisagé. Si une mesure quantitative de la RBNS n’a pas encore été effectuée et si le patient ne présente aucune contre-indication médicale, il convient d’y procéder immédiatement après deux semaines au moins d’exposition sur le lieu de travail.
Cette étape consiste à réaliser des mesures en série du DEP quotidiennement toutes les deux heures, et cela pendant un congé d’au moins neuf jours (par exemple, cinq jours d’arrêt de travail précédés et suivis d’une fin de semaine). Si ces mesures, comparées à celles effectuées quotidiennement au travail, ne suffisent pas pour diagnostiquer un AP, elles devraient être poursuivies pendant une deuxième semaine consécutive d’arrêt de travail. Après deux semaines de repos ou plus, il est possible d’effectuer une mesure quantitative de la RBNS et de la comparer à la valeur mesurée en période de travail. Si aucune mesure en série du DEP n’a été pratiquée pendant deux semaines de travail au moins, il est alors possible de procéder à un essai diagnostique d’arrêt de travail (voir l’étape 4), après avoir soigneusement informé les intéressés et en étroite collaboration avec le médecin traitant. L’étape 5 joue souvent un rôle extrêmement important dans la confirmation ou l’exclusion du diagnostic d’AP, bien qu’elle puisse également être l’étape la plus délicate et onéreuse. Si un arrêt de travail prolongé est tenté, la meilleure façon d’optimiser la procédure diagnostique et son efficacité consiste à y inclure des mesures du DEP, du VEMS et de la RBNS pour que le bilan soit complet. Une consultation médicale hebdomadaire destinée à conseiller le patient et à analyser le tracé du DEP peut contribuer à l’obtention de résultats complets et précis. Lorsque la surveillance du patient pendant deux semaines de travail et deux semaines de repos au moins ne suffit pas pour apporter la preuve diagnostique, il faut alors envisager l’étape 6, si elle est réalisable.
Les tests de provocation bronchique spécifique utilisant une chambre d’exposition et des niveaux d’exposition normalisés ont été qualifiés d’«étalon or» du diagnostic de l’AP. Ils ont pour avantage de confirmer formellement l’AP en permettant d’identifier une réponse asthmatique à un taux subirritant d’agents sensibilisants spécifiques qu’il est ensuite possible d’éviter soigneusement. De toutes les méthodes diagnostiques, c’est la seule qui permette d’établir une distinction fiable entre l’asthme induit par un agent sensibilisant et une provocation par des agents irritants. Cette méthode présente toutefois plusieurs inconvénients, notamment son coût et la nécessité d’une surveillance attentive ou d’une hospitalisation pendant plusieurs jours; en outre, elle n’est applicable que dans quelques centres spécialisés. Des faux négatifs peuvent s’observer s’il n’est pas possible d’appliquer la méthodologie standard à tous les agents suspectés, si certains agents sont soupçonnés à tort ou s’il s’est écoulé trop de temps entre la dernière exposition et le test. Par ailleurs, des faux positifs peuvent s’observer si les niveaux d’exposition entraînant des phénomènes d’irritation ont été atteints par inadvertance. Pour toutes ces raisons, les tests de provocation bronchique spécifique restent une procédure expérimentale dans la plupart des cas d’AP.
Les tests de provocation sur le lieu de travail consistent en une série d’épreuves spirométriques effectuées à fréquence élevée, sous la direction d’un technicien (par exemple, toutes les heures), avant et pendant toute la durée de l’exposition aux agents ou aux processus présumés responsables tout au long d’une journée de travail. Ils peuvent être plus sensibles que les tests de provocation bronchique spécifique, car ils font intervenir les expositions réelles; mais, comme l’obstruction des voies respiratoires peut être déclenchée par des agents irritants ou sensibilisants, la positivité des tests ne traduit pas obligatoirement une sensibilisation. Ces tests exigent également la coopération de l’employeur et demandent beaucoup de temps au technicien qui doit utiliser un spiromètre portable. Les deux méthodes mentionnées comportent certains risques de déclenchement d’une crise d’asthme grave et devraient donc être appliquées sous surveillance étroite de spécialistes en la matière.
Le traitement de l’AP comprend des interventions médicales et préventives adaptées à chaque patient, ainsi que le recours à certaines mesures de prévention dans les milieux de travail présentant un risque élevé d’AP. Le traitement médical est le même que celui de l’asthme non professionnel et a fait l’objet d’une étude approfondie (NAEP, 1991). Le traitement médical seul permet rarement un contrôle symptomatique correct et la prévention par la limitation ou l’arrêt de l’exposition fait partie intégrante du traitement. Celui-ci doit être précédé du diagnostic exact et de l’identification des expositions et conditions de travail responsables. En ce qui concerne l’AP induit par un agent sensibilisant, la réduction de l’exposition à cet agent ne suffit généralement pas pour faire disparaître complètement les symptômes. Des épisodes asthmatiques graves ou une aggravation progressive de la maladie peuvent être causés par des expositions à de très faibles concentrations de l’agent et il est recommandé, par conséquent, de soustraire complètement et définitivement le sujet à toute exposition dangereuse. Dans certains cas, il peut être indispensable de procéder en temps utile à la réadaptation professionnelle ou au recyclage du travailleur. Si une éviction totale de l’exposition est impossible, sa forte réduction, associée à une surveillance médicale étroite et à un traitement médical approprié, peut être une solution acceptable, bien qu’elle ne soit pas toujours applicable et que son efficacité à long terme n’ait pas été évaluée. Ainsi, il serait difficile de justifier la toxicité d’une corticothérapie systémique à long terme destinée à permettre au patient de continuer à exercer sa profession. En ce qui concerne l’asthme induit ou déclenché par des agents irritants, la relation dose-réponse est facile à prévoir et une réduction des concentrations de l’agent irritant, accompagnée d’une surveillance médicale étroite, est probablement moins dangereuse et plus efficace que dans le cas de l’AP induit par un agent sensibilisant. Si le patient continue à travailler dans des conditions modifiées, le suivi médical devrait comprendre des consultations médicales fréquentes avec examen des mesures du DEP notées dans le protocole, un accès facilité aux services d’urgence et des épreuves spirométriques en série accompagnées ou non de tests de provocation à la méthacholine, selon les cas.
Dès qu’on soupçonne un lieu de travail d’être à haut risque en raison de l’apparition d’un cas sentinelle d’AP ou de l’utilisation d’agents asthmogènes connus, le recours à des mesures de santé publique peut être extrêmement utile. Le dépistage précoce, un traitement efficace, la prévention d’une incapacité de travail parmi les travailleurs atteints d’AP et la prévention de nouveaux cas sont primordiaux, au même titre que l’identification du ou des agents spécifiques et des processus industriels responsables. Dans un premier temps, il est utile de mener sur place une enquête par questionnaire et d’évaluer les réponses en fonction des critères A, B, C et D1 ou D5 de la définition des cas d’AP. Cette façon de procéder permet de repérer les sujets pour lesquels une évaluation clinique plus poussée s’impose, tout en facilitant la détection des agents ou des conditions de travail responsables de la situation. L’évaluation des résultats collectifs peut contribuer à décider s’il convient d’approfondir les investigations sur le terrain ou d’envisager d’autres interventions et, si c’est le cas, d’indiquer où les efforts de prévention ultérieurs pourront être les plus efficaces. Un questionnaire ne permet cependant pas, dans ce cas, de porter un diagnostic d’AP à l’échelon individuel, car la valeur prédictive des réponses collectives n’est pas suffisamment élevée. Si l’on veut atteindre un degré de certitude diagnostique plus élevé, on peut également envisager un dépistage médical faisant appel à des procédures diagnostiques telles que la spirométrie, la détermination quantitative de la RBNS, des mesures en série du DEP et des tests immunologiques. Dans les lieux de travail à risque confirmé, il peut être utile d’assurer une surveillance suivie et un programme de dépistage. Cependant, l’exclusion sélective des travailleurs asymptomatiques ayant des antécédents d’atopie ou d’autres facteurs sensibilisants potentiels liés au travail et présumés à haut risque provoquerait le retrait d’un grand nombre de travailleurs pour prévenir un nombre relativement restreint de cas d’AP; les études publiées jusqu’à présent ne confirment pas le bien-fondé d’une telle démarche.
En réduisant les concentrations de substances nocives, ou en les éliminant, ou encore en évitant, par une réorganisation du travail, les périodes d’exposition à des concentrations élevées, on protégera les collègues de travail du «cas sentinelle» contre une sensibilisation aux substances incriminées et contre le développement d’un AP. Il convient de mettre en place, selon les cas et dans l’ordre de priorité ci-après, les diverses mesures dont on dispose: substitution, prévention technique et dispositions administratives, équipement de protection individuelle, éducation des travailleurs et des cadres. Les employeurs soucieux de faire de la prévention mettront ces mesures en œuvre en totalité ou en partie; si ces mesures s’avèrent inefficaces et si le risque demeure élevé pour les travailleurs, il peut être utile de faire appel aux services d’inspection gouvernementaux.
Par incapacité fonctionnelle, on entend un trouble fonctionnel résultant d’un état morbide, alors que l’invalidité se rapporte au retentissement global de l’incapacité fonctionnelle sur la vie du patient, compte tenu de nombreux facteurs non médicaux tels que l’âge et le statut socio-économique (ATS, 1995).
L’incapacité fonctionnelle est évaluée par le médecin et peut inclure un indice d’incapacité calculé, ainsi que d’autres considérations cliniques. L’indice d’incapacité est fondé sur: 1) le degré de limitation ventilatoire après administration d’un bronchodilatateur; 2) le degré de réversibilité de la limitation ventilatoire avec un bronchodilatateur ou l’hyperréactivité des voies respiratoires lors de la mesure quantitative de la RBNS; 3) le traitement minimal nécessaire pour contrôler l’asthme. L’autre élément majeur de l’évaluation d’une incapacité fonctionnelle est l’opinion du médecin quant à l’aptitude du patient à travailler dans l’environnement responsable de son asthme. Par exemple, un patient atteint d’AP induit par un agent sensibilisant peut souffrir d’une incapacité fonctionnelle seulement lorsqu’il est en présence de l’agent auquel il a été sensibilisé. S’il ne présente des troubles que lorsqu’il est exposé à cet agent, il pourra exercer d’autres activités, mais il sera définitivement incapable d’exercer le métier dans lequel il avait acquis le plus de compétence et d’expérience.
L’évaluation de l’invalidité due à l’asthme (y compris l’AP) nécessite la prise en compte non seulement du handicap, mais aussi d’autres facteurs non médicaux retentissant sur la capacité de travail et la vie de tous les jours. L’invalidité est d’abord évaluée par le médecin, qui doit identifier tous les facteurs intervenant dans le retentissement de l’altération sur la vie du patient. De nombreux facteurs tels que la profession, le niveau d’instruction, la possession d’autres aptitudes, les conditions économiques et d’autres facteurs sociaux peuvent se traduire par différents degrés d’invalidité chez des sujets ayant la même incapacité fonctionnelle. Ces informations sont ensuite utilisées par l’administration pour déterminer le degré d’incapacité aux fins de réparation.
L’incapacité fonctionnelle et l’invalidité peuvent être temporaires ou permanentes selon la probabilité d’une amélioration significative et si des contrôles efficaces de l’exposition sont instaurés sur le lieu de travail. Ainsi, un sujet atteint d’un AP induit par un agent sensibilisant sera, en règle générale, jugé définitivement et totalement inapte à toute profession impliquant une exposition à l’agent responsable. Si, en revanche, les symptômes disparaissent partiellement ou totalement après l’arrêt de l’exposition, le sujet pourra être considéré comme moins inapte ou apte à d’autres travaux. On considère souvent cela comme une incapacité fonctionnelle ou une invalidité partielle permanente, mais la terminologie peut varier. Un asthmatique dont l’asthme est déclenché de façon dose-dépendante par des agents irritants présents sur le lieu de travail devrait être jugé atteint d’une incapacité temporaire quand il est symptomatique, et être jugé moins inapte ou apte en cas d’instauration de contrôles satisfaisants de l’exposition assurant une atténuation efficace ou la disparition des symptômes. En l’absence de mesures adéquates de limitation de l’exposition, le même sujet devra peut-être être jugé comme définitivement inapte à l’exercice de son métier, avec recommandation d’arrêt pour raison médicale. Si nécessaire, des évaluations de l’incapacité fonctionnelle ou de l’invalidité à long terme pourront être répétées deux ans après la réduction ou la disparition de l’exposition, quand on estimera que l’amélioration de l’AP a atteint un palier. Si le patient continue à travailler, la surveillance médicale devrait être poursuivie et l’évaluation de l’inaptitude ou de l’invalidité répétée au besoin.
En cas d’invalidité due à un AP ou à un AAT, le travailleur peut prétendre à une prise en charge de ses frais médicaux ou à une indemnisation pour perte de salaire, ou aux deux à la fois. Outre qu’elle réduit directement l’impact financier de l’invalidité sur les travailleurs et leur famille, l’indemnisation peut être nécessaire pour assurer un traitement médical correct, l’instauration de mesures préventives et l’accès à la réinsertion professionnelle. Une bonne connaissance des questions médico-légales de la part du travailleur et de son médecin peut être nécessaire pour garantir que le bilan diagnostique satisfait aux obligations locales et qu’il ne compromet pas les droits du travailleur affecté.
Quand on parle de faire des économies, on pense surtout aux insuffisances des systèmes de réparation. En réalité, si l’on veut réduire les charges financières et les dépenses de santé imposées à la société par l’AP et l’AAT, il faudrait s’inquiéter bien davantage de l’efficacité des moyens techniques mis en œuvre pour détecter et combattre, et même supprimer, de façon radicale, les risques d’exposition aux agents nocifs responsables de nouveaux cas d’asthme.
L’AP est devenu la principale maladie respiratoire professionnelle dans de nombreux pays. Il est plus fréquent qu’on ne le pense habituellement, peut être sévère et invalidant et est généralement évitable. Son dépistage précoce et des mesures préventives efficaces peuvent réduire considérablement le risque d’invalidité permanente et le coût humain et financier élevé associé à l’asthme chronique. Pour de nombreuses raisons, l’AP justifie une attention accrue de la part des médecins praticiens, des services de sécurité et de santé, des chercheurs, des responsables de la politique sanitaire, des hygiénistes industriels et de toutes les autres personnes concernées par la prévention des maladies professionnelles.
Les poussières d’origine végétale, animale et microbienne ont toujours fait partie de l’environnement humain. Quand les premiers organismes aquatiques ont abordé la terre ferme il y a environ 450 millions d’années, ils ont rapidement élaboré des systèmes de défense contre les nombreuses substances nocives (pour la plupart d’origine végétale) présentes dans l’environnement terrestre. L’exposition à cet environnement ne pose généralement aucun problème spécifique, bien que les végétaux renferment diverses substances extrêmement toxiques, en particulier celles présentes dans les moisissures ou produites par celles-ci.
Au cours du développement de la civilisation, les conditions climatiques rencontrées dans quelques parties du monde ont exigé que certaines activités se déroulent en milieu clos. Dans les pays scandinaves, le battage du blé avait lieu à l’intérieur pendant l’hiver, d’après les chroniqueurs de l’Antiquité. Le confinement des processus dégageant de la poussière a entraîné des maladies chez les personnes exposées; l’une des premières maladies à avoir fait l’objet d’une publication a été rapportée par un évêque danois, Olaus Magnus, en 1555 (cité par Rask-Andersen, 1988). Il décrivait ainsi cette maladie des batteurs de grain scandinaves:
Pour séparer le grain de la balle, il faut veiller à choisir un jour de vent pour que la poussière du grain soit dispersée et ne provoque aucune lésion des organes vitaux des batteurs. Cette poussière est si fine qu’elle pénètre de façon pratiquement imperceptible dans la bouche et s’accumule dans la gorge. Si l’on ne l’élimine pas rapidement en buvant de la bière fraîche, il se peut que le batteur ne mange jamais, ou seulement pendant peu de temps, le grain qu’il a battu.
Avec l’introduction du traitement mécanique des matières organiques, les opérations mettant en œuvre d’importantes quantités de matières à l’intérieur de locaux mal ventilés ont provoqué des concentrations élevées de poussières en suspension dans l’air. Les observations de l’évêque Olaus Magnus et, plus tard, de Ramazzini (1713) ont été suivies de plusieurs constats sur les maladies et les poussières organiques au cours du XIXe siècle, en particulier chez les ouvriers des filatures de coton (Leach, 1863; Prausnitz, 1936). Par la suite, on a également décrit la maladie pulmonaire spécifique fréquemment observée chez les paysans manipulant des matières portant des moisissures (Campbell, 1932).
Au cours des dernières décennies, un grand nombre de rapports sur les maladies observées chez les personnes exposées aux poussières organiques ont été publiés. Au début, la plupart d’entre eux concernaient des personnes ayant recouru à une assistance médicale. Le nom des maladies, dans ce cas, était souvent lié à l’environnement particulier dans lequel la maladie avait été identifiée pour la première fois; il en est résulté un nombre incroyable de dénominations telles que poumon du fermier, poumon du champignonniste, poumon brun et fièvre des humidificateurs.
Avec le développement de l’épidémiologie moderne, on a obtenu des chiffres plus fiables sur l’incidence des maladies respiratoires professionnelles liées à l’inhalation de poussières organiques (Rylander, Donham et Peterson, 1986; Rylander et Peterson, 1990). Des progrès ont également été réalisés dans la connaissance des mécanismes physiopathologiques sous-jacents, en particulier la réponse inflammatoire (Henson et Murphy, 1989). Toutes ces avancées ont permis l’élaboration d’un tableau plus cohérent des maladies provoquées par les poussières organiques (Rylander et Jacobs, 1997).
On trouvera ci-après un aperçu des divers environnements comportant des poussières organiques et dans lesquels des cas de maladie ont été signalés, avec l’indication des diverses entités nosologiques elles-mêmes; il sera également question de la byssinose, ainsi que des mesures de prévention qui s’imposent.
Les poussières organiques sont des particules atmosphériques d’origine végétale, animale ou microbienne.
Le tableau 10.9 offre des exemples de milieux, de processus industriels et d’agents comportant un risque d’exposition à ces poussières organiques.
|
Agriculture Manipulation des grains, du foin et des autres productions végétales Traitement de la canne à sucre Serres Silos Animaux Porcheries, étables à vaches laitières Elevage et transformation de la volaille Animaux de laboratoire, animaux de ferme et animaux de compagnie Traitement des déchets Eaux usées et boues Déchets ménagers Compostage |
Industrie Travail des fibres végétales (coton, lin, chanvre, jute, sisal) Fermentation Abattage et travail du bois Boulangeries Produits biotechnologiques Bâtiments Eau contaminée des humidificateurs Prolifération microbienne sur les structures ou dans les conduits de ventilation |
On sait désormais que le développement des maladies causées par les poussières organiques est dû essentiellement à des agents spécifiques présents dans les poussières. Les poussières organiques contiennent une foule d’agents susceptibles d’avoir certains effets biologiques. Les principaux agents incriminés sont mentionnés au tableau 10.10.
|
Agents végétaux Tannins Histamine Acide plicatique Alcaloïdes (nicotine, par exemple) Cytochalasines |
Agents animaux Protéines Enzymes Agents microbiens Endotoxines (1-3)-beta-D-glucane Protéases Mycotoxines |
Le rôle relatif de chacun d’eux dans le développement des maladies — qu’il soit isolé ou associé à d’autres agents — est pratiquement inconnu. La plupart des informations dont on dispose se rapportent à des endotoxines bactériennes présentes dans toutes les poussières organiques.
Les endotoxines sont des liposaccharides fixés sur la surface externe des bactéries à Gram négatif. Elles possèdent de nombreuses propriétés biologiques. Après avoir été inhalées, elles provoquent une inflammation aiguë (Snella et Rylander, 1982; Brigham et Meyrick, 1986), réaction qui se caractérise par un afflux de granulocytes neutrophiles (leucocytes) dans les poumons et par la sécrétion de médiateurs de l’inflammation. Après des expositions répétées, l’inflammation s’atténue (il y a adaptation). La réaction se limite à la muqueuse des voies respiratoires et l’on ne constate pas d’atteinte importante du parenchyme pulmonaire.
Un autre agent spécifique des poussières organiques est le (1-3)-beta-D-glucane. Il s’agit d’un polyoside présent dans la structure pariétale des moisissures et de certaines bactéries. Il stimule la réponse inflammatoire provoquée par les endotoxines et altère la fonction des cellules inflammatoires, en particulier celle des macrophages et des lymphocytes T (Di Luzio, 1985; Fogelmark et coll., 1992).
Parmi les autres agents spécifiques présents dans les poussières organiques, on peut citer des protéines, des tannins, des protéases et d’autres enzymes, ainsi que les toxines sécrétées par les moisissures. On ne dispose que de très peu de données sur la concentration de ces agents dans les poussières organiques. Quelques-uns d’entre eux, comme les protéines et les enzymes, sont des allergènes.
Les maladies provoquées par les poussières organiques sont énumérées au tableau 10.11, avec les codes correspondants de la Classification internationale des maladies (CIM) (Rylander et Jacobs, 1994).
|
Bronchite et pneumopathies (CIM J40) Pneumopathies toxiques (fièvre d�inhalation, syndrome toxique des poussières organiques) Inflammation des voies respiratoires (inflammation des membranes muqueuses) Bronchite chronique (CIM J42) Pneumopathies d�hypersensibilisation (alvéolite allergique) (CIM J67) Asthme (CIM J45) Rhinite, conjonctivite |
La principale voie d’exposition aux poussières organiques est l’inhalation; ce sont donc surtout les effets pulmonaires qui ont retenu l’attention des chercheurs comme des cliniciens. Il ressort cependant de plus en plus nettement des études épidémiologiques publiées et des études de cas, ainsi que d’études isolées, que ces poussières ont également des effets systémiques. Le mécanisme impliqué semble être une inflammation locale de l’organe cible, le poumon, accompagnée d’une libération ultérieure de cytokines qui exercent soit des effets systémiques (Dunn, 1992; Michel et coll., 1991), soit un effet sur l’épithélium intestinal (Axmacher et coll., 1991). Les effets cliniques extrapulmonaires sont de la fièvre, des arthralgies, des effets neurosensoriels, des troubles cutanés et intestinaux, de la fatigue et des céphalées.
Les différentes entités nosologiques décrites au tableau 10.11 sont d’un diagnostic aisé dans les cas typiques; les aspects anatomopathologiques sous-jacents sont nettement différents. Cependant, un travailleur atteint d’une maladie due à une exposition à des poussières organiques présente souvent en réalité un mélange d’entités nosologiques. Un sujet peut souffrir d’une inflammation des voies respiratoires pendant un certain nombre d’années, puis faire de l’asthme du jour au lendemain en manifestant en outre des symptômes de pneumopathie toxique en cas d’exposition particulièrement intense. Un autre peut avoir une pneumopathie d’hypersensibilité infraclinique, accompagnée d’une hyperlymphocytose dans les voies respiratoires et développer une pneumonie toxique lorsque l’exposition est particulièrement forte.
La byssinose est un bon exemple du mélange d’entités morbides susceptibles d’apparaître. Cette maladie a été constatée pour la première fois dans les filatures de coton, mais ses diverses composantes pathologiques s’observent aussi dans d’autres environnements comportant des émissions de poussières organiques. On en trouvera une description générale ci-après.
Le premier constat de byssinose a été dressé dans les années mille huit cent. Prausnitz (1936) en a fait une étude classique comportant une partie clinique et une partie expérimentale; il a décrit comme suit les symptômes observés chez des ouvriers des filatures de coton:
Après plusieurs années de travail sans problème notable, à l’exception d’une petite toux, les ouvriers des filatures de coton remarquent une soudaine aggravation de leur toux qui devient sèche et extrêmement irritante [...] Ces crises surviennent habituellement le lundi [...], mais les symptômes commencent progressivement à s’étendre aux autres jours de la semaine; à terme, la différence s’estompe et les symptômes deviennent permanents.
Les premières études épidémiologiques ont été réalisées en Angleterre au cours des années cinquante (Schilling et coll., 1955; Schilling, 1956). Le diagnostic initial reposait sur l’apparition d’une oppression thoracique typique le lundi, confirmée par un questionnaire. Une échelle d’évaluation de la gravité de la byssinose, fondée sur le type et la périodicité des symptômes, a été établie (Mekky, Roach et Schilling, 1967; Schilling et coll., 1955). On s’est servi de la durée d’exposition pour mesurer la dose, et celle-ci a été mise en rapport avec l’importance de la réaction. Grâce aux interrogatoires cliniques d’un grand nombre de travailleurs, cette échelle d’évaluation a été modifiée par la suite afin de mieux refléter les durées nécessaires à la diminution du VEMS (Berry et coll., 1973).
On a pu, dans une étude, observer des différences de la prévalence de la byssinose dans les filatures traitant diverses sortes de coton (Jones et coll., 1979). Dans celles employant du coton de qualité supérieure pour fabriquer des fils plus fins, la prévalence était moindre que dans celles fabriquant des fils grossiers et utilisant un coton de qualité inférieure. C’est ainsi qu’outre l’intensité et la durée de l’exposition — deux variables dose-dépendantes — le type de poussière est devenu une variable importante de l’évaluation de l’exposition. On a montré par la suite que les différences de réponse des travailleurs exposés aux cotons grossiers ou de qualité moyenne ne dépendaient pas seulement du type de coton, mais aussi de l’hygrométrie, de la ventilation et d’autres variables liées à la fabrication, comme les différentes méthodes de traitement des fils (Berry et coll., 1973).
La connaissance plus approfondie que l’on a de la relation entre l’exposition à la poussière de coton et une réponse (qu’il s’agisse de symptômes ou des mesures objectives de la fonction pulmonaire) provient d’études américaines comparant des ouvriers travaillant sur un coton à 100% et d’autres ouvriers utilisant le même coton (mais dans un mélange de 50/50 avec des fibres synthétiques), avec des témoins non exposés au coton (Merchant et coll., 1973). On a trouvé la plus forte prévalence de byssinose chez les ouvriers travaillant avec du coton pur (100%) et cela, indépendamment du tabagisme, l’un des facteurs de confusion à prendre en compte. Cette relation semi-quantitative entre la dose et la réponse à la poussière de coton a été étudiée de façon plus approfondie dans un groupe d’ouvriers du textile stratifiés en fonction du sexe, de l’existence d’un tabagisme, de la zone de travail et du type de filature. Dans chacune de ces catégories, une relation a été mise en évidence entre les concentrations de poussière proches de la valeur plancher et la prévalence de la byssinose ou les modifications du volume expiratoire maximal seconde (VEMS).
Dans les études plus récentes, on s’est servi de la diminution du VEMS au cours de la journée de travail pour évaluer les effets de l’exposition; ce facteur fait également partie de la norme américaine sur la poussière de coton (Cotton Dust Standard).
La byssinose a été longtemps considérée comme une maladie particulière caractérisée par une série de symptômes, mais dont on ignorait la pathologie spécifique. Quelques auteurs ont suggéré qu’il s’agissait d’un asthme professionnel (Bouhuys, 1976). Lors d’un symposium tenu en 1987, on a analysé la symptomatologie et la physiopathologie de la maladie (Rylander et coll., 1987) et adopté l’idée que cette maladie comporte plusieurs entités cliniques, généralement liées à une exposition à des poussières organiques.
Des cas de pneumonie toxique ont été notés chez des ouvriers travaillant pour la première fois dans une filature, en particulier dans les ateliers où l’on procédait à l’ouverture des balles, au soufflage ou au cardage (Trice, 1940). En dépit du développement d’une accoutumance, les symptômes peuvent réapparaître ultérieurement après une exposition exceptionnellement intense.
L’inflammation des voies respiratoires est la maladie la plus largement répandue; elle peut présenter différents degrés de gravité, allant d’une simple irritation du nez et des voies aériennes à une toux sèche sévère accompagnée de dyspnée. L’inflammation entraîne une constriction des voies respiratoires et une diminution du VEMS. La réactivité des voies respiratoires est accrue, comme en témoignent les tests à la méthacholine ou à l’histamine. On s’est demandé si l’inflammation des voies respiratoires devait être considérée comme une entité nosologique en soi ou si elle ne constituait qu’un symptôme. Etant donné que les symptômes observés à la suite d’un examen clinique, à savoir une toux sévère et une constriction des voies respiratoires, peuvent aboutir à une diminution de la capacité de travail, il est justifié de considérer l’inflammation des voies respiratoires comme une maladie professionnelle.
La persistance d’une inflammation de ce type pendant plusieurs années peut déboucher sur une bronchite chronique, surtout chez les travailleurs soumis à des expositions importantes dans les ateliers de soufflage et de cardage. Le tableau clinique serait alors celui d’une broncho-pneumopathie chronique obstructive (BPCO).
Un asthme professionnel apparaît chez un petit pourcentage de travailleurs, mais il n’est généralement pas diagnostiqué dans les études transversales, car la maladie contraint les ouvriers à abandonner leur travail. Aucune pneumopathie d’hypersensibilité n’a été décelée dans les études épidémiologiques entreprises et aucun cas n’a été rapporté en relation avec une exposition à la poussière de coton. L’absence de pneumopathie d’hypersensibilité peut être due à la quantité relativement faible de moisissures dans le coton, car le coton moisi ne peut être utilisé.
Une sensation subjective d’oppression thoracique, plus fréquente le lundi, constitue le symptôme classique de l’exposition à la poussière de coton (Schilling et coll., 1955). Elle n’est cependant pas pathognomonique de l’exposition à la poussière de coton, car on la note également chez des sujets soumis à d’autres types de poussières organiques (Donham et coll., 1989). L’oppression thoracique apparaît lentement, en plusieurs années, mais elle peut également se produire chez des personnes non exposées antérieurement si le niveau d’exposition est élevé (Haglind et Rylander, 1984). La présence d’une oppression thoracique n’est pas directement liée à une diminution du VEMS. Son mécanisme physiopathologique demeure inexpliqué. Certains auteurs ont émis l’hypothèse que les symptômes seraient dus à une augmentation de l’adhésivité des plaquettes qui s’accumulent dans les capillaires pulmonaires et élèvent la pression artérielle pulmonaire. Il est probable que l’oppression thoracique implique une certaine forme de sensibilisation cellulaire, car des expositions répétées sont nécessaires pour que ce symptôme apparaisse. Cette hypothèse semble confirmée par l’étude des monocytes sanguins chez les travailleurs de l’industrie cotonnière (Beijer et coll., 1990); on a observé chez eux une plus grande aptitude à sécréter un facteur de coagulation, ce qui traduit une sensibilisation cellulaire par rapport à des sujets témoins.
L’évolution de la maladie a été décrite pour la première fois chez des ouvriers des filatures de coton, de lin et de chanvre. Au cours de la première phase de traitement du coton dans les filatures — ouverture des balles, soufflage et cardage — plus de la moitié des ouvriers peuvent présenter des troubles du type oppression thoracique ou inflammation des voies respiratoires. L’incidence diminue au fur et à mesure que le traitement du coton se poursuit, reflétant ainsi l’élimination progressive de l’agent responsable des fibres. La byssinose a été décrite dans tous les pays où les filatures de coton ont fait l’objet d’enquêtes. L’incidence est cependant anormalement faible dans certains pays comme l’Australie (Gun et coll., 1983).
Il est désormais généralement admis que des endotoxines bactériennes sont responsables de la pneumopathie toxique et de l’inflammation des voies respiratoires (Castellan et coll., 1987; Pernis et coll., 1961; Rylander, Haglind et Lundholm, 1985; Rylander et Haglind, 1986; Herbert et coll., 1992; Sigsgaard et coll., 1992). Des relations dose-effet ont été mises en évidence et les symptômes caractéristiques ont été provoqués par l’inhalation d’une endotoxine purifiée (Rylander et coll., 1989; Michel et coll., 1995). Bien que cela n’exclue pas la possibilité que d’autres agents puissent intervenir dans la pathogenèse, les endotoxines peuvent servir de marqueurs du risque morbide. Il est peu probable qu’elles soient responsables de l’apparition d’un asthme professionnel, mais elles peuvent faciliter l’action d’allergènes potentiels de la poussière de coton.
Le diagnostic de byssinose est généralement porté en ayant recours à des questionnaires comportant la question spécifique: «Ressentez-vous une oppression thoracique, et dans l’affirmative, quel jour de la semaine?». Les sujets ressentant une oppression thoracique le lundi matin sont considérés comme atteints de byssinose, conformément au protocole proposé par Schilling (1956). Une épreuve spirométrique peut être pratiquée et, en fonction des différentes combinaisons d’oppression thoracique et de diminution du VEMS, on a établi le schéma diagnostique présenté au tableau 10.12.
|
Degré � |
Oppression thoracique le premier jour de certaines semaines de travail |
|
Degré 1 |
Oppression thoracique le premier jour de chaque semaine de travail |
|
Degré 2 |
Oppression thoracique le premier jour et certains autres jours de la semaine de travail |
|
Degré 3 |
Symptômes du degré 2 accompagnés de signes établis d�incapacité permanente tels qu�une diminution de la tolérance à l�effort ou de la capacité ventilatoire |
Le traitement de la byssinose à ses premiers stades est symptomatique et la plupart des ouvriers apprennent à vivre avec la faible oppression thoracique et la bronchoconstriction qu’ils ressentent le lundi ou quand ils nettoient des machines ou effectuent des tâches analogues comportant une exposition supérieure à la normale. Les stades plus avancés d’inflammation des voies respiratoires ou d’oppression thoracique régulière, plusieurs jours par semaine, exigent le passage à des postes moins empoussiérés. L’asthme professionnel nécessite généralement un changement de travail.
La prévention en général est décrite en détail dans une autre partie de l’Encyclopédie. Les principes de base de la prévention, à savoir l’utilisation de produits de substitution, la limitation de l’exposition, la protection des travailleurs exposés et le dépistage des maladies, s’appliquent également à l’exposition à la poussière de coton.
En ce qui concerne le remplacement du produit ordinaire, on a proposé l’utilisation d’un coton à contamination bactérienne faible. Cette méthode trouve sa justification dans le fait que, selon des rapports datant de 1863 déjà, la prévalence des symptômes a augmenté chez les ouvriers après qu’ils ont été obligés de travailler avec du coton souillé (Leach, 1863). Il est également possible de passer à d’autres fibres, en particulier les fibres synthétiques, quoique cela ne soit pas toujours réalisable pour des questions de qualité des produits. Il n’existe actuellement aucune technique applicable à la production qui permette de réduire la teneur en endotoxines des fibres de coton.
En ce qui concerne la lutte contre les poussières, des programmes ont été mis en œuvre avec succès aux Etats-Unis et ailleurs (Jacobs, 1987). Ces programmes sont néanmoins onéreux et leur coût peut être prohibitif pour les pays en cours d’industrialisation (Corn, 1987).
En ce qui concerne la limitation de l’exposition, la mesure du taux d’empoussièrement n’est pas un indice suffisamment précis du risque. Selon le degré de contamination par des bactéries à Gram négatif et, par conséquent, par des endotoxines, un taux donné peut constituer un risque ou non. Pour les endotoxines, aucune directive officielle n’a été établie. On a recommandé de fixer la valeur seuil à 200 ng/m3 pour la pneumopathie toxique, à 100-200 ng/m3 pour la bronchoconstriction aiguë au cours de la journée de travail et à 10 ng/m3 pour l’inflammation des voies respiratoires (Rylander et Jacobs, 1997).
Il est important, en vue de la prévention, de connaître les facteurs de risque et les conséquences de l’exposition. Nos connaissances de base se sont fortement enrichies ces dernières années, mais une grande partie n’est pas encore présentée dans les manuels et les autres sources d’information. Un autre problème tient au fait que les symptômes et les signes des maladies respiratoires induites par les poussières organiques sont aspécifiques et se manifestent normalement au sein de la population, ce qui peut compliquer le dépistage précoce.
La diffusion correcte des connaissances relatives aux effets du coton et des autres poussières organiques exige l’établissement de programmes de formation adaptés. Ceux-ci ne devraient pas être axés uniquement sur les travailleurs soumis à une exposition potentielle, mais aussi sur les employeurs et le personnel des services de santé, en particulier les médecins inspecteurs du travail et les techniciens des services du travail. L’information doit porter sur l’origine du problème, la description des symptômes et de la maladie proprement dite, ainsi que sur les méthodes de protection. Un travailleur bien informé reconnaît plus facilement des symptômes d’origine professionnelle et les signale plus efficacement au médecin du travail. En ce qui concerne la surveillance médicale et le dépistage, les questionnaires sont un outil précieux. Plusieurs versions de questionnaires spécialement conçus pour diagnostiquer les maladies induites par les poussières organiques ont été décrites dans les ouvrages spécialisés (Rylander, Peterson et Donham, 1990; Schwartz et coll., 1995). Les épreuves fonctionnelles respiratoires représentent un instrument utile de surveillance et de diagnostic. Les mesures de la réactivité des voies respiratoires se sont également avérées utiles (Rylander et Bergström, 1993; Carvalheiro et coll., 1995). Les autres examens diagnostiques — tels que l’évaluation précise des médiateurs de l’inflammation ou de l’activité cellulaire — sont encore à l’état expérimental.
Cet article est tiré en partie de l'article sur la bérylliose rédigé par H.L. Hardy, L.B. Tepper et R.I. Chamberlain et publié dans la 3e édition de l'Enclopaedia of Occupational Health and Safety.
La bérylliose est une maladie systémique atteignant plusieurs organes, les manifestations pulmonaires étant les plus nombreuses et les plus fréquentes. Elle apparaît à la suite de l’exposition au béryllium utilisé pour fabriquer des alliages ou de nombreuses substances chimiques. La voie d’exposition est l’inhalation; la maladie peut être aiguë ou chronique. La forme aiguë est actuellement très rare et aucun cas n’a été rapporté depuis que des mesures d’hygiène industrielle visant à réduire l’exposition à des doses élevées ont été prises durant les années quarante, époque à laquelle le béryllium était utilisé en quantité dans l’industrie. Des cas de bérylliose chronique continuent à être signalés.
Le béryllium, substance industrielle soupçonnée d’être cancérogène, se caractérise par sa légèreté, sa résistance élevée à la traction et sa résistance à la corrosion.
Le tableau 10.13 résume les propriétés du béryllium et de ses composés.
|
Masse atomique relative |
Densité |
Point de fusion/ d�ébullition (°C) |
Solubilité |
Description |
|
|
Béryllium (Be) |
9,01 (moyenne) |
1,85 |
1 298±5/2 970 |
— |
Métal gris argent |
|
Chlorure de béryllium1 |
79,9 |
1,90 |
405/520 |
Très soluble dans l�eau; soluble dans l�alcool éthylique, le benzène, l�éther éthylique et le sulfure de carbone |
Cristaux déliquescents blancs ou jaune pâle |
|
Fluorure de béryllium2 |
47,02 |
1,99 |
Sublimation à 800 |
Assez soluble dans l�eau; peu soluble dans l�alcool éthylique |
Solide hygroscopique |
|
Nitrate de béryllium3 |
187,08 |
1,56 |
60/142 |
Soluble dans l�eau et l�alcool éthylique |
Cristaux déliquescents blancs ou jaune très pâle |
|
Nitrure de béryllium4 |
55,06 |
— |
2 200±100/— |
— |
Cristaux durs, réfractaires, de couleur blanche |
|
Oxyde de béryllium |
25 |
3,02 |
2 530±30/— |
Soluble dans les acides et les bases; insoluble dans l�eau |
Poudre amorphe blanche |
|
Sulfate de béryllium |
177,2 |
1,71 |
100/— |
Soluble dans l�eau; insoluble dans l�alcool éthylique |
Cristaux incolores |
1 Le chlorure de béryllium est fabriqué en faisant passer du chlore sur un mélange d�oxyde de béryllium et de carbone. 2 Le fluorure de béryllium est obtenu par décomposition à 900-950 °C du fluorure double d�ammonium et du béryllium. Il est surtout employé pour la production du béryllium métallique par réduction par le magnésium. 3 Le nitrate de béryllium est obtenu par l�action d�acide nitrique sur de l�oxyde de béryllium. On l�emploie comme réactif chimique et comme durcisseur des récipients de gaz. 4 Le nitrure de béryllium est obtenu par chauffage de poudre de béryllium sous atmosphère d�azote exempte d�oxygène, à 700-1 400 °C. On l�emploie dans les réactions atomiques, y compris dans la production de l�isotope radioactif du carbone, le carbone 14. 5 Le sulfate de béryllium hydraté est obtenu par traitement du minerai fritté avec de l�acide sulfurique concentré. On l�utilise dans la production de béryllium métallique par le procédé au sulfate.
Le béryl (3BeO·Al2O3·6SiO2) est la principale source commerciale de béryllium; c’est le plus abondant des minerais contenant des concentrations élevées d’oxyde de béryllium (10 à 13%). Les principales sources de béryl se trouvent en Argentine, au Brésil, en Inde, au Zimbabwe et en Afrique du Sud. Aux Etats-Unis, le béryl est extrait dans le Colorado, le Dakota du Sud, au Nouveau-Mexique et dans l’Utah. La bertrandite, un minerai de qualité inférieure (0,1 à 3%) contenant du béryllium soluble dans l’acide, est désormais extrait et traité dans l’Utah.
Les deux principales méthodes d’extraction du béryllium du minerai sont le procédé au sulfate et le procédé au fluorure.
Dans le procédé au sulfate, le béryl broyé est fondu dans un four à arc chauffé à 1 650 °C, puis versé dans un courant d’eau à grande vitesse pour être fritté. Après traitement thermique, la fritte est broyée dans un broyeur à boulets et mélangée à de l’acide sulfurique concentré pour former des boues qui sont envoyées à travers une buse dans un moulin rotatif à sulfatation et à chauffage direct. Le béryllium, qui se trouve alors sous forme hydrosoluble, est lessivé à partir de la boue; on ajoute de l’hydroxyde d’ammonium au liquide de lixiviation qui est ensuite versé dans un cristallisoir où l’alun ammonié est séparé en cristaux. On ajoute des chélateurs au liquide pour maintenir en solution le fer et le nickel, puis de l’hydroxyde de sodium; le béryllate de sodium ainsi formé est hydrolysé pour précipiter l’hydroxyde de béryllium. Ce dernier produit peut être transformé en fluorure de béryllium pour être réduit en béryllium métallique par le magnésium ou en chlorure de béryllium en vue d’une réduction électrolytique.
Dans le procédé au fluorure (voir figure 10.11), un mélange comprimé de minerai broyé, de silicofluorure de sodium et de soude est fritté dans un four rotatif. Le produit fritté est concassé, broyé et lessivé. On ajoute de l’hydroxyde de sodium à la solution de fluorure de béryllium ainsi obtenue et le précipité d’hydroxyde de béryllium est filtré sur un filtre rotatif. Le béryllium métallique est obtenu, de la même façon que dans le procédé précédent, par réduction par le magnésium du fluorure de béryllium ou par électrolyse du chlorure de béryllium.
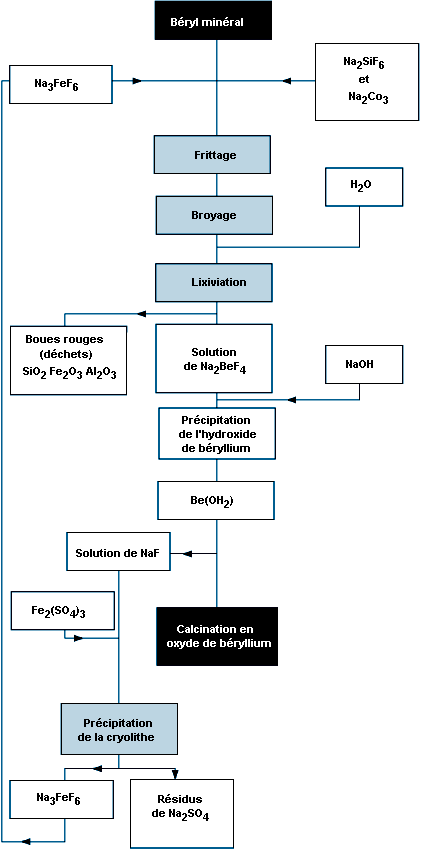
Le béryllium entre dans la fabrication d’alliages avec un grand nombre de métaux dont l’acier, le nickel, le magnésium, le zinc et l’aluminium, l’alliage le plus utilisé étant le cuprobéryllium — appelé à juste titre «un bronze» — qui possède une grande résistance à la traction et la capacité de durcir après traitement thermique. Les bronzes au béryllium servent à fabriquer des outils antiétincelants, des contacts et rupteurs électriques, des spiraux de montre, des diaphragmes, des cames, des paliers et des coussinets.
Ce métal est surtout utilisé comme ralentisseur des neutrons thermiques dans les réacteurs nucléaires et comme réflecteur pour réduire la fuite des neutrons du cœur des réacteurs. On utilise souvent un mélange d’uranium et de béryllium comme source de neutrons. Conditionné en feuille, le béryllium sert à fabriquer des fenêtres dans les tubes à rayons X. Sa légèreté, son module d’élasticité élevé et sa grande stabilité thermique en font un matériau de choix pour l’industrie aéronautique et aérospatiale.
L’oxyde de béryllium est obtenu par chauffage de nitrate ou d’hydroxyde de béryllium. On l’utilise dans la fabrication des céramiques, des produits réfractaires et d’autres composés du béryllium. Il entrait également dans la fabrication des composés phosphorés des lampes à fluorescence jusqu’au moment où l’on a renoncé à l’utiliser en raison de la fréquence des cas de bérylliose industrielle (en 1949 aux Etats-Unis).
Les procédés mettant en œuvre du béryllium présentent des risques d’incendie et des risques pour la santé. La poudre fine de béryllium peut s’enflammer, le degré de combustibilité dépendant de la taille des particules. Des incendies se sont produits dans des unités de filtration de la poussière et pendant le soudage de gaines de ventilation dans lesquelles du béryllium finement divisé était présent.
Le béryllium et ses composés sont des substances hautement toxiques. Le béryllium peut affecter tous les organes, quoique sa principale cible soit le poumon. Le béryllium provoque une maladie systémique par inhalation et peut diffuser à l’ensemble de l’organisme après avoir été absorbé par les poumons. Son absorption digestive est faible. Le béryllium peut entraîner une irritation cutanée et son introduction traumatique dans les tissus sous-cutanés peut induire une irritation locale et la formation de granulomes.
La maladie a été associée à toutes les formes de béryllium, à l’exception du minerai, le béryl. Le béryllium pénètre par inhalation et, dans la maladie aiguë, il exerce un effet toxique direct sur la muqueuse naso-pharyngée et sur celle de l’ensemble de l’arbre trachéo-bronchique, provoquant la formation d’un œdème et une inflammation. Au niveau du poumon, il induit une pneumopathie chimique aiguë. La principale manifestation toxique du béryllium est actuellement la bérylliose chronique. Le plus important mécanisme de cette affection chronique fait intervenir une hypersensibilité à retardement, propre au béryllium. La pénétration systémique du béryllium par les poumons entraîne une prolifération de lymphocytes CD4 spécifiques, le béryllium se comportant comme un antigène spécifique, seul ou en tant qu’haptène, par un processus faisant intervenir les récepteurs de l’interleukine-2 (IL-2). La sensibilité individuelle au béryllium peut ainsi s’expliquer par la réponse individuelle des lymphocytes CD4. La libération de lymphokines par les lymphocytes activés peut alors induire la formation de granulomes et le recrutement de macrophages. Le béryllium peut être emmené dans des sites extrapulmonaires où il provoque la formation de granulomes. Le béryllium est libéré lentement par les différents sites et est excrété par les reins; cette libération peut durer de vingt à trente ans. La chronicité et le temps de latence de la maladie peuvent s’expliquer par la lenteur du métabolisme et par un phénomène de relargage. Les mécanismes immunitaires impliqués dans la pathogenèse de la bérylliose permettent également de s’appuyer sur des critères précis pour le diagnostic (voir ci-après).
La principale anomalie anatomopathologique observée dans la bérylliose est la formation de granulomes non caséeux dans les poumons, les ganglions lymphatiques et d’autres parties du corps. Les études histopathologiques des poumons de patients atteints de bérylliose aiguë ont mis en évidence une bronchite aiguë ou subaiguë non spécifique et une pneumopathie. La bérylliose chronique, de son côté, se caractérise par divers degrés d’infiltration lymphocytaire de l’interstitium pulmonaire et la formation de granulomes non caséeux (voir figure 10.12).
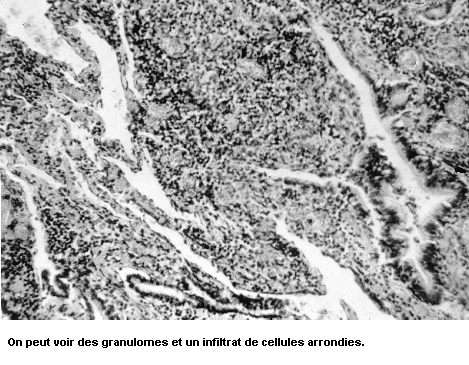
De nombreux granulomes se situent dans les zones péribronchiolaires. De plus, il est possible d’y trouver des histiocytes, des plasmocytes et des cellules géantes contenant des inclusions calcifiées. Si les lésions se limitent à la seule formation de granulomes, le pronostic à long terme est meilleur. L’aspect histologique des poumons dans la bérylliose chronique est indiscernable de celui de la sarcoïdose. On note également la présence de granulomes non caséeux dans les ganglions lymphatiques, le foie, la rate, les muscles et la peau.
Les sels acides de béryllium induisent une dermatose de contact allergique. Ces lésions peuvent être érythémateuses, papuleuses ou papulo-vésiculeuses; elles sont fréquemment prurigineuses et se localisent aux zones exposées du corps. On observe généralement un intervalle de deux semaines entre l’exposition initiale et l’apparition de la dermatose, sauf dans le cas d’une exposition particulièrement forte qui peut provoquer une réaction irritative immédiate. On estime que cet intervalle correspond au temps nécessaire au développement de l’état d’hypersensibilité.
L’implantation accidentelle de béryllium métallique ou de cristaux d’un composé de béryllium soluble dans une excoriation, une gerçure ou sous l’ongle peut provoquer une induration avec suppuration centrale. Des granulomes peuvent également se former à ces endroits.
Une conjonctivite ou une dermatose peuvent se développer, seules ou associées. En cas de conjonctivite, l’œdème périorbitaire peut être important.
La rhino-pharyngite béryllienne se caractérise par une tuméfaction et une hyperémie des muqueuses, des zones hémorragiques, des fissures et des ulcérations. On a signalé des perforations du septum nasal. L’arrêt de l’exposition stoppe le processus inflammatoire en trois à six semaines.
L’atteinte trachéale et bronchique consécutive à l’exposition à des taux plus élevés de béryllium entraîne une toux non productive, des douleurs sous-sternales et une dyspnée modérée. Des ronchi ou des râles sont audibles à l’auscultation et les radiographies pulmonaires peuvent montrer une accentuation de la trame broncho-vasculaire. Le caractère et la vitesse d’apparition de l’affection, ainsi que la sévérité de ces signes et symptômes, dépendent de la nature et de l’importance de l’exposition. La guérison peut survenir en une à quatre semaines si le sujet est soustrait à l’exposition.
La corticothérapie est très utile dans le traitement de la forme aiguë de cette maladie. Aucun nouveau cas de bérylliose aiguë n’a été inscrit dans le registre américain des cas de bérylliose depuis plus de trente ans. Ce registre, instauré par Harriet Hardy en 1952, comprend près de 1 000 cas, dont 212 cas aigus. Presque tous se sont produits dans des fabriques de lampes fluorescentes. Dans 44 cas, la maladie est passée au stade chronique.
La bérylliose chronique est une granulomatose pulmonaire et systémique secondaire à l’inhalation de béryllium. Elle peut rester latente pendant une période de un à trente ans et survient généralement dix à quinze ans après la première exposition. La bérylliose chronique a une évolution variable comportant des poussées aiguës et des phases de rémission de ses manifestations cliniques. Il s’agit cependant d’ordinaire d’une maladie à évolution progressive. On a rapporté quelques cas d’anomalies radiologiques associées à un état clinique stable et à une absence de symptômes significatifs.
La dyspnée d’effort est le symptôme le plus fréquent de la bérylliose chronique. Les autres symptômes sont la toux, la fatigue, l’amaigrissement, les douleurs thoraciques et les arthralgies. L’examen clinique peut être parfaitement normal ou révéler des crépitants dans les deux bases pulmonaires, une lymphadénopathie, des lésions cutanées, une hépato-splénomégalie et un hippocratisme digital. On peut constater des signes d’hypertension artérielle pulmonaire dans les cas sévères évoluant depuis longtemps.
Une lithiase rénale et une hyperuricémie peuvent être observées chez certains patients; on a également rapporté quelques rares cas d’augmentation de volume de la parotide et d’atteinte du système nerveux central. Les manifestations cliniques de la bérylliose chronique sont très proches de celles de la sarcoïdose.
L’aspect radiologique de la bérylliose chronique est aspécifique et proche de celui qu’on peut observer dans la sarcoïdose, la fibrose pulmonaire idiopathique, la tuberculose, les mycoses et les maladies consécutives à l’inhalation de poussières (voir figure 10.13). Au début de l’évolution, les clichés peuvent présenter des opacités granuleuses, nodulaires ou linéaires. Ces anomalies peuvent s’accentuer, régresser ou rester inchangées, avec ou sans fibrose. Une atteinte du lobe supérieur est fréquente. Des adénopathies hilaires, observées chez un tiers environ des patients, sont généralement bilatérales et s’accompagnent d’une réticulation dans les deux champs pulmonaires. L’absence d’anomalies pulmonaires en présence d’adénopathies est un indice, mais non une preuve absolue, qu’il peut s’agir d’une sarcoïdose et non d’une bérylliose chronique. Des adénopathies hilaires unilatérales sont possibles, mais très rares.
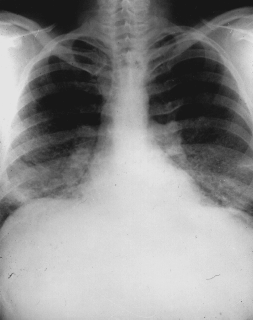
Les radiographies sont sans corrélation nette avec l’état clinique et ne reflètent pas d’aspects qualitatifs ou quantitatifs particuliers de l’exposition responsable.
Les données du registre américain des cas de bérylliose indiquent qu’il est possible de rencontrer trois types d’anomalies dans la bérylliose chronique. Sur 41 patients étudiés pendant vingt-trois ans en moyenne après l’exposition initiale au béryllium, 20% présentaient un trouble restrictif, 36% un trouble interstitiel (volumes et débits pulmonaires normaux, avec diminution de la capacité de diffusion du monoxyde de carbone) et 39% un trouble obstructif; 5% étaient normaux. Le type obstructif, observé chez les fumeurs comme chez les non-fumeurs, était associé à des granulomes péribronchiques. L’étude a montré que le type d’anomalie influe sur le pronostic. Les patients présentant un trouble interstitiel ont eu l’évolution la plus favorable, avec la détérioration la moins importante sur une période de cinq ans, tandis que les patients atteints de troubles obstructifs ou restrictifs ont présenté une aggravation de leurs troubles malgré la corticothérapie.
Les études de la fonction pulmonaire réalisées chez des ouvriers asymptomatiques travaillant à l’extraction du béryllium ont montré la présence d’une petite hypoxie artérielle. Ce phénomène s’observe généralement au cours des dix premières années d’exposition. Chez des travailleurs exposés au béryllium pendant vingt ans ou plus, on a noté une diminution de la capacité vitale expiratoire forcée (CVF) et du volume expiratoire maximal seconde (VEMS). Ces constatations suggèrent que la petite hypoxie initiale pourrait être due à l’alvéolite précoce et, qu’à la longue, si l’exposition persiste, la diminution du VEMS et de la CVF pourraient être un signe de fibrose et de formation de granulomes.
Des anomalies biologiques non spécifiques ont été mentionnées dans la bérylliose chronique: augmentation de la vitesse de sédimentation, polyglobulie, élévation des gammaglobulines, hyperuricémie et hypercalcémie.
Le test cutané de Kveim est négatif dans la bérylliose, alors qu’il est positif dans la sarcoïdose. Le taux de l’enzyme de conversion de l’angiotensine est habituellement normal dans la bérylliose, mais il peut être augmenté chez 60% ou plus des patients atteints de sarcoïdose évolutive.
Pendant de nombreuses années, le diagnostic de la bérylliose chronique a reposé sur les critères énoncés à partir du registre des cas de bérylliose, à savoir:
Il fallait répondre à quatre de ces six critères, dont obligatoirement le premier ou le sixième. Depuis les années quatre-vingt, les progrès réalisés dans le domaine de l’immunologie ont permis de poser le diagnostic de bérylliose sans nécessiter de biopsies tissulaires pour examen histologique ou recherche de béryllium. La transformation des lymphocytes sanguins en réponse à l’exposition au béryllium (comme dans le test de transformation lymphoblastique, TTL) ou des lymphocytes du liquide de lavage broncho-alvéolaire (LBA) a été proposée par Newman et coll. (1989) comme test diagnostique de la bérylliose chez les sujets exposés. Leurs données indiquent que la positivité d’un TTL sanguin est évocatrice d’une sensibilisation. Cependant, des données récentes montrent que la corrélation entre le TTL sanguin et la maladie respiratoire n’est pas nette. La corrélation entre la transformation des lymphocytes du LBA et les anomalies fonctionnelles pulmonaires est beaucoup plus claire, mais ce n’est pas le cas en ce qui concerne les anomalies concomitantes du TTL sanguin. Pour porter le diagnostic de bérylliose, il faut donc déceler à la fois des anomalies cliniques, des anomalies radiologiques et des anomalies fonctionnelles pulmonaires, ainsi qu’un TTL positif sur LBA. Un TTL sanguin positif n’est pas pathognomonique en soi. La technique de détection de la présence de béryllium par microsonde dans de petits échantillons tissulaires constitue une innovation récente susceptible de contribuer au diagnostic de la maladie sur de petits échantillons tissulaires obtenus par biopsie pulmonaire transbronchique.
La sarcoïdose est la maladie qui ressemble le plus à la bérylliose, ce qui peut rendre le diagnostic différentiel difficile. Jusqu’ici, on n’a pas observé de kystes osseux ou d’atteintes oculaires ou amygdaliennes dans la bérylliose. Le test de Kveim est également négatif dans le cas de la bérylliose. Il n’est pas recommandé d’effectuer des tests cutanés pour mettre en évidence une sensibilisation au béryllium, puisque le test est sensibilisant, qu’il peut éventuellement provoquer des réactions systémiques chez les personnes sensibilisées et qu’il ne permet pas de savoir avec certitude si la maladie en question est liée au béryllium.
Les progrès réalisés dans les techniques d’établissement d’un diagnostic différentiel fondées sur l’analyse des réactions immunitaires devraient permettre d’établir plus facilement la distinction entre la bérylliose et la sarcoïdoise.
Le pronostic de la bérylliose chronique a évolué favorablement au fil des ans; on pense que l’allongement du délai d’apparition observé chez les travailleurs manipulant du béryllium pourrait venir d’une réduction de l’exposition ou d’une charge corporelle moindre en béryllium, avec pour résultat une évolution moins grave. Sur le plan clinique, on a constaté que la corticothérapie à doses adéquates, prescrite dès l’apparition d’une incapacité mesurable, administrée pendant des périodes suffisantes, améliore l’état clinique de nombreux patients et permet même à certains d’entre eux de reprendre un travail actif. La preuve absolue d’une guérison de l’intoxication chronique par le béryllium grâce à la corticothérapie n’a pas encore été établie.
Chez l’animal, l’administration expérimentale de béryllium est cancérogène et induit un sarcome ostéogénique après injection intraveineuse chez le lapin et un cancer pulmonaire après inhalation chez le rat et le singe. Le potentiel cancérogène du béryllium chez l’humain reste une question controversée. Certaines études épidémiologiques ont évoqué une association, en particulier après une bérylliose aiguë, mais cette observation a été mise en doute par d’autres auteurs. Il est possible de conclure que le béryllium est cancérogène chez l’animal et qu’il peut y avoir un lien entre le cancer du poumon et le béryllium chez l’humain, en particulier après une bérylliose aiguë.
Ces mesures doivent viser les risques d’incendie, ainsi que les risques beaucoup plus graves d’intoxication.
Des dispositions doivent être prises pour éliminer les éventuelles sources d’ignition, telles que la formation d’étincelles ou d’arcs électriques, le frottement, etc., à proximité de la poudre de béryllium finement divisée. Les récipients ayant contenu cette poudre devraient être vidés et nettoyés avant toute opération de soudage à l’acétylène ou à l’arc. La poudre de béryllium ultrafine, exempte d’oxyde et qui a été préparée sous atmosphère de gaz inerte, peut s’enflammer spontanément au contact de l’air.
Il convient d’utiliser une poudre sèche appropriée — jamais d’eau — pour éteindre un incendie en présence de béryllium. Les sapeurs-pompiers devraient porter un équipement de protection complet, y compris un appareil de protection respiratoire; ils devraient ensuite prendre un bain et faire laver leur linge séparément.
Les opérations impliquant la manipulation de béryllium doivent se dérouler de manière parfaitement contrôlée afin de protéger les travailleurs et la population. Le principal risque prend la forme d’une contamination atmosphérique; par conséquent, les installations et les opérations devraient être conçues de manière à générer aussi peu de poussières et de fumées que possible. Les procédés humides sont préférables aux procédés secs et les composants des préparations de béryllium devraient être mis en œuvre en suspensions aqueuses plutôt qu’en poudres sèches. Chaque installation devrait être composée, autant que possible, d’unités autonomes closes. La concentration admissible de béryllium dans l’air est si faible qu’un confinement peut s’imposer, même avec les procédés humides, sinon les éclaboussures et les divers liquides peuvent sécher et les poussières passer dans l’atmosphère.
Les opérations susceptibles de produire des poussières devraient s’effectuer dans des zones présentant le confinement optimal compatible avec les nécessités du travail. Certaines opérations sont exécutées dans des boîtes à gants, mais la plupart le sont dans des endroits clos munis d’un dispositif d’évacuation semblable à celui des hottes recueillant les fumées de substances chimiques. Les opérations d’usinage devraient s’effectuer sous aspiration localisée à grande vitesse et faible volume, ou en enceintes closes munies d’une hotte d’aspiration.
Le contrôle de l’efficacité de ces diverses mesures exige d’effectuer des prélèvements d’ambiance pour déterminer l’exposition quotidienne moyenne des travailleurs aux particules de béryllium respirables. La zone de travail devrait être nettoyée régulièrement au moyen d’un aspirateur efficace ou d’un balai-éponge humide. Les opérations mettant en œuvre du béryllium devraient se dérouler à l’écart dans des locaux séparés.
Un équipement de protection individuelle devrait être fourni aux travailleurs exposés. S’ils sont engagés à temps complet dans des processus comportant une manipulation de composés de béryllium ou dans des processus en rapport avec l’extraction du métal à partir du minerai, des dispositions devraient être prises pour qu’ils puissent se changer complètement et ne pas rentrer chez eux avec leurs vêtements de travail. Des mesures devraient aussi être prises pour que ces vêtements puissent être lavés sans danger et des combinaisons protectrices devraient être fournies aux employés des laveries. Le blanchissage à domicile devrait être proscrit; des cas d’intoxication par le béryllium imputés aux vêtements contaminés ramenés à domicile ou portés chez eux par les travailleurs ont en effet été constatés.
La limite d’exposition de 2 µg/m3 proposée en 1949 par un comité opérant sous le patronage de la Commission américaine de l’énergie atomique (U.S. Atomic Energy Commission) est appliquée dans la plupart des cas. Les interprétations actuelles tolèrent généralement des excursions jusqu’à une valeur plafond de 5 µg/m3, pour autant que la valeur moyenne d’exposition pondérée dans le temps (Time-Weighted Average (TWA)) ne soit pas dépassée. On admet en outre des pointes de concentration supérieures à cette valeur à condition qu’elles n’excèdent pas 25 µg/m3 pendant trente minutes au maximum. De telles concentrations peuvent effectivement être atteintes dans le cadre des activités industrielles et rien ne prouve qu’elles ont un effet néfaste sur la santé des ouvriers travaillant dans un environnement convenablement contrôlé. En raison d’un lien possible entre le béryllium et le cancer du poumon, on a proposé d’abaisser à 1 µg/m3 la limite autorisée, mais aucune mesure officielle dans ce sens n’a été prise jusqu’ici aux Etats-Unis.
Les travailleurs susceptibles de contracter une bérylliose sont ceux qui sont exposés au béryllium au cours de son extraction ou de ses utilisations ultérieures. On a cependant rapporté quelques cas de contamination indirecte due à la présence d’une usine d’extraction distante de 1 ou 2 km.
Dans plusieurs pays, les travailleurs exposés au béryllium et à ses composés doivent subir un examen médical avant d’être embauchés, puis des examens périodiques par la suite. Le bilan recommandé comprend un questionnaire annuel sur la fonction respiratoire, une radiographie pulmonaire et des épreuves fonctionnelles respiratoires. Grâce aux progrès réalisés dans le domaine de l’immunologie, le TTL pourrait également devenir courant, bien que l’on n’ait pas encore de preuves suffisantes de son utilité pour recommander son emploi systématique. En cas de diagnostic ferme, il n’est pas prudent de permettre au travailleur concerné de rester exposé au béryllium, même si la concentration de béryllium dans l’air reste dans les limites admissibles à l’endroit où il travaille.
La principale mesure thérapeutique consiste à écarter toute nouvelle exposition au béryllium. La corticothérapie est le principal mode de traitement de la bérylliose chronique. Les corticoïdes semblent en effet ralentir l’évolution de la maladie, sans toutefois la guérir.
La corticothérapie devrait débuter par l’administration quotidienne d’une dose relativement forte de Prednisone (de 0,5 à 1 mg/kg ou plus) et se poursuivre jusqu’à ce que l’état clinique ou les résultats des épreuves fonctionnelles respiratoires s’améliorent ou se stabilisent, ce qui prend généralement de quatre à six semaines. On recommande une réduction progressive des doses et, pour finir, l’administration du médicament un jour sur deux. La corticothérapie est généralement un traitement à vie.
D’autres mesures d’appoint telles que l’oxygénothérapie, les diurétiques, les digitaliques et les antibiotiques (en cas d’infection) sont indiquées selon l’état clinique du patient. La vaccination contre la grippe et le pneumocoque devrait également être envisagée, comme chez tous les patients porteurs d’une maladie respiratoire chronique.
Le terme pneumoconiose, du grec pneuma (air, souffle) et konios (poussière), a été forgé en Allemagne par Zenker en 1867 pour désigner les altérations pulmonaires provoquées par l’accumulation de poussières inhalées. La nécessité d’une distinction entre les effets de différents types de poussières s’est fait progressivement sentir. Il est ainsi devenu nécessaire d’établir une distinction entre les poussières minérales ou végétales et leur composante microbiologique. En conséquence, la troisième Conférence internationale d’experts en pneumoconioses, organisée par le BIT à Sydney, en 1950, a adopté la définition suivante: «La pneumoconiose est une maladie pulmonaire pouvant être diagnostiquée, due à l’inhalation de poussières, le terme ‘poussières’ s’appliquant à des particules à l’état solide, à l’exclusion des organismes vivants».
Le terme maladie qui apparaît dans cette définition semble impliquer une altération de l’état de santé, ce qui n’est pas forcément le cas avec les pneumoconioses ne comportant pas de lésions fibreuses ou cicatricielles des poumons. En règle générale, la réaction du tissu pulmonaire à la présence de poussières varie avec la nature de celles-ci. Les poussières non fibrogènes induisent une réaction tissulaire des poumons caractérisée par une réaction fibreuse minime et une absence d’anomalies fonctionnelles respiratoires. Ces poussières — citons à titre d’exemple les poussières finement broyées de kaolinite, de dioxyde de titane, d’oxyde stanneux, de sulfate de baryum ou d’oxyde de fer — sont souvent considérées comme biologiquement inertes.
Les poussières fibrogènes comme la silice et l’amiante induisent une réaction fibreuse plus marquée qui aboutit à la formation de cicatrices au sein du tissu pulmonaire; dans ce cas, la maladie est patente. La division des poussières en fibrogènes et non fibrogènes n’a rien d’absolu: de nombreux minéraux, en effet, et notamment les silicates, ont un potentiel fibrogène pulmonaire intermédiaire. Elle s’est néanmoins révélée utile à des fins cliniques et se reflète dans la classification des pneumoconioses.
Une nouvelle définition des pneumoconioses a été adoptée par le groupe de travail réuni par le BIT dans le cadre de la quatrième Conférence internationale sur les pneumoconioses, tenue à Bucarest en 1971: «La pneumoconiose correspond à l’accumulation de poussières dans les poumons et à la réaction des tissus à la présence de ces poussières. Dans le cadre de cette définition, on entend par ‘poussière’ un aérosol composé de particules solides inertes».
Pour éviter toute erreur d’interprétation, le terme non néoplasique est parfois ajouté à l’expression «réaction des tissus».
A cette conférence, le groupe de travail a adopté une déclaration détaillée dont l’essentiel est résumé ci-après:
Définition de la pneumoconiose
Dans le passé, en 1950, une définition de la pneumoconiose a été établie lors de la troisième Conférence internationale d’experts sur les pneumoconioses et a été utilisée jusqu’ici.
Depuis 1950, le développement de nouvelles technologies a aggravé les risques professionnels, en particulier ceux liés à l’inhalation de polluants en suspension dans l’air.
Le développement des connaissances dans le domaine de la médecine du travail a permis l’identification de nouvelles maladies respiratoires d’origine professionnelle, mais il a également montré la nécessité d’un réexamen de la définition des pneumoconioses donnée en 1950.
Le BIT a donc constitué un groupe de travail dans le cadre de la quatrième Conférence internationale sur les pneumoconioses afin d’étudier la question de la définition des pneumoconioses.
Le groupe de travail a examiné les propositions soumises par ses membres avant d’adopter une nouvelle définition de la pneumoconiose à laquelle il a joint un certain nombre de commentaires.
Ces dernières années, pour des raisons socio-économiques, plusieurs pays ont inclus dans les pneumoconioses des maladies qui n’en sont manifestement pas, mais qui sont cependant des maladies respiratoires professionnelles. Par «maladie», on entend, pour des raisons préventives, les toutes premières manifestations qui ne sont pas forcément invalidantes ou menaçantes pour le pronostic vital.
Le groupe de travail a donc entrepris de redéfinir la pneumoconiose (voir ci-dessus).
Sur le plan anatomopathologique, les pneumoconioses peuvent être divisées en formes collagènes et non collagènes.
Une pneumoconiose non collagène est due à une poussière non fibrogène et présente les caractéristiques suivantes:
Comme exemples de pneumoconioses non collagènes, on peut citer celles provoquées par les poussières d�oxyde d�étain (stannose) et de sulfate de baryum (barytose).
Les pneumoconioses collagènes se caractérisent par:
Ces pneumoconioses collagènes peuvent être provoquées par des poussières fibrogènes ou par la réponse d’un tissu lésé à une poussière non fibrogène.
Comme exemples de pneumoconioses collagènes dues à des poussières fibrogènes, on peut citer la silicose et l’asbestose, tandis que la pneumoconiose des houilleurs ou fibrose massive progressive (FMP) correspond à la réponse d’un tissu altéré à une poussière relativement non fibrogène.
En pratique, la distinction entre pneumoconioses collagènes et non collagènes est difficile à établir. L’exposition continue à la même poussière peut entraîner le passage d’une forme non collagène à une forme collagène. De plus, l’exposition à une seule poussière est désormais moins courante et les expositions à des poussières mixtes, de potentiels fibrogènes différents, peuvent induire des pneumoconioses de formes diverses, collagènes ou non.
Il existe également des maladies respiratoires chroniques professionnelles qui, bien qu’elles apparaissent à la suite de l’inhalation de poussières, ne sont pas des pneumoconioses du fait que les particules ne sont pas censées s’accumuler dans les poumons.
La byssinose, la bérylliose, le poumon du fermier et les maladies apparentées sont des exemples de maladies respiratoires chroniques professionnelles, potentiellement invalidantes. Elles ont pour dénominateur commun la sensibilisation du tissu pulmonaire ou bronchique par le composant étiologique de la poussière, de sorte que si le tissu pulmonaire réagit, l’inflammation a tendance à être de type granulomateux, alors que si c’est le tissu bronchique qui réagit, une bronchoconstriction est possible.
L’exposition à des substances nocives inhalées dans certaines industries s’associe à un risque accru de mortalité par cancer de l’appareil respiratoire. Les substances radioactives, l’amiante et les chromates sont des exemples de ces substances.
Adoptée à la quatrième Conférence internationale du BIT sur les pneumoconioses, Bucarest, 1971.
En dépit de tous les efforts nationaux et internationaux consacrés à leur prévention, les pneumoconioses sont toujours présentes dans les pays industriels et les pays en développement où elles entraînent l’incapacité de travail de nombreux travailleurs. C’est la raison pour laquelle le Bureau international du Travail (BIT), l’Organisation mondiale de la santé (OMS) et de nombreuses institutions nationales de sécurité et de santé au travail continuent à les combattre et à proposer des programmes de prévention à long terme. Le BIT, l’OMS et, aux Etats-Unis, l’Institut national de la sécurité et de la santé au travail (National Institute for Occupational Safety and Health (NIOSH)) s’emploient officiellement à lutter ensemble contre la silicose. Un aspect de cette collaboration vise une surveillance médicale comportant notamment l’examen de radiographies pulmonaires pour faciliter le diagnostic de cette forme de pneumoconiose. C’est dans ce but que le BIT, en collaboration avec de nombreux experts, a mis au point et tient régulièrement à jour une classification des aspects radiologiques des pneumoconioses qui permet d’enregistrer systématiquement les anomalies radiologiques thoraciques dues à l’inhalation de poussières. Il s’agit de classifier les images de radiographies du thorax prises en incidence postéro-antérieure (PA).
Cette classification a pour objet de codifier les anomalies radiographiques des pneumoconioses de façon simple et reproductible. Elle ne définit pas d’entités nosologiques et ne prend pas non plus en considération l’incapacité de travail. La classification n’implique aucune définition légale des pneumoconioses à des fins de réparation, ni une valeur seuil à partir de laquelle une réparation serait due. Il s’est néanmoins avéré qu’elle est utilisée de manière plus étendue que prévu. Elle est désormais largement utilisée au niveau international pour la recherche épidémiologique, pour la surveillance de la santé des travailleurs dans différentes branches, ainsi qu’à des fins cliniques. Son utilisation a également permis d’améliorer la comparabilité internationale des statistiques de pneumoconioses. Enfin, elle sert à décrire et à enregistrer, de manière systématique, une partie des informations nécessaires à une éventuelle réparation.
La principale condition d’utilisation optimale de ce système de classification, du point de vue scientifique et éthique, est toujours de lire les clichés en les comparant systématiquement aux 22 clichés types de la Classification internationale du BIT. Si le lecteur tente de classifier un cliché sans se référer à l’un de ces clichés de référence, il ne pourra pas être fait mention d’une lecture conforme à la Classification internationale. Le risque de s’écarter de la classification par une lecture par excès ou par défaut est si important qu’une telle lecture ne devrait pas être utilisée à des fins de recherche épidémiologique ou en vue d’une comparaison internationale des statistiques de pneumoconioses.
Une première classification avait été adoptée pour la silicose par la première Conférence internationale d’experts en pneumoconioses, tenue à Johannesburg en 1930. Elle associait des critères radiologiques, cliniques et physiologiques (fonction respiratoire). En 1958, une nouvelle classification, basée sur les anomalies radiologiques, a été établie (Classification de Genève, 1958). Elle a été révisée par la suite à plusieurs reprises, pour la dernière fois en 1980, toujours dans le but de fournir une version améliorée permettant une large utilisation à des fins cliniques et épidémiologiques. Chaque nouvelle version de la Classification du BIT a apporté des modifications basées sur l’expérience internationale acquise avec les classifications précédentes.
Pour permettre une utilisation claire de la classification, le BIT a publié en 1970 la Classification internationale des radiographies de pneumoconioses, 1968 dans la série Sécurité, Hygiène et Médecine du Travail (no 22). Cette publication a été révisée en 1972 sous le titre Classification internationale BIT U/C des radiographies de pneumoconioses, 1971, puis une nouvelle fois en 1980 sous le titre Instructions pour l’utilisation de la Classification internationale du BIT des radiographies de pneumoconioses, édition révisée en 1986. La description des clichés types est fournie au tableau 10.14.
|
|
Petites opacités |
Epaississements pleuraux |
||||||||||
|
|
Paroi |
|||||||||||
|
thoracique |
||||||||||||
|
Cliché type de 1980 montrant |
Qualité technique |
Densité |
Forme et taille |
Etendue |
Grandes opacités |
Circonscrit (plaques) |
Diffus |
Diaphragme |
Comblement de l�angle costo-diaphragmatique |
Calcifications pleurales |
Symboles |
Commentaires |
|
0/0 |
1 |
0/0 |
— |
— |
Non |
Non |
Non |
Non |
Non |
Non |
Non |
Le dessin vasculaire est bien illustré. |
|
0/0 |
1 |
0/0 |
— |
— |
Non |
Non |
Non |
Non |
Non |
Non |
Non |
Montre également bien le dessin vasculaire, moins clairement que dans l�exemple 1. |
|
1/1; p/p |
1 |
1/1 |
p/p |
R L |
A |
Non |
Non |
Non |
Non |
Non |
rp. |
Pneumoconiose rhumatoïde dans la zone inférieure gauche. Les petites opacités sont présentes dans toutes les zones, mais la densité dans la zone supérieure droite est typique de ce qui est classifiable en catégorie bien que certains puissent l�estimer légèrement plus dense. |
|
2/2; p/p |
2 |
2/2 |
p/p |
R L |
— |
Non |
Non |
Non |
Non |
Non |
pi; tb. |
Insuffisance de qualité: la radiographie est trop claire. |
|
3/3; p/p |
1 |
3/3 |
p/p |
R L |
Non |
Non |
Non |
Non |
Oui |
Non |
ax. |
— |
|
1/1; q/q |
1 |
1/1 |
q/q |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
Non |
La densité 1/1 est mieux illustrée que la forme et la taille. |
|
2/2; q/q |
1 |
2/2 |
q/q |
R L |
Non |
Non |
Oui |
Non |
Oui |
Non |
Non |
— |
|
3/3; q/q |
2 |
3/3 |
q/q |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
pi. |
Insuffisance de qualité: médiocre définition de la plèvre et des sinus costo- |
|
1/1; r/r |
2 |
1/1 |
r/r |
R L |
Non |
Non |
Non |
Non |
Oui |
Non |
Non |
Insuffisance de qualité: mouvement des sujets. Densité des petites opacités les plus marquées dans le poumon droit. |
|
2/2; r/r |
2 |
2/2 |
r/r |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
Non |
Insuffisance de qualité: radiographie trop claire et contraste trop haut. L�ombre du cœur est légèrement déplacée vers la gauche. |
|
3/3; r/r |
1 |
3/3 |
r/r |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
ax; ih. |
— |
|
1/1; s/t |
2 |
1/1 |
s/t |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
kl. |
Insuffisance de qualité: amputation des bases. Ligne de Kerley dans la zone inférieure droite. |
|
2/2; s/s |
2 |
2/2 |
s/s |
R L |
Non |
Non |
Non |
Non |
Non |
Non |
em. |
Insuffisance de qualité: distension des bases due à la contraction. Emphysème dans les zones supérieures. |
La révision de 1980 a été entreprise par le BIT avec la collaboration de la Commission des Communautés européennes, du NIOSH et du Collège américain de radiologie (American College of Radiology). Le tableau 10.15 en présente un résumé. La Classification de 1980 conserve le principe des classifications antérieures (1968 et 1971).
|
Données |
|
Codes |
Définitions |
|
Qualité technique |
|||
|
|
|
1 |
Bonne. |
|
|
|
2 |
Acceptable, sans défaut technique susceptible de gêner la classification de la radiographie dans le domaine des pneumoconioses. |
|
|
|
3 |
Avec quelques défauts techniques, mais encore acceptable en vue de la classification. |
|
|
|
4 |
Inacceptable. |
|
Anomalies parenchymateuses |
|||
|
Petites opacités |
Densité |
— |
La catégorie de densité est basée sur l�évaluation de la concentration des opacités par comparaison avec le cliché type. |
|
|
|
0/� 0/0 0/1 |
Catégorie 0 — petites opacités absentes ou moins nombreuses que la limite inférieure de la catégorie 1. |
|
|
Situation |
RU RM RL |
On notera les régions où sont observées les opacités. Le champ pulmonaire droit (R) et gauche (L) sont tous les deux divisés en trois zones: supérieure (U), moyenne (M) et inférieure (L). |
|
|
Taille et forme: |
|
|
|
|
arrondies |
p/p q/q r/r |
Les lettres p, q et r concernent la présence de petites opacités arrondies. Trois tailles sont définies par les images des clichés types: |
|
|
irrégulières |
s/s t/t u/u |
Les lettres s, t et u concernent la présence de petites opacités irrégulières. Trois tailles sont définies par les images des clichés types: |
|
|
mixtes |
p/s p/t p/u p/q p/r |
Pour les formes (ou tailles) mixtes des petites opacités, la forme et la taille prédominantes sont notées d�abord. La présence d�un nombre significatif d�une autre forme ou taille est enregistrée après une barre oblique. |
|
Grandes opacités |
|
A B C |
Les catégories sont définies en terme de dimension des opacités. |
|
Anomalies pleurales |
|||
|
Epaississement pleural: |
|
|
|
|
Paroi thoracique |
Type |
— |
Deux types d�épaississement pleural de la paroi thoracique sont définis: circonscrits (plaques) et diffus. Les deux types peuvent être simultanément présents. |
|
|
Siège |
R L |
L�épaississement pleural de la paroi thoracique est noté séparément pour le champ pulmonaire droit (R) et gauche (L). |
|
|
Epaisseur |
a b c |
La mesure du degré d�épaississement pleural sur la paroi thoracique se fait depuis la limite intérieure de la paroi jusqu�à la marge interne de l�opacité dans la zone où la frontière pleuro-parenchymateuse est la plus clairement définie. L�épaisseur maximale est habituellement constatée à la limite interne de l�ombre costale à son point extrême. |
|
|
Vue de face |
Y N |
La présence d�un épaississement pleural vu de face est notée habituellement si elle peut être également vue de profil. Si l�épaississement pleural est seulement vu de face, l�épaisseur ne peut habituellement être mesurée. |
|
|
Etendue |
1 2 3 |
L�étendue de l�épaississement pleural est définie en terme de hauteur maximum de zone pleurale concernée ou comme la somme des longueurs maximales, qu�elle soit vue de profil ou de face. |
|
Diaphragme |
Présence |
Y N |
Une plaque concernant la plèvre diaphragmatique est notée comme présente (Y) ou- absente (N), séparément pour la droite (R) et la gauche (L) de l�image thoracique. |
|
|
Siège |
R L |
— |
|
Oblitération de l�angle costophrénique |
Présence |
Y N |
La présence (Y) ou l�absence (N) de l�oblitération de l�angle costo-phrénique est enregistrée (séparément de l�épaississement en d�autres zones) pour le côté droit (R) et le côté gauche (L) du thorax. La limite inférieure de cette oblitération est définie par un cliché type. |
|
|
Siège |
R L |
Si l�épaississement s�étend en hauteur sur la paroi thoracique, dans ce cas l�oblitération de l�angle costo-phrénique d�une part, et l�épaisseur pleurale d�autre part doivent être enregistrées. |
|
Calcifications pleurales |
Siège |
— |
Le siège et l�étendue de la calcification pleurale sont notés séparément pour les deux poumons et l�étendue est définie en terme de dimension. |
|
|
Paroi thoracique |
R L |
— |
|
|
Diaphragme |
R L |
— |
|
|
Autres |
R L |
�Autres� concernent les calcifications de la plèvre médiastinale ou péricardiaque. |
|
|
Etendue |
1 2 3 |
1 = une zone de plèvre calcifiée dont le plus grand diamètre peut atteindre 20 mm ou un nombre de telles zones dont la somme des plus grands diamètres n�excède pas 20 mm environ. |
|
Symboles |
|||
|
|
|
|
Il est admis que la définition de chacun des symboles peut être précédée d�un mot ou d�une expression appropriés tels que �suspect de�, �altération suggérant��, �opacités évoquant��, etc. |
|
|
|
ax |
Coalescence de petites opacités pneumoconiotiques. |
|
|
|
bu |
Bulles. |
|
|
|
ca |
Cancer du poumon ou de la plèvre. |
|
|
|
cn |
Calcification au sein de petites opacités pneumoconiotiques. |
|
|
|
co |
Anomalies du volume ou de la silhouette cardiaque. |
|
|
|
cp |
Cœur pulmonaire. |
|
|
|
cv |
Image cavitaire. |
|
|
|
di |
Distension marquée des organes intrathoraciques. |
|
|
|
ef |
Epanchement pleural. |
|
|
|
em |
Emphysème marqué. |
|
|
|
es |
Calcification en coquille d�œuf des ganglions lymphatiques hilaires ou médiastinaux. |
|
|
|
Fr |
Fracture de côte(s). |
|
|
|
Hi |
Elargissement des ganglions hilaires ou médiastinaux. |
|
|
|
Ho |
Aspect en �nid d�abeilles�. |
|
|
|
Id |
Diaphragme mal défini. |
|
|
|
Ih |
Silhouette cardiaque mal définie. |
|
|
|
Kl |
Lignes de Kerley. |
|
|
|
Od |
Autres anomalies significatives. |
|
|
|
Pi |
Epaississement pleural dans la scissure interlobaire ou le médiastin. |
|
|
|
Px |
Pneumothorax. |
|
|
|
Rp |
Pneumoconiose rhumatoïde. |
|
|
|
Tb |
Tuberculose. |
|
Commentaires |
|||
|
|
Présence |
Y N |
La classification du cliché doit être assortie de commentaires, surtout si l�on estime qu�une image radiologique, pouvant être attribuée par certains à une pneumoconiose, est en fait imputable à une autre cause; un commentaire est également nécessaire pour les radiographies dont la lecture peut avoir été sensiblement influencée par le niveau de la qualité technique. |
Elle est fondée sur un jeu de 22 clichés types, des instructions et une notice explicative. Aucune donnée visible sur une radiographie pulmonaire n’est pathognomonique d’une exposition aux poussières. Le principe essentiel est qu’il faut classifier tous les aspects compatibles avec ceux définis et représentés sur les clichés types et dans les instructions pour l’utilisation de la Classification internationale. Si le lecteur estime qu’un aspect n’a probablement ou formellement aucun rapport avec la poussière, la radiographie ne doit pas être classifiée, mais faire l’objet d’un commentaire approprié. Les 22 clichés types ont été sélectionnés à la suite d’études faites au niveau international; ils illustrent les images des catégories médianes pour les petites opacités (mm) et fournissent des exemples des catégories A, B et C pour les grandes opacités (diamètre 10 mm). Les anomalies pleurales (épaississement pleural diffus, plaques pleurales et comblement de l’angle costo-phrénique) sont également visibles sur différents clichés.
Les discussions ultérieures, en particulier lors de la septième Conférence internationale sur les pneumoconioses, tenue à Pittsburgh en 1988, ont montré qu’il fallait améliorer certaines parties de la classification, surtout celles concernant les anomalies pleurales. Une réunion du groupe de travail pour la révision de la Classification internationale du BIT des radiographies de pneumoconioses s’est tenue à Genève en novembre 1989. Les experts ont émis l’opinion que la classification abrégée n’était d’aucune utilité et qu’il était possible de la supprimer. En ce qui concerne les anomalies pleurales, le groupe a reconnu que cette classification pouvait désormais être divisée en trois parties: épaississement pleural diffus, plaques pleurales et comblement de l’angle costo-phrénique. L’épaississement pleural diffus peut être divisé en atteinte de la paroi thoracique et en atteinte diaphragmatique. On a identifié ces atteintes d’après six zones — parties supérieure, moyenne et inférieure des poumons droit et gauche. Si un épaississement pleural est limité, il peut être considéré comme une plaque. Toutes les plaques devraient être mesurées en centimètres. Le comblement de l’angle costo-phrénique devrait être consigné systématiquement (qu’il existe ou non). Il est important de noter si l’angle costo-phrénique est visible ou non, en raison de son importance par rapport à l’épaississement pleural diffus. Un symbole devrait être utilisé pour indiquer si les plaques ont été classées ou non. L’aplatissement du diaphragme devrait être signalé par un autre symbole, car il s’agit d’une caractéristique très importante dans l’exposition à l’amiante. La présence de plaques devrait être indiquée dans les cases appropriées en utilisant les symboles «c» (calcifiées) ou «h» (hyalines).
Une description complète de la Classification, avec ses applications et limitations, se trouve dans la publication mentionnée plus haut (BIT, 1986). La révision de cette classification retient en permanence l’attention du BIT; des instructions révisées devraient être publiées d’ici à l’an 2000 pour tenir compte des recommandations du groupe de travail.
Les pneumoconioses sont reconnues depuis longtemps déjà comme des maladies professionnelles. De grands efforts ont été faits dans les domaines de la recherche, de la prévention primaire et du traitement médical. Mais, de l’avis des médecins et des hygiénistes, le problème demeure présent dans les pays industriels comme dans les pays en cours d’industrialisation (Valiante, Richards et Kinsley, 1992; Markowitz, 1992). Etant donné que les trois principaux minerais industriels responsables des pneumoconioses (amiante, charbon et silice) sont fort probablement appelés à conserver une certaine importance économique, on peut s’attendre que le problème continue à se poser avec une certaine intensité dans le monde entier, en particulier parmi la main-d’œuvre souvent délaissée des petites entreprises industrielles et des petites exploitations minières. Les difficultés pratiques de la prévention primaire et la méconnaissance des mécanismes responsables de l’apparition et du développement de la maladie sont des facteurs qui peuvent tous expliquer la persistance du problème.
L’étiopathogenèse des pneumoconioses peut se définir comme l’évaluation et la compréhension de tous les phénomènes survenant au niveau des poumons à la suite de l’inhalation de particules de poussières fibrogènes. L’expression cascade d’événements se retrouve souvent dans la littérature consacrée à ce sujet; elle désigne une série d’événements qui débute avec la première exposition et qui aboutit aux formes pathologiques les plus graves. Si l’on excepte les rares formes de silicose accélérée qui peuvent se développer après quelques mois seulement d’exposition, la plupart des pneumoconioses apparaissent à la suite d’une période d’exposition qui se compte en décennies plutôt qu’en années. C’est particulièrement vrai de nos jours dans les entreprises qui observent les normes modernes de prévention. Le phénomène étiopathogénique doit donc être analysé dans la perspective d’une dynamique à long terme.
Ces vingt dernières années, une foule d’informations ont été recueillies sur les nombreuses et complexes réactions pulmonaires impliquées dans la fibrose pulmonaire interstitielle induite par plusieurs agents, dont les poussières minérales. Ces réactions ont été décrites sur le plan biochimique et cellulaire (Richards, Masek et Brown, 1991). Les médecins, les chercheurs en médecine expérimentale, de même que les cliniciens utilisant le lavage broncho-alvéolaire comme nouvelle technique d’étude pulmonaire, ont tous apporté leur contribution. L’étiopathogenèse est présentée comme une entité extrêmement complexe, mais qui peut néanmoins être fragmentée pour montrer différentes facettes: 1) l’inhalation elle-même de particules de poussières et la constitution et l’importance de la charge pulmonaire résultante (relation exposition-dose); 2) les caractéristiques physico-chimiques des particules fibrogènes; 3) les réactions biochimiques et cellulaires induisant les lésions fondamentales de pneumoconiose; 4) les facteurs déterminants de l’évolution et des complications de la maladie. Cette dernière facette ne doit pas être négligée, car les formes les plus sévères de pneumoconiose sont celles qui conduisent à l’incapacité de travail et à l’invalidité.
Une analyse détaillée de l’étiopathogenèse des pneumoconioses sort du cadre du présent article. Il faudrait faire la distinction entre plusieurs types de poussières et approfondir l’étude de nombreux domaines spécialisés dont certains font encore l’objet de recherches actives. Il est cependant possible de tirer des notions générales intéressantes des connaissances actuelles. Nous les présenterons ici dans le cadre des quatre facettes citées plus haut; la bibliographie permettra au lecteur intéressé de consulter des ouvrages plus spécialisés. Des exemples seront fournis essentiellement pour les trois principales pneumoconioses, qui sont également les mieux documentées: l’asbestose, la pneumoconiose des houilleurs (PH) et la silicose. Les éventuelles conséquences sur la prévention seront abordées.
Les pneumoconioses résultent de l’inhalation de certaines particules de poussières fibrogènes. En physique des aérosols, le terme poussière a une signification bien précise (Hinds, 1982). Il désigne les particules en suspension dans l’air obtenues par division mécanique d’une substance mère à l’état solide. Les particules générées par d’autres procédés ne devraient pas être qualifiées de poussières. Les nuages de poussière observés dans différents environnements industriels (mines, minières et carrières, percement de galeries, sablage, etc.) sont généralement constitués d’un mélange de plusieurs types de poussière. Les particules en suspension dans l’air n’ont pas une taille homogène, mais une distribution granulométrique. La taille et d’autres paramètres physiques (masse volumique, forme et charge superficielle) déterminent le comportement aérodynamique des particules et la probabilité de leur pénétration et de leur accumulation dans les différentes régions de l’appareil respiratoire.
Dans le domaine des pneumoconioses, le secteur le plus intéressant est le compartiment alvéolaire. Les particules en suspension dans l’air suffisamment petites pour atteindre ce compartiment sont appelées particules respirables ou alvéolaires. Toutes les particules atteignant le compartiment alvéolaire ne s’y déposent pas systématiquement, certaines restant présentes dans l’air expiré. Les mécanismes physiques responsables de leur déposition sont maintenant bien connus dans les cas des particules isométriques (Raabe, 1984) et des particules fibreuses (Sébastien, 1991). Les fonctions liant les probabilités de déposition aux paramètres physiques ont été définies. Les particules respirables et les particules déposées dans le compartiment alvéolaire ont des caractéristiques de taille quelque peu différentes. Pour les particules non fibreuses, on se sert d’instruments d’échantillonnage de l’air avec dispositif de sélection par fraction granulométrique et d’instruments à lecture directe pour mesurer la concentration pondérale des particules respirables. Pour les particules fibreuses, l’approche est différente; la technique consiste à recueillir la «poussière totale» sur des filtres et à compter les fibres au microscope optique. Dans ce cas, la sélection granulométrique s’effectue en excluant du comptage les fibres «non respirables» ayant des dimensions sortant des limites préétablies.
Une fois les particules déposées à la surface des alvéoles commence le processus dit de clairance alvéolaire dont les premières phases consistent en un recrutement chimiotactique des macrophages et en une phagocytose. Cette clairance peut prendre plusieurs formes: élimination des macrophages chargés de poussières vers les voies respiratoires ciliées, interaction avec les cellules épithéliales et transport des particules libres à travers les membranes alvéolaires, phagocytose par les macrophages, séquestration dans l’interstitium et transport vers les ganglions lymphatiques (Lauweryns et Baert, 1977), chacune de ces formes de clairance ayant une cinétique particulière. L’activation des différents processus responsables de la rétention des agents contaminants dans les poumons est déclenchée non seulement par la nature de l’exposition, mais aussi par les caractéristiques physico-chimiques des particules déposées.
La notion de processus rétentionnel propre à chaque type de poussière est relativement nouvelle, mais on dispose désormais d’un nombre suffisant d’arguments pour l’intégrer dans les schémas étiopathogéniques. Par exemple, l’un des auteurs du présent article a constaté qu’après une exposition prolongée à l’amiante les fibres s’accumulent dans les poumons si elles sont du type amphibole, mais non si elles sont du type chrysotile (Sébastien, 1991). On a pu montrer par ailleurs que les fibres courtes sont éliminées plus rapidement que les longues. On sait aussi que le quartz présente un certain tropisme lymphatique et qu’il pénètre facilement dans le système lymphatique. On a démontré que la modification des caractères chimiques superficiels des particules de quartz influe sur la clairance alvéolaire (Hemenway et coll., 1994; Dubois et coll., 1988). L’exposition simultanée à plusieurs types de poussières peut influer elle aussi sur la clairance alvéolaire (Davis, Jones et Miller, 1991).
Au cours du processus de clairance alvéolaire, les particules de poussières subissent des modifications chimiques et physiques, telles que l’enrobage avec une substance ferrugineuse, le lessivage de certains composants élémentaires et l’adsorption de certaines molécules biologiques.
Une autre notion récemment dérivée des expériences chez l’animal est celle de la «surcharge pulmonaire» (Mermelstein et coll., 1994). Des rats soumis à une inhalation massive d’un ensemble de poussières insolubles ont réagi de la même façon: inflammation chronique, augmentation du nombre de macrophages chargés de particules, augmentation du nombre de particules dans l’interstitium, épaississement des septa, lipoprotéinose et fibrose. Ces anomalies n’ont pas été imputées à la réactivité de la poussière testée (dioxyde de titane, cendres volcaniques, cendres volantes, coke de pétrole, poly(chlorure de vinyle), toner, noir de carbone et particules d’échappement des moteurs diesel), mais à une exposition pulmonaire excessive. On ignore s’il faut tenir compte de la surcharge pulmonaire dans le cas d’une exposition humaine à des poussières fibrogènes.
Parmi les différents processus de clairance, le passage dans l’interstitium semble jouer un rôle particulièrement important dans la genèse des pneumoconioses. La clairance des particules séquestrées dans l’interstitium est beaucoup moins efficace que celle des particules absorbées par les macrophages dans l’espace alvéolaire et éliminées par les voies respiratoires ciliées (Vincent et Donaldson, 1990). Chez l’humain, on a constaté qu’après une exposition prolongée à un certain nombre de polluants inorganiques en suspension dans l’air la rétention dans les macrophages interstitiels était beaucoup plus importante que dans les macrophages alvéolaires (Sébastien et coll., 1994). On a également suggéré que la fibrose pulmonaire induite par la silice résulte plutôt de la réaction des particules avec les macrophages interstitiels qu’avec ceux des alvéoles (Bowden, Hedgecock et Adamson, 1989). La rétention est responsable de la «dose» qui mesure le contact des particules de poussières avec leur milieu biologique. Pour décrire correctement la dose, il faudrait connaître à chaque instant la quantité de poussières accumulée dans les structures et les cellules pulmonaires, l’état physico-chimique de ces particules (y compris leur état de surface), ainsi que les interactions entre les particules et les cellules et liquides pulmonaires. L’évaluation directe de la dose chez l’humain est de toute évidence impossible, même si l’on disposait de méthodes de mesure des particules dans plusieurs échantillons biologiques d’origine pulmonaire comme les crachats, le liquide de lavage broncho-alvéolaire et les prélèvements biopsiques ou autopsiques (Bignon, Sébastien et Bientz, 1979). Ces méthodes ont été utilisées à un certain nombre de fins: fournir des informations sur les mécanismes de rétention, valider des informations sur l’exposition, étudier le rôle de plusieurs types de poussières dans le développement pathogénique (par exemple, l’exposition à des fibres de type amphibole ou chrysotile dans l’asbestose ou l’exposition au quartz par rapport à l’exposition au charbon dans la PH) et contribuer au diagnostic.
Ces mesures directes n’offrent toutefois qu’un tableau instantané de la rétention au moment de l’échantillonnage et ne permettent pas au chercheur de reconstituer les données relatives à la dose. De nouveaux modèles dosimétriques semblent prometteurs à cet égard (Katsnelson et coll., 1994; Smith, 1991; Vincent et Donaldson, 1990); ils ont été conçus pour évaluer la dose à partir d’informations sur l’exposition en tenant compte de la probabilité de déposition et de la cinétique des différents processus de clairance. On a récemment intégré à ces modèles la notion intéressante de nocivité des polluants (Vincent et Donaldson, 1990); cette notion prend en compte la réactivité spécifique des particules déposées, chacune d’elles étant considérée comme une source d’entités toxiques diffusant dans le milieu pulmonaire. Dans le cas des particules de quartz, par exemple, on peut imaginer que certains sites superficiels pourraient constituer la source de dérivés oxygénés actifs. Les modèles mis au point selon ces axes pourraient également être affinés pour tenir compte de la grande variabilité interindividuelle de la clairance alvéolaire généralement observée. Ce phénomène a été documenté expérimentalement avec l’amiante, les animaux à taux de rétention élevé présentant un risque accru de développer une asbestose (Bégin, Massé et Sébastien, 1989).
Jusqu’ici, les modèles en question étaient utilisés exclusivement en médecine expérimentale. Ils pourraient cependant être utiles aux épidémiologistes (Smith, 1991). La plupart des études épidémiologiques analysant la relation exposition-réponse reposent sur «l’exposition cumulée», c’est-à-dire un index d’exposition obtenu en intégrant dans le temps la concentration estimée des poussières en suspension dans l’air à laquelle avaient été exposés des travailleurs (produit intensité x durée). L’emploi de l’exposition cumulée a toutefois certaines limites. Les analyses basées sur cet index supposent implicitement que la durée et l’intensité ont des effets équivalents sur le risque (Vacek et McDonald, 1991).
L’utilisation de modèles dosimétriques très élaborés pourrait peut-être expliquer une observation fréquemment rencontrée dans l’épidémiologie des pneumoconioses, à savoir «les différences considérables d’une population de travailleurs à l’autre»; ce phénomène a été particulièrement net avec l’asbestose (Becklake, 1991) et la PH (Attfield et Morring, 1992). En mettant en relation la prévalence de la maladie avec l’exposition cumulée, on a observé de grandes différences de risques (jusqu’à cinquante fois) entre certaines catégories professionnelles. L’origine géologique du charbon (qualité du charbon) a fourni une explication partielle à la PH, les gisements de qualité supérieure (charbon à teneur élevée en carbone, comme l’anthracite) étant associés à un risque plus grand. Le phénomène reste inexpliqué dans le cas de l’asbestose. Les incertitudes quant à la justesse de la courbe exposition-réponse influent, théoriquement au moins, sur les résultats, même avec les normes d’exposition actuelles.
De façon plus générale, la mesure de l’exposition demeure indispensable à l’évaluation du risque et à l’établissement de limites d’exposition. L’utilisation des nouveaux modèles dosimétriques pourra améliorer l’évaluation du risque lié aux pneumoconioses; son but ultime est d’augmenter le degré de protection assuré par les limites d’exposition (Kriebel, 1994).
La toxicité spécifique de chaque type de poussière, liée aux caractéristiques physico-chimiques des particules (y compris les caractéristiques les plus subtiles telles que les caractéristiques de surface), constitue probablement la notion la plus importante qui s’est progressivement imposée au cours des vingt dernières années. Au tout début des recherches, on ne faisait pas de distinction entre les diverses «poussières minérales». Par la suite, on a introduit des catégories génériques: amiante, charbon, fibres inorganiques artificielles, phyllosilicates et silice. Mais cette classification s’est montrée trop imprécise pour tenir compte du grand nombre d’effets biologiques observés. On a recours aujourd’hui à une classification minéralogique plus précise: c’est ainsi que l’on distingue les divers types minéralogiques d’amiante: chrysotile (groupe serpentine), amosite, crocidolite et trémolite (groupe amphibole). En ce qui concerne la silice, on fait généralement une distinction entre le quartz (de loin le plus abondant), les autres cristaux polymorphes et les variétés amorphes. Dans l’industrie charbonnière, les charbons de qualité supérieure et inférieure doivent être traités séparément, car il est établi que le risque de PH, et surtout le risque de fibrose massive progressive, est beaucoup plus grand en cas d’exposition aux poussières provenant des mines de charbon de qualité supérieure.
Mais la classification minéralogique connaît elle aussi des limites. Il existe des arguments, tant expérimentaux qu’épidémiologiques (prenant en considération les «différences considérables d’une population de travailleurs à l’autre»), qui suggèrent que la toxicité intrinsèque d’un type minéralogique particulier de poussières peut être modulée en agissant sur les caractéristiques physico-chimiques des particules. Cela pose la délicate question de la signification toxicologique de chacun des nombreux paramètres pouvant servir à décrire une particule de poussière ou un nuage de poussières. Au niveau particulaire, plusieurs paramètres peuvent être envisagés: chimie stérique, structure cristalline, forme, masse volumique, taille, surface, chimie de surface et charge superficielle. On atteint un degré de complexité plus élevé avec les nuages de poussières du fait des variations de ces paramètres (par exemple, la granulométrie et la composition des poussières mixtes).
La taille des particules et leur chimie de surface ont été les deux paramètres les plus étudiés pour expliquer l’effet de modulation. Comme nous l’avons vu, les mécanismes de rétention varient avec la taille. Mais la taille peut, elle aussi, moduler la toxicité in situ, comme en témoignent de nombreuses études animales et in vitro.
Dans le domaine des fibres minérales, la taille était un facteur jugé si important que c’est sur elle que reposait une théorie pathogénétique. Celle-ci attribuait la toxicité des particules fibreuses (naturelles aussi bien qu’artificielles) à la forme et à la taille des particules et ne laissait aucun rôle à la composition chimique. Dans le cas des fibres, le facteur taille exige que l’on tienne compte de leur longueur et de leur diamètre; une matrice bidimensionnelle devrait être utilisée pour la définition de leur granulométrie, les plages utiles étant de 0,03 à 2,0 µm pour le diamètre et de 0,3 à 300 µm pour la longueur (Sébastien, 1991). En intégrant les résultats de nombreuses études, Lippman (1988) a assigné un index de toxicité à plusieurs cellules de cette matrice. On a généralement tendance à croire que les fibres longues et fines sont les plus dangereuses. Comme les normes actuellement utilisées en hygiène industrielle sont basées sur un examen au microscope optique, elles négligent les fibres les plus fines. S’il y a un certain intérêt théorique à évaluer la toxicité spécifique de chaque cellule de la matrice, cet intérêt est limité en pratique par le fait que chaque type de fibre est associé à une granulométrie spécifique qui demeure relativement uniforme. Pour les particules compactes telles que le charbon et la silice, on ignore s’il est possible d’attribuer un rôle spécifique aux différentes sous-fractions granulométriques des particules déposées dans le compartiment alvéolaire des poumons.
Des théories pathogéniques plus récentes émises dans le domaine des poussières minérales font intervenir des sites chimiques actifs (ou fonctionnalités) présents à la surface des particules. La naissance d’une particule par division de la substance mère provoque la rupture hétérolytique ou homolytique de certaines liaisons chimiques. Ce qui se passe au cours de la rupture et des recombinaisons ou réactions ultérieures avec les molécules de l’air atmosphérique ou les molécules biologiques relève de la chimie de surface des particules. En ce qui concerne les particules de quartz, par exemple, plusieurs fonctionnalités chimiques particulièrement intéressantes ont été décrites: ponts siloxanes, groupes de silanols, groupements partiellement ionisés et radicaux à base de silicone.
Ces fonctionnalités peuvent amorcer des réactions de type acide-base et oxydoréduction (redox) sur lesquelles l’attention n’a été attirée que récemment (Dalal, Shi et Vallyathan, 1990; Fubini et coll., 1990; Pézerat et coll., 1989; Kamp et coll., 1992; Kennedy et coll., 1989; Razzaboni et Bolsaitis, 1990). On a maintenant la preuve que les particules porteuses de radicaux en surface peuvent induire la formation de composés oxygénés réactifs, même en milieu cellulaire. Il n’est pas certain que toute la production des composés oxygénés soit imputable aux radicaux de surface. On a émis l’hypothèse que ces sites peuvent déclencher l’activation de cellules pulmonaires (Hemenway et coll., 1994). D’autres sites peuvent participer à l’activité membranolytique des particules cytotoxiques par des réactions telles que l’attraction ionique ou la formation de liaisons hydrogènes ou hydrophobes (Nolan et coll., 1981; Heppleston, 1991).
A partir du moment où l’importance de la chimie de surface a été reconnue en tant que facteur déterminant de la toxicité des poussières, plusieurs tentatives ont été faites pour modifier les surfaces naturelles des particules de poussières minérales afin de réduire leur toxicité, comme l’avaient montré les modèles expérimentaux.
On a constaté que l’adsorption d’aluminium sur des particules de quartz réduit leur potentiel fibrogène et facilite la clairance alvéolaire (Dubois et coll., 1988). L’administration de N-oxyde de polyvinylpyridine (PVPNO) a également eu un effet prophylactique (Goldstein et Rendall, 1987; Heppleston, 1991). Plusieurs autres procédés de modification ont été utilisés: polissage, traitement thermique, attaque à l’acide et adsorption de molécules organiques (Wiessner et coll., 1990). Des particules de quartz fraîchement concassé ont présenté une activité de surface extrêmement importante (Kuhn et Demers, 1992; Vallyathan et coll., 1988). Il est intéressant de noter que chaque modification de la «surface fondamentale» a entraîné une diminution de la toxicité du quartz (Sébastien, 1990). La pureté superficielle de plusieurs variétés naturelles de quartz pourrait être responsable de certaines différences observées dans leur toxicité (Wallace et coll., 1994). Il existe des arguments en faveur de l’hypothèse selon laquelle l’importance de la surface de quartz non contaminée est un paramètre important (Kriegseis, Scharmann et Serafin, 1987).
La multiplicité des paramètres entrant en ligne de compte, ainsi que leur distribution dans le nuage de poussières ouvrent un très grand nombre de possibilités de description de la concentration dans l’air: concentration pondérable, concentration numérique, concentration en surface et concentration par fractions granulométriques. C’est dire qu’il est possible de définir de nombreux indices d’exposition et nécessaire d’évaluer la signification toxicologique de chacun d’eux. Les normes actuellement utilisées en hygiène industrielle reflètent cette multiplicité. Pour l’amiante, elles reposent sur la concentration numérique des particules fibreuses dans une plage granulométrique donnée. Pour la silice et le charbon, elles sont basées sur la concentration pondérale des particules respirables. Certaines normes ont également été établies pour les cas d’exposition à des mélanges de particules contenant du quartz. Aucune norme n’est fondée sur les propriétés de surface.
Les pneumoconioses sont des fibroses pulmonaires interstitielles diffuses ou nodulaires. La réaction fibreuse implique une activation des fibroblastes pulmonaires (Goldstein et Fine, 1986), ainsi que la production et le métabolisme des composants du tissu conjonctif (collagène, élastine et glycosaminoglycanes). On estime qu’elle correspond à un stade tardif de cicatrisation d’une lésion pulmonaire (Niewoehner et Hoidal, 1982). Même si plusieurs facteurs, essentiellement liés aux caractéristiques de l’exposition, peuvent moduler la réponse pathologique, il est intéressant de noter que chaque type de pneumoconiose se caractérise par ce qu’il est possible d’appeler une lésion fondamentale. L’alvéolite fibrosante qui se développe autour des voies respiratoires périphériques constitue la lésion fondamentale de l’exposition à l’amiante (Bégin et coll., 1992). Le nodule silicotique est la lésion fondamentale de la silicose (Ziskind, Jones et Weil, 1976), tandis que la PH simple est formée de macules et de nodules (Seaton, 1983).
La pathogenèse des pneumoconioses est généralement présentée comme une cascade d’événements qui se succèdent ainsi: alvéolite alvéolaire macrophagique, information par les cytokines des cellules inflammatoires, lésion oxydative, prolifération et activation des fibroblastes et métabolisme du collagène et de l’élastine. L’alvéolite alvéolaire macrophagique est une réaction caractérisée à la rétention de poussières minérales fibrosantes (Rom, 1991). L’alvéolite se définit comme une augmentation du nombre de macrophages alvéolaires activés qui libèrent d’importantes quantités de médiateurs: oxydants, chimiotaxines, facteurs de croissance des fibroblastes et protéases. Les chimiotaxines attirent les granulocytes neutrophiles et, avec les macrophages, elles peuvent libérer des oxydants susceptibles de léser les cellules épithéliales alvéolaires. Les facteurs de croissance des fibroblastes gagnent l’interstitium où ils induisent la réplication des fibroblastes et augmentent la production de collagène.
La cascade commence lors de la première déposition des particules dans les alvéoles. Avec l’amiante, par exemple, la lésion pulmonaire initiale survient presque immédiatement après l’exposition au niveau des bifurcations des canaux alvéolaires. Chez les animaux de laboratoire, une heure d’exposition environ suffit pour provoquer la fixation active des fibres par les cellules épithéliales de type I (Brody et coll., 1981). En quarante-huit heures, un nombre accru de macrophages alvéolaires s’accumule au niveau des sites de déposition. En cas d’exposition chronique, ce processus peut induire une alvéolite fibrosante péribronchiolaire.
On ne connaît pas le mécanisme exact par lequel les particules déposées entraînent une lésion biochimique primaire du revêtement alvéolaire, d’une cellule spécifique ou d’un de ses organites. Il est possible que des réactions biochimiques extrêmement rapides et complexes induisent la formation de radicaux libres, une peroxydation des lipides et une déplétion de certains types de molécules protectrices des cellules essentielles. On a démontré que les particules minérales peuvent se comporter comme des substrats catalytiques dans la production de radicaux hydroxyle et superoxyde (Guilianelli et coll., 1993).
Au niveau cellulaire, on dispose d’un peu plus d’informations. Après déposition dans les alvéoles, les très fines cellules épithéliales de type I sont facilement lésées (Adamson, Young et Bowden, 1988). Les macrophages et d’autres cellules inflammatoires sont attirés par la lésion et la réponse inflammatoire est amplifiée par la libération de métabolites de l’acide arachidonique tels que les prostaglandines et les leucotriènes, accompagnée d’une exposition de la membrane basale (Holtzman, 1991; Kuhn et coll., 1990; Englen et coll., 1989). A ce stade de la lésion primaire, l’architecture pulmonaire se désorganise en générant un œdème interstitiel.
Au cours du processus inflammatoire chronique, la surface des particules de poussières et les cellules inflammatoires activées libèrent dans les voies respiratoires inférieures d’importantes quantités de composés oxygénés réactifs. L’agression oxydative des poumons entraîne des effets détectables sur le système de défense antioxydant (Heffner et Repine, 1989), avec expression d’enzymes antioxydantes comme la superoxyde dismutase, les glutathion peroxydases et la catalase (Engelen et coll., 1990). Ces facteurs se trouvent dans le tissu pulmonaire, le liquide interstitiel et les hématies circulantes. Le nature des enzymes antioxydantes peut dépendre du type de poussière fibrogène (Janssen et coll., 1992). On sait que les radicaux libres sont des médiateurs des lésions tissulaires et de la maladie (Kehrer, 1993).
La fibrose interstitielle résulte d’un processus de réparation. De nombreuses théories ont été avancées pour expliquer la mise en œuvre d’un tel processus; c’est l’interaction entre les macrophages et des fibroblastes qui a reçu le plus d’attention. Les macrophages activés sécrètent une série de cytokines proinflammatoires: TNF, IL-1, «transforming growth factor» (facteur de croissance transformant) et «platelet-derived growth factor» (facteur de croissance d’origine plaquettaire). Ils produisent également de la fibronectine, glycoprotéine de la surface cellulaire qui exerce une attraction chimique et qui, dans certaines conditions, se comporte comme un stimulant de la croissance des cellules mésenchymateuses. Quelques auteurs estiment que certains facteurs sont plus importants que d’autres. Par exemple, on a émis l’hypothèse que le TNF joue un grand rôle dans la pathogenèse de la silicose. Chez des souris de laboratoire, on a pu montrer que les anticorps anti-TNF inhibent presque complètement la déposition du collagène après l’instillation de silice (Piguet et coll., 1990). On a également attribué un grand rôle à la libération du facteur de croissance d’origine plaquettaire et du facteur de croissance transformant dans la pathogenèse de l’asbestose (Brody, 1993).
Malheureusement, la plupart des théories impliquant les macrophages et les fibroblastes ont tendance à ignorer l’équilibre potentiel entre les cytokines fibrogènes et leurs inhibiteurs (Kelley, 1990). En effet, le déséquilibre qui apparaît entre les agents oxydants et antioxydants, les protéases et les antiprotéases, les métabolites de l’acide arachidonique, les élastases et les collagénases, ainsi que les déséquilibres entre les diverses cytokines et les facteurs de croissance seraient à l’origine du remodelage de la composante interstitielle aboutissant aux différentes formes de pneumoconioses (Porcher et coll., 1993). Dans les pneumoconioses, l’équilibre se déplace nettement vers la prédominance des effets lésionnels des cytokines.
Comme les cellules de type I sont incapables de se diviser à la suite de la lésion primaire, la barrière épithéliale est remplacée par des cellules de type II (Lesur et coll., 1992). Il semble que si cette réparation épithéliale est efficace et que les cellules régénérantes de type II ne subissent pas d’autre agression, le risque de fibrogenèse est peu probable. Dans certaines conditions, la réparation par les cellules de type II est excessive et aboutit à une protéinose alvéolaire. Ce processus a été parfaitement mis en évidence après exposition à la silice (Heppleston, 1991). On ignore l’importance de l’influence des altérations des cellules épithéliales sur les fibroblastes. Il semble donc que la fibrogenèse débute dans les zones qui sont le siège d’une importante lésion épithéliale, car les fibroblastes se répliquent, puis se différencient et sécrètent davantage de collagène, de fibronectine et d’autres composants de la matrice extracellulaire.
Il existe une littérature abondante sur la biochimie des différents types de collagène formés dans les pneumoconioses (Richards, Masek et Brown, 1991). Le métabolisme de ces collagènes et leur stabilité dans les poumons sont des éléments importants de la fibrogenèse. Il en est probablement de même pour les autres composants du tissu conjonctif lésé. Le métabolisme du collagène et de l’élastine est particulièrement impliqué dans la phase de cicatrisation, car ces protéines sont indispensables à la structure et à la fonction des poumons. On a également démontré que les troubles de la synthèse de ces protéines permettent de déterminer si un emphysème ou une fibrose se développe après une lésion pulmonaire (Niewoehner et Hoidal, 1982). Au cours de la maladie, des mécanismes tels que l’augmentation de l’activité transglutaminase pourraient favoriser la formation de masses protéiques stables. Dans certaines lésions fibreuses de la PH, la fraction protéique représente un tiers des lésions, le reste étant composé de poussières et de phosphate de calcium.
Si l’on ne considère que le métabolisme du collagène, plusieurs stades de fibrose sont possibles, dont certains sont potentiellement réversibles, alors que d’autres ont une évolution progressive. On a démontré expérimentalement qu’à moins d’une exposition considérable les lésions initiales peuvent régresser et qu’il est alors peu probable que s’installe une fibrose irréversible. Dans l’asbestose, par exemple, plusieurs types de réactions pulmonaires ont été décrits (Bégin, Cantin et Massé, 1989): réaction inflammatoire transitoire sans lésion, réaction avec faible rétention et cicatrices fibreuses limitées aux voies respiratoires distales, réaction inflammatoire majeure entretenue par le maintien de l’exposition et la faible élimination des fibres les plus longues.
On peut conclure de ces études que l’exposition aux particules de poussières fibrogènes peut déclencher divers processus biochimiques et cellulaires complexes qui interviennent dans les lésions pulmonaires et leur réparation. Les modalités d’exposition, les caractéristiques physico-chimiques des particules de poussières et une éventuelle susceptibilité individuelle semblent être les facteurs déterminants de l’équilibre délicat régnant entre ces différents processus. Les caractéristiques physico-chimiques détermineront le type de lésion fondamentale finale. Les modalités de l’exposition semblent conditionner la succession des événements. Certains faits paraissent indiquer que dans la plupart des cas d’exposition relativement peu importante, la réaction pulmonaire peut se limiter à l’apparition de lésions non progressives, sans incapacité de travail ni invalidité.
La surveillance médicale et le dépistage ont toujours fait partie de la stratégie préventive des pneumoconioses. Dans ce contexte, la possibilité de déceler des lésions précoces est intéressante. L’amélioration des connaissances physiopathologiques a permis la mise au point de plusieurs marqueurs biologiques (Borm, 1994) et la sophistication et l’utilisation de techniques d’investigation pulmonaire «non classiques», telles que la mesure de la clairance des dépositions de diéthylènetriamine pentacétique marqué au technétium 99 (99Tc-DTPA) pour évaluer l’intégrité de l’épithélium pulmonaire (O’Brodovich et Coates, 1987) et le balayage pulmonaire quantitatif au gallium 67 pour apprécier l’activité inflammatoire (Bisson, Lamoureux et Bégin, 1987).
Plusieurs marqueurs biologiques ont été envisagés dans le domaine des pneumoconioses: les macrophages de l’expectoration, les facteurs de croissance sériques, le procollagène sérique de type III, les antioxydants érythrocytaires, la fibronectine, l’élastase leucocytaire, la métalloendopeptidase neutre et les peptides d’élastine plasmatiques, les hydrocarbures volatils de l’air expiré et la libération de TNF par les monocytes du sang périphérique. Les marqueurs biologiques sont théoriquement très intéressants, mais il faudra encore de nombreuses études pour évaluer précisément leur signification. Cet effort de validation sera très exigeant, car il faudra que les chercheurs réalisent des études épidémiologiques prospectives. Cet effort a été fait récemment pour la sécrétion de TNF par les monocytes du sang périphérique dans la PH. Le TNF s’est avéré être un marqueur intéressant de la progression de la PH (Borm, 1994). Outre les aspects scientifiques du rôle des marqueurs biologiques dans la physiopathologie des pneumoconioses, il convient d’examiner soigneusement d’autres questions liées à l’utilisation de ces marqueurs (Schulte, 1993), à savoir les possibilités de prévention, le retentissement sur la médecine du travail et les problèmes éthiques et légaux.
Au cours des premières décennies de ce siècle, la pneumoconiose était considérée comme une maladie entraînant l’invalidité des sujets jeunes et une mort prématurée. Dans les pays industriels, elle est désormais considérée comme une simple anomalie radiologique, sans incapacité fonctionnelle ou invalidité (Sadoul, 1983). Cependant, deux constatations s’opposent à ce tableau optimiste. Premièrement, même si la pneumoconiose reste une maladie relativement silencieuse et asymptomatique en cas d’exposition limitée, il faut savoir qu’elle peut évoluer vers des formes plus sévères et invalidantes. Les facteurs influant sur cette progression sont extrêmement importants à envisager dans le cadre de l’étiopathogenèse de la maladie. En second lieu, on a désormais la preuve que certaines pneumoconioses peuvent retentir sur l’état général et favoriser l’apparition d’un cancer pulmonaire.
La nature chronique et progressive de l’asbestose a été documentée, de la lésion infraclinique initiale jusqu’à l’asbestose clinique (Bégin, Cantin et Massé, 1989). Les techniques modernes d’investigation pulmonaire (LBA, TDM, scintigraphie pulmonaire au gallium 67) ont révélé que l’inflammation et les lésions étaient présentes en permanence dès l’exposition et jusqu’au développement de la maladie clinique, en passant par la phase de latence ou infraclinique. On a rapporté (Bégin et coll., 1985) que 75% des sujets sans asbestose clinique ayant une scintigraphie au gallium 67 positive évoluaient vers une asbestose clinique diffuse en quatre ans. Chez l’humain et les animaux de laboratoire, l’asbestose peut s’aggraver après le diagnostic de la maladie et la cessation de l’exposition. Il est très probable que l’histoire de l’exposition précédant le diagnostic soit un élément majeur de l’évolution. Certaines données expérimentales militent en faveur de la notion d’une asbestose non progressive associée à une exposition inductrice légère et à l’arrêt de l’exposition au moment du diagnostic (Sébastien, Dufresne et Bégin, 1994). En supposant qu’il peut en être de même chez l’humain, il serait de première importance de déterminer avec précision la métrologie de l’«exposition inductrice légère». Malgré tous les efforts de dépistage au sein des populations de travailleurs exposés à l’amiante, cette information fait toujours défaut.
On sait parfaitement que l’exposition à l’amiante peut entraîner un risque majeur de cancer du poumon. Bien que l’on admette que l’amiante est cancérogène en soi, on a longtemps débattu pour savoir si le risque de cancer pulmonaire chez les travailleurs de l’industrie de l’amiante était lié à l’exposition à l’amiante ou à la fibrose pulmonaire (Hughes et Weil, 1991). Cette question n’a pas encore été résolue.
Grâce à l’amélioration continuelle des conditions de travail dans l’industrie minière moderne, la PH est aujourd’hui une maladie qui ne concerne pratiquement que des mineurs retraités. Si la PH simple est une maladie asymptomatique et sans effets évidents sur la fonction pulmonaire, la fibrose massive progressive (FMP) est un état beaucoup plus sévère, comportant des altérations importantes de la structure pulmonaire, une atteinte de la fonction respiratoire et une diminution de l’espérance de vie. De nombreuses études ont essayé d’identifier les facteurs déterminant l’évolution vers la FMP (rétention importante de poussières dans les poumons, qualité du charbon, infection mycobactérienne ou stimulation immunologique). Une théorie unificatrice a été proposée (Vanhee et coll., 1994), basée sur une inflammation alvéolaire continue et sévère avec activation des macrophages alvéolaires et production importante de composés oxygénés réactifs, de facteurs chimiotactiques et de fibronectine. Les autres complications de la PH sont l’infection mycobactérienne, le syndrome de Caplan et la sclérodermie. Il n’existe aucune preuve de l’augmentation du risque de cancer pulmonaire chez les houilleurs.
La forme chronique de la silicose résulte d’une exposition, mesurée en décennies plutôt qu’en années, à des poussières respirables contenant généralement moins de 30% de quartz. Mais dans les cas d’exposition non contrôlée à des poussières riches en quartz (antécédents d’exposition par sablage, par exemple), des formes aiguës et accélérées peuvent apparaître en quelques mois seulement. Les cas aigus et accélérés présentent un risque particulièrement élevé de complication par la tuberculose (Ziskind, Jones et Weil, 1976). Il est également possible d’observer une évolution, avec apparition de lésions de grande taille oblitérant les structures pulmonaires, que l’on appelle silicose compliquée ou FMP.
Quelques études ont été consacrées à l’évolution de la silicose en fonction de l’exposition et ont donné des résultats contradictoires quant aux relations entre l’évolution et l’exposition, avant et après la survenue des troubles (Hessel et coll., 1988). Infante-Rivard et coll. (1991) ont récemment étudié les facteurs pronostiques influant sur la survie des patients silicotiques au bénéfice de prestations d’invalidité. Les patients présentant uniquement de petites opacités sur leur radiographie pulmonaire, sans dyspnée, sans expectoration et sans bruits anormaux à l’auscultation, avaient une survie comparable à celle des témoins. La survie des autres patients était inférieure. Enfin, il faut noter que la relation entre silice, silicose et cancer du poumon a récemment suscité des inquiétudes. Des arguments ont été avancés pour et contre le potentiel cancérogène intrinsèque de la silice (Agius, 1992). Celle-ci peut renforcer l’effet de puissants cancérogènes ambiants, notamment de la fumée du tabac, en agissant comme un activateur peu puissant de la cancérogenèse ou en perturbant leur élimination. De plus, il se peut que le processus pathologique associé à la silicose ou y conduisant comporte un risque accru de cancer du poumon.
De nos jours, l’évolution et les complications des pneumoconioses pourraient être considérées comme un problème majeur sous l’angle de leur prise en charge médicale. L’emploi des techniques classiques d’investigation pulmonaire a été amélioré afin de permettre un diagnostic précoce de la maladie (Bégin et coll., 1992), c’est-à-dire à un stade où la pneumoconiose se limite à ses signes radiologiques, sans incapacité fonctionnelle ni invalidité. Dans un avenir proche, il est probable que l’on disposera d’une batterie de marqueurs biologiques permettant la mise en évidence de stades encore plus précoces de la maladie. La question de savoir s’il faut autoriser un travailleur chez qui l’on a diagnostiqué une pneumoconiose — ou chez qui l’on a confirmé ce diagnostic à un stade précoce — à continuer d’exercer sa profession a longtemps préoccupé les responsables de la santé au travail. Cette question plutôt délicate comporte des aspects éthiques, sociaux et scientifiques. Si l’on dispose d’une littérature scientifique abondante sur l’induction de la pneumoconiose, les informations concernant son évolution et utilisables par les décideurs sont peu nombreuses et relativement contradictoires. Quelques tentatives ont été faites pour étudier le rôle de variables telles que l’histoire de l’exposition, l’accumulation de poussières et l’état de santé lors des premières manifestations. Les relations entre ces différentes variables compliquent encore le problème. Des recommandations ont été émises pour le dépistage et la surveillance médicale des travailleurs exposés aux poussières minérales (Wagner, 1998). Des programmes sont déjà ou vont être mis en œuvre dans ce sens; il est évident qu’ils profiteraient grandement de l’amélioration des connaissances scientifiques sur l’évolution de la maladie et, en particulier, sur la relation entre l’exposition et les caractéristiques de la rétention.
Une véritable masse d’informations a été apportée par de nombreuses disciplines scientifiques pour étayer l’étiopathogenèse des pneumoconioses. La principale difficulté consiste désormais à rassembler les éléments épars du puzzle pour les intégrer dans les mécanismes conduisant aux lésions fondamentales des pneumoconioses. Sans cette intégration indispensable, nous continuerons à avoir d’une part un petit nombre de lésions fondamentales, et d’autre part un très grand nombre de réactions biochimiques et cellulaires.
Jusqu’ici, les connaissances étiopathogéniques ont peu influencé les pratiques de l’hygiène industrielle, malgré la volonté marquée des hygiénistes de travailler en utilisant des limites d’exposition ayant une certaine signification biologique. Ils ont intégré deux notions importantes à leur pratique: la sélection granulométrique des particules de poussières respirables et la corrélation entre la toxicité et le type de poussières. Cette corrélation a conduit à quelques limites spécifiques pour chaque type de poussières. L’évaluation quantitative du risque, étape indispensable dans l’établissement des limites d’exposition, est un exercice compliqué, et, cela, pour plusieurs raisons, notamment le grand nombre d’indices d’exposition possibles, le manque d’informations sur l’exposition antérieure, la difficulté rencontrée avec les modèles épidémiologiques comportant de multiples indices et la difficulté à estimer la dose à partir des informations sur l’exposition. Les limites d’exposition actuelles, parfois extrêmement imprécises, sont probablement suffisamment basses pour assurer une protection correcte. Les différences dans la relation exposition-réponse observées d’une population de travailleurs à l’autre reflètent cependant nos carences dans la maîtrise du phénomène.
L’apport de nouvelles connaissances sur la cascade d’événements physiopathologiques aboutissant à l’installation d’une pneumoconiose n’a pas modifié l’approche classique de la surveillance des travailleurs, mais elle a considérablement contribué à faciliter le diagnostic médical de la maladie (pneumoconiose) à un stade précoce, alors que la maladie n’a qu’un retentissement limité sur la fonction respiratoire. Ce sont précisément les sujets qui sont encore aux premiers stades de la maladie qu’il faut identifier et soustraire à toute nouvelle exposition importante afin d’éviter, par une surveillance médicale appropriée, que l’affection ne devienne invalidante.
La silicose est une maladie pulmonaire fibrosante provoquée par l’inhalation et la rétention de poussières renfermant de la silice libre et la réaction pulmonaire à ces poussières. Bien que l’on en connaisse la cause, la prévalence de cette maladie respiratoire professionnelle grave, mutilante et parfois mortelle, continue à être importante dans le monde entier. La silice (dioxyde de silicium) est le principal composant de l’écorce terrestre. L’exposition professionnelle à des particules de silice de taille respirable (diamètre aérodynamique compris entre 0,5 et 5 µm) est associée à l’exploitation des mines, minières et carrières, aux travaux de forage, au percement de galeries et de tunnels et au sablage (projection d’abrasifs contenant du quartz). L’exposition à la silice présente également des risques pour les tailleurs de pierre, les potiers, les fondeurs et les ouvriers manipulant de la silice concassée ou des matériaux réfractaires. L’exposition à la silice étant extrêmement répandue et le sable siliceux un élément bon marché et polyvalent dans de nombreux procédés de fabrication, des millions de travailleurs dans le monde courent le risque de contracter cette maladie dont on ne connaît pas la prévalence réelle.
La silicose est une affection respiratoire professionnelle résultant de l’inhalation de poussières de dioxyde de silicium, communément appelé silice, sous forme cristalline (généralement du quartz), mais aussi sous d’autres formes cristallines importantes, par exemple la cristobalite et la tridymite. Ces formes sont également désignées sous l’appellation de «silice libre» pour les distinguer des silicates. La teneur en silice des différentes formations rocheuses, telles que le grès, le granit ou l’ardoise, varie de 20% à près de 100%.
Bien que la silicose soit une maladie ancienne, de nouveaux cas continuent à être déclarés tant dans les pays développés qu’en développement. Au début de ce siècle, la silicose était une cause majeure de morbidité et de mortalité. Les travailleurs sont aujourd’hui encore exposés aux poussières de silice dans un grand nombre de professions; si les techniques mises en œuvre ne sont pas assorties d’un contrôle rigoureux de l’empoussiérage, il peut en résulter une exposition à des concentrations de particules bien plus dangereuses que celles rencontrées dans les ateliers non mécanisés. Chaque fois que l’on s’attaque à l’écorce terrestre et que l’on utilise ou traite des roches ou du sable siliceux, il y a un risque respiratoire potentiel pour les travailleurs. On continue à rapporter des cas de silicose dans des branches et des professions qui n’étaient pas reconnus auparavant comme des zones à risque, ce qui dénote la présence ubiquitaire de la silice. En fait, en raison du temps de latence et de la chronicité de cette affection — qui peut apparaître et progresser même après la cessation de l’exposition —, des travailleurs actuellement exposés pourront fort bien ne pas présenter de troubles avant le siècle prochain. Dans de nombreux pays, les mines, minières et carrières, les travaux en galeries, les fonderies et les travaux de sablage présentent toujours un risque majeur d’exposition à la silice et des épidémies de silicose continuent à se produire, même dans les pays développés.
On décrit habituellement des formes chroniques, accélérées et aiguës de la silicose. Ces expressions anatomocliniques de la maladie correspondent à des différences en termes d’intensité de l’exposition, de période de latence et d’évolution. La forme chronique ou classique succède habituellement à une ou plusieurs décennies d’exposition à des poussières respirables contenant du quartz et elle peut évoluer vers une fibrose massive progressive (FMP). La forme accélérée succède à une exposition plus courte et plus intense et évolue plus rapidement. Quant à la forme aiguë, elle peut apparaître à la suite d’une exposition brève et intense à de fortes concentrations de poussières respirables ayant une teneur élevée en silice, et, cela, pendant une durée qui se mesure en mois plutôt qu’en années.
La silicose chronique constitue la forme classique de cette affection; elle peut être asymptomatique ou provoquer une dyspnée d’effort qui s’aggrave insidieusement ou de la toux (souvent imputée à tort au vieillissement). Elle se traduit par des anomalies radiologiques à petites (<10 mm) opacités arrondies prédominant dans les lobes supérieurs. L’anamnèse révèle souvent une période d’exposition précédant de quinze années ou plus l’apparition des premiers symptômes. Sur le plan anatomopathologique, la forme chronique se caractérise par la présence de nodules silicotiques. La lésion consiste en une zone centrale acellulaire, entourée de bandes de fibres collagènes hyalinisées à disposition concentrique, elles-mêmes entourées de tissu conjonctif cellulaire contenant des fibres de réticuline. La silicose chronique peut évoluer vers une FMP (parfois appelée silicose compliquée), même après le retrait de l’exposition aux poussières siliceuses.
La fibrose massive progressive est plus susceptible d’entraîner une dyspnée d’effort. Cette forme de maladie se caractérise par des opacités nodulaires de plus de 1 cm sur les radiographies pulmonaires et généralement par une chute de la DLCO (capacité de diffusion du monoxyde de carbone), une diminution de la pression de l’oxygène dans le sang artériel au repos et à l’effort et un important syndrome restrictif en spirométrie ou à la mesure du volume pulmonaire. Une déformation de l’arbre bronchique peut également provoquer une obstruction des voies respiratoires et une toux productive. Des infections bactériennes récidivantes, comparables à celles observées dans la dilatation des bronches, peuvent se produire. La survenue d’un amaigrissement et l’apparition de cavernes au sein des opacités de grande taille doit faire suspecter une tuberculose ou une autre infection mycobactérienne. Le pneumothorax est une complication pouvant menacer le pronostic vital, car la fibrose pulmonaire peut gêner la réexpansion pulmonaire. Au stade terminal, on observe habituellement une insuffisance respiratoire hypoxique avec cœur pulmonaire.
La silicose accélérée peut apparaître après des expositions plus intenses de durée plus brève (cinq à dix ans). Les symptômes, les anomalies radiologiques et les mesures physiologiques sont les mêmes que ceux observés dans la forme chronique. La détérioration de la fonction pulmonaire est plus rapide et de nombreux travailleurs atteints de la forme accélérée peuvent présenter une surinfection mycobactérienne. La silicose accélérée s’accompagne souvent d’une maladie auto-immune, sclérodermie ou sclérose systémique. La progression des anomalies radiologiques et des troubles fonctionnels peut être extrêmement rapide en cas de maladie auto-immune associée à la silicose.
Une silicose aiguë peut se développer après une exposition massive à la silice allant de quelques mois à deux ans. Une dyspnée majeure, un affaiblissement et un amaigrissement sont des symptômes inauguraux fréquents. Les images radiologiques de comblement alvéolaire diffus diffèrent de celles obtenues dans les formes plus chroniques de silicose. On a décrit les mêmes anomalies histologiques que dans la protéinose alvéolaire pulmonaire et des anomalies extrapulmonaires (rénales et hépatiques) ont parfois été signalées. L’aggravation rapide vers une insuffisance respiratoire hypoxique grave est l’évolution habituelle.
La tuberculose peut compliquer toutes les formes de silicose, mais le risque est maximal chez les patients atteints d’une forme aiguë ou accélérée. L’exposition à la silice seule, même en l’absence de silicose, peut également prédisposer à cette infection. M. tuberculosis est d’ordinaire le germe responsable, mais des mycobactéries atypiques s’observent également.
Même en l’absence de silicose radiologique, les travailleurs exposés à la silice peuvent présenter d’autres maladies associées à une exposition professionnelle aux poussières, telle qu’une bronchite chronique avec emphysème associé. Ces anomalies sont liées à de nombreuses expositions aux poussières minérales, y compris aux poussières contenant de la silice.
La pathogenèse exacte de la silicose n’est pas bien connue, mais de nombreux arguments militent en faveur d’une interaction entre les macrophages alvéolaires pulmonaires et les particules de silice déposées dans les poumons. Les caractéristiques de surface des particules de silice semblent favoriser l’activation des macrophages. Ces cellules libèrent alors des facteurs chimiotactiques et des médiateurs de l’inflammation qui induisent une nouvelle réponse cellulaire faisant intervenir les leucocytes polynucléaires, les lymphocytes et d’autres macrophages. Il se produit une libération de facteurs stimulant les fibroblastes qui favorisent la hyalinisation et la déposition du collagène. La lésion silicotique anatomopathologique qui en résulte est le nodule hyalin qui comprend une partie centrale acellulaire contenant de la silice libre entourée de volutes de collagène et de fibroblastes, et une partie périphérique active composée de macrophages, de fibroblastes, de plasmocytes et aussi de silice libre, comme le montre la figure 10.14.
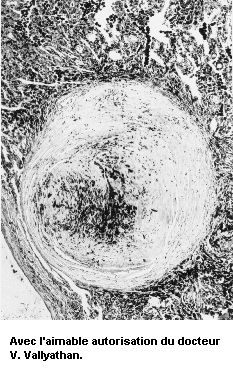
On ne connaît pas précisément les propriétés des particules de silice qui induisent la réponse pulmonaire décrite ci-dessus, mais les caractéristiques de surface peuvent jouer un rôle important. La nature et la portée de la réponse biologique sont généralement liées à l’intensité de l’exposition; toutefois, il semble de plus en plus évident que la silice fraîchement concassée peut être plus toxique que des poussières siliceuses plus anciennes, cet effet étant peut-être lié à la présence de radicaux réactifs sur les plans de clivage de la silice fraîchement concassée. Cela fournirait une explication physiopathologique aux cas de maladie avancée chez les sableurs et les foreurs au rocher qui sont soumis à une exposition particulièrement intense à ce type de silice fraîchement désintégrée.
La lésion toxique inaugurale peut résulter d’une réaction immunologique minime; elle peut cependant induire une réponse immunologique prolongée qui peut jouer un grand rôle dans les manifestations chroniques de la silicose. Ainsi, des anticorps antinucléaires peuvent apparaître dans la silicose accélérée et une sclérodermie, ou une autre connectivité, chez les travailleurs exposés à la silice. La sensibilité des travailleurs silicotiques aux infections, telles que la tuberculose et l’infection à Nocardia asteroides, est probablement liée à l’effet toxique de la silice sur les macrophages pulmonaires.
Le lien entre la silicose et la tuberculose est connu depuis près d’un siècle. Une tuberculose évolutive peut s’observer chez plus de 20% des travailleurs silicotiques dans les cas où la prévalence de la tuberculose dans la population est élevée. Là encore, le risque semble être beaucoup plus grand chez les sujets atteints de silicose aiguë.
Le principal symptôme de la silicose est habituellement la dyspnée, qui apparaît tout d’abord pendant l’activité ou à l’effort, puis au repos, à la suite de la disparition de la réserve pulmonaire. Cependant, en l’absence d’autre maladie respiratoire, la dyspnée peut être absente et le tableau peut être celui d’un travailleur asymptomatique ayant une radiographie pulmonaire anormale. La radiographie peut parfois montrer des signes de maladie très avancée, alors que les symptômes sont minimes. La survenue ou l’aggravation de la dyspnée peuvent annoncer le développement de complications telles que la tuberculose, l’obstruction des voies respiratoires ou la FMP. Une toux est souvent présente, secondaire à la bronchite chronique résultant d’une exposition professionnelle aux poussières, d’un tabagisme ou des deux à la fois. La toux peut parfois aussi être secondaire à la pression exercée par d’importantes masses de ganglions lymphatiques silicotiques sur la trachée ou les grosses bronches.
Les autres symptômes thoraciques sont moins fréquents que la dyspnée et la toux. L’hémoptysie est rare et devrait faire évoquer une complication. Une respiration sifflante et une oppression thoracique peuvent apparaître, généralement dans le cadre d’une obstruction des voies respiratoires ou d’une bronchite. Les douleurs thoraciques et l’hippocratisme digital ne sont pas caractéristiques de la silicose. Les symptômes systémiques, comme la fièvre et l’amaigrissement, suggèrent une complication à type d’infection ou de néoplasie. Les formes avancées de silicose sont associées à une insuffisance respiratoire progressive, avec ou sans cœur pulmonaire. Les signes physiques sont peu nombreux, sauf en cas de complication.
Les tout premiers signes radiologiques de silicose non compliquée sont généralement de petites opacités arrondies. On peut les décrire à l’aide de la Classification internationale du BIT des radiographies de pneumoconioses en se basant sur leur taille, leur forme et leur nombre. Dans la silicose, les opacités de type «q» et «r» prédominent. On a également décrit d’autres anomalies telles que des opacités linéaires ou irrégulières. Les opacités observées sur les radiographies représentent la sommation de nodules silicotiques pathologiques. Elles prédominent généralement dans les zones supérieures et, par la suite, elles peuvent atteindre d’autres sites. On note aussi parfois une lymphadénopathie hilaire qui précède les opacités parenchymateuses nodulaires. Une calcification en coquille d’œuf est fortement évocatrice d’une silicose, quoique cette anomalie soit rare.
La FMP se caractérise par la formation de grandes opacités. Celles-ci peuvent être classées dans les catégories A, B ou C en fonction de leur taille, en utilisant la Classification du BIT. Les opacités de grande taille ou les lésions de FMP tendent à se contracter, généralement dans les lobes supérieurs, en laissant un emphysème compensateur sur leurs bords et souvent dans les bases pulmonaires. Il s’ensuit que les petites opacités arrondies initialement observées peuvent parfois disparaître ou devenir moins nombreuses. Des anomalies pleurales peuvent s’observer, mais elles ne constituent pas une caractéristique radiologique fréquente de la silicose. Les opacités de grande taille peuvent faire évoquer un néoplasme; en l’absence de clichés plus anciens, le diagnostic différentiel peut être délicat. Toutes les lésions qui se creusent ou se modifient rapidement devraient faire rechercher une tuberculose évolutive. Une silicose aiguë peut se manifester par un comblement alvéolaire radiologique avec développement rapide d’une FMP ou de lésions massives compliquées (voir figures 10.15 et 10.16).
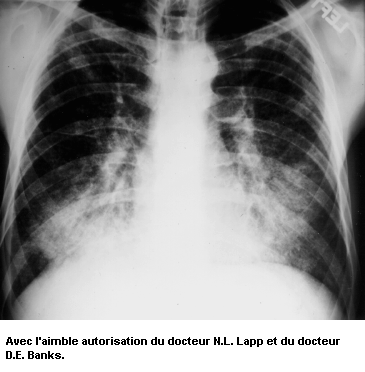
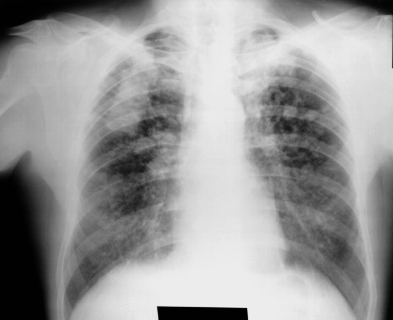
Les épreuves fonctionnelles respiratoires — spirométrie et capacité de diffusion — sont utiles pour évaluer cliniquement les sujets chez qui l’on suspecte une silicose. La spirométrie peut également être intéressante pour déceler précocement le retentissement sur la santé des expositions professionnelles aux poussières, car elle peut détecter les anomalies physiologiques susceptibles de précéder les anomalies radiologiques. Les troubles ventilatoires observés dans la silicose ne sont pas univoques. La spirométrie peut être normale ou, quand elle est anormale, les enregistrements peuvent mettre en évidence une obstruction, une restriction ou un trouble mixte. En fait, les troubles obstructifs sont les plus fréquents. Ces modifications ont tendance à s’aggraver avec la progression de la catégorie radiologique. Cependant, la corrélation entre les anomalies radiologiques et les troubles ventilatoires est médiocre. Dans la silicose aiguë et accélérée, les troubles fonctionnels sont plus marqués et leur progression est plus rapide. Dans la silicose aiguë, la progression radiologique s’accompagne d’une aggravation des troubles ventilatoires et d’altérations des échanges gazeux qui aboutissent à une insuffisance respiratoire et, en fin de compte, à la mort par hypoxie irréductible.
Si l’on dispose d’une anamnèse satisfaisante et d’une radiographie pulmonaire caractéristique, le diagnostic de silicose est généralement aisé à établir. Des difficultés ne surgissent qu’en cas d’aspect radiologique inhabituel ou quand l’histoire de l’exposition n’est pas connue. Une biopsie pulmonaire est rarement nécessaire au diagnostic. Cependant, des échantillons tissulaires sont utiles dans certaines situations cliniques, quand des complications sont présentes ou quand il faut procéder à un diagnostic différentiel avec une tuberculose, un cancer ou une FMP. Le matériel biopsique devrait être mis en culture; dans le cadre de recherches, il peut également être indiqué d’analyser les poussières. Si des fragments tissulaires sont nécessaires, il faut généralement procéder à une biopsie pulmonaire sous thoracoscopie pour recueillir un matériel d’examen correct.
La recherche d’une complication infectieuse, en particulier d’une tuberculose, est essentielle; toute modification de la toux ou la survenue d’une hémoptysie, d’une fièvre ou d’une perte de poids devrait appeler un bilan permettant d’exclure cette maladie curable.
La relation entre l’exposition à la silice, la silicose et le cancer du poumon continue à faire l’objet de controverses et à susciter de nouvelles recherches. En octobre 1996, un comité du Centre international de recherche sur le cancer (CIRC) a classé la silice cristalline parmi les substances cancérogènes du groupe I, sa décision reposant sur «des indications de cancérogénicité suffisantes» chez l’humain. Il persiste des incertitudes sur les mécanismes physiopathologiques sous-tendant le développement d’un cancer du poumon dans les populations exposées à la silice, et l’on s’interroge encore sur la nature de la relation entre silicose (ou fibrose pulmonaire) et cancer chez les travailleurs exposés. Quel que soit le mécanisme en cause, on en sait assez sur le lien entre l’exposition à la silice et la silicose pour insister sur la réduction et le contrôle de l’exposition chez les travailleurs risquant de développer la maladie.
La prévention reste la pierre angulaire de l’élimination de cette affection respiratoire professionnelle. L’amélioration des installations de ventilation et d’aspiration localisée, le confinement des opérations, les procédés par voie humide, la protection individuelle avec un choix correct d’appareils de protection respiratoire et, si possible, l’utilisation dans l’industrie d’agents moins dangereux que la silice sont autant de moyens de réduire l’exposition. Il importe également de parfaire l’éducation des travailleurs et des employeurs quant au danger de l’exposition aux poussières de silice et aux mesures permettant de lutter contre cette menace.
Si l’on diagnostique une silicose chez un travailleur, il est recommandé de le soustraire à toute nouvelle exposition à la silice; malheureusement, la maladie peut s’aggraver en dépit de cette mesure. Enfin, la détection d’un cas de silicose, en particulier s’il s’agit d’une forme aiguë ou accélérée, devrait inciter à une évaluation du lieu de travail afin de protéger les autres travailleurs exposés.
Les travailleurs exposés à la silice et à d’autres poussières minérales devraient subir un dépistage périodique des effets néfastes sur leur santé en complément, mais non pas en lieu et place, des mesures de lutte contre les poussières. Ce dépistage comporte généralement la recherche de symptômes respiratoires, d’anomalies de la fonction pulmonaire et de signes de cancer, ainsi que de tuberculose. Outre le dépistage individuel des travailleurs, il faut collecter des données sur des groupes de travailleurs à des fins de surveillance et de prévention. Des directives pour ces types d’études sont incluses dans la liste des références en fin de chapitre.
En cas d’insuccès de la prévention et de développement d’une silicose, le traitement vise essentiellement les complications de la maladie. Les mesures thérapeutiques sont les mêmes que celles communément utilisées pour traiter l’obstruction des voies respiratoires, les infections, le pneumothorax, l’hypoxie et l’insuffisance respiratoire compliquant les autres maladies respiratoires. Historiquement parlant, l’inhalation d’aérosols d’aluminium a échoué en tant que traitement spécifique de la silicose. Le N-oxyde de polyvinylpyridine (PVNO), polymère ayant protégé des animaux de laboratoire, ne peut être utilisé chez l’humain. Des études expérimentales récentes de la tétrandrine ont montré in vivo une diminution de la fibrose et de la synthèse du collagène chez des animaux exposés à la silice et traités avec ce médicament. On manque cependant actuellement de preuves valables de son efficacité chez l’humain et sa toxicité potentielle soulève des inquiétudes, en particulier son potentiel mutagène. Compte tenu de la prévalence élevée de la silicose dans certains pays, les études sur les associations de médicaments et d’autres mesures thérapeutiques se poursuivent. Aucune approche n’a été couronnée de succès pour l’instant et la recherche d’un traitement spécifique de la silicose s’est avérée décevante.
Toute poursuite de l’exposition est néfaste. Il convient de conseiller au malade de changer d’activité en lui fournissant les informations nécessaires sur la nature du risque auquel il a été exposé.
La recherche d’une complication infectieuse, en particulier d’une tuberculose, est un élément essentiel de la prise en charge médicale de la silicose. La pratique du BCG chez les patients silicotiques ayant une réaction tuberculinique négative n’est pas recommandée, mais l’administration préventive d’isoniazide (INH) chez ceux qui présentent une réaction positive à la tuberculine est conseillée dans les pays où la tuberculose a une prévalence faible. Le diagnostic d’une tuberculose évolutive chez des patients atteints de silicose peut être difficile. Certains symptômes tels que l’amaigrissement, la fièvre, les sueurs et le sentiment de malaise devraient inciter à pratiquer des radiographies et une recherche de bacilles acido-résistants dans les crachats, avec mise en culture. Les modifications radiologiques — l’agrandissement ou l’excavation de lésions coalescentes ou d’opacités nodulaires — sont particulièrement significatives. Les examens bactériologiques des crachats ne sont pas toujours fiables dans la silico-tuberculose. Il est souvent utile de réaliser une bronchoscopie permettant de recueillir d’autres échantillons à des fins de culture pour faciliter le diagnostic de tuberculose évolutive. L’utilisation d’une polychimiothérapie antituberculeuse chez les silicotiques est justifiée en présence d’un degré de suspicion moindre que chez les non-silicotiques en raison de la difficulté à apporter la preuve formelle d’une infection active. La rifampicine semble avoir accru le taux de succès du traitement de la silicose compliquée de tuberculose; dans certaines études récentes, la réponse au traitement à court terme en cas de silico-tuberculose a été comparable à celle observée chez les témoins atteints de tuberculose primaire.
Une assistance ventilatoire est indiquée en cas d’aggravation de l’insuffisance respiratoire par une complication curable. Le pneumothorax, spontané ou induit par la ventilation assistée, est généralement traité par la mise en place d’un drain thoracique. Une fistule broncho-pleurale peut apparaître et un avis et un traitement chirurgical devraient être envisagés.
Une silicose aiguë peut rapidement évoluer vers l’insuffisance respiratoire. Dans des cas où cette maladie ressemblait à une protéinose alvéolaire pulmonaire avec hypoxie majeure, on a tenté un traitement agressif comportant un lavage de la totalité des poumons sous anesthésie générale pour essayer d’améliorer les échanges gazeux et éliminer les débris alvéolaires. Bien que théoriquement prometteuse, l’efficacité du lavage pulmonaire total n’a pas été établie. On a également utilisé la corticothérapie dans la silicose aiguë, mais son intérêt reste à démontrer.
Certains patients jeunes atteints de silicose au stade terminal peuvent être candidats à une greffe de poumons ou d’un bloc cœur-poumons dans les centres ayant l’expérience de cette procédure coûteuse et à haut risque. Il convient d’offrir précocement à certains patients la possibilité de bénéficier d’une telle intervention.
L’éventualité d’une intervention thérapeutique agressive et hautement sophistiquée comme la transplantation souligne bien la nature grave et potentiellement mortelle de la silicose et met l’accent sur le rôle crucial de la prévention primaire. La lutte contre la silicose dépend en dernier recours de la réduction et du contrôle des expositions aux poussières sur le lieu de travail. Ce résultat peut être obtenu grâce à l’application rigoureuse et scrupuleuse des principes fondamentaux d’hygiène industrielle et de prévention technique.
Les mineurs de charbon (houilleurs) sont sujets à un certain nombre de maladies et de troubles respiratoires résultant de leur exposition aux poussières de charbon. Il s’agit de la pneumoconiose du houilleur, de la bronchite chronique et de la broncho-pneumopathie chronique obstructive du mineur. La survenue et la gravité de la maladie dépendent de l’intensité et de la durée de l’exposition aux poussières. La composition particulière des poussières présentes dans les mines de charbon joue également un rôle dans certains processus pathologiques.
Dans les pays développés où la prévalence des maladies respiratoires était autrefois élevée, la réduction de l’empoussièrement grâce à des mesures réglementaires a entraîné une chute de la prévalence depuis les années soixante-dix. Par ailleurs, la diminution importante de la main-d’œuvre minière dans la plupart de ces pays, au cours des dernières décennies, due en partie au progrès technologique et à l’accroissement de la productivité qui en ont résulté, va entraîner une nouvelle diminution de la fréquence globale de ces affections. Les mineurs des pays dans lesquels l’exploitation des ressources minières est un phénomène plus récent et où la lutte contre les poussières est moins élaborée n’ont pas été aussi chanceux. Le problème est encore aggravé par le coût élevé des techniques modernes d’exploitation minière qui contraignent à l’embauche d’une main-d’œuvre importante dont une bonne partie est exposée à un risque élevé de contracter une maladie.
On trouvera ci-après une description de chacune des maladies susceptibles de frapper les mineurs de charbon. Celles qui sont spécifiques à l’extraction du charbon, comme la pneumoconiose du houilleur, sont décrites en détail; la description des autres, comme la broncho-pneumopathie chronique obstructive, sera limitée aux aspects en rapport avec les mineurs de charbon et l’exposition aux poussières.
La pneumoconiose du houilleur (PH) est la plus répandue des affections associées à l’exploitation des mines de charbon. Ce n’est pas une maladie à évolution rapide; il lui faut généralement une dizaine d’années au moins pour se manifester et souvent beaucoup plus longtemps quand l’exposition est peu intense. Aux premiers stades, elle est caractérisée par une rétention excessive de poussières dans les poumons et peut alors laisser apparaître quelques signes et symptômes. Cependant, au fur et à mesure de son évolution, elle entraîne chez le mineur un risque accru de développement d’une fibrose massive progressive (FMP) beaucoup plus grave.
La lésion classique de la PH se présente sous la forme de la macule de charbon, une collection de poussières et de macrophages ayant phagocyté des poussières, située en périphérie des bronchioles. Les macules contiennent peu de collagène et ne sont généralement pas palpables. Elles ont une taille de 1 à 5 mm et s’accompagnent fréquemment d’une augmentation de volume des espaces aériens voisins, appelée emphysème en foyer. Bien que souvent très nombreuses, elles n’apparaissent généralement pas sur les radiographies pulmonaires.
Le nodule de charbon est une autre lésion associée à la PH. Ces lésions de plus grande taille sont palpables et contiennent un mélange de macrophages remplis de poussières, de collagène et de réticuline. La présence de nodules de charbon, avec ou sans nodules silicotiques (voir ci-après), traduit une fibrose pulmonaire et est largement responsable des opacités observées sur les radiographies pulmonaires. Des macronodules, d’une taille de 7 à 20 mm, peuvent s’agglomérer pour donner une fibrose massive progressive (FMP) (voir ci-après) qui peut se développer à partir d’un seul macronodule.
On a trouvé des nodules silicotiques (décrits dans l’article «La silicose») dans une importante minorité de mineurs de fond. Chez la plupart d’entre eux, la seule présence de silice dans les poussières de charbon peut en être la cause, bien que l’exposition à la silice pure dans certaines activités représente incontestablement un facteur de causalité important (chez les foreurs, les conducteurs d’engins souterrains et les poseurs de boulons d’ancrage du toit, par exemple).
Le meilleur indice d’une PH chez un mineur est fourni par la radiographie pulmonaire systématique. Les dépôts de poussières et les réactions tissulaires nodulaires arrêtent les rayons X et donnent des opacités sur les clichés. La densité de ces opacités peut être évaluée systématiquement par une méthode normalisée de description radiologique comme celle élaborée par le BIT et décrite ailleurs dans le présent chapitre. Dans cette méthode, différents clichés pris en incidence postéro-antérieure sont comparés à des clichés types montrant de petites opacités de densité croissante; le cliché est ensuite classé dans l’une des quatre grandes catégories (0, 1, 2, 3) en se référant aux clichés types. On procède aussi à une classification secondaire basée sur l’évaluation par le lecteur de la ressemblance du cliché avec les autres catégories de la Classification du BIT. On note également les autres caractères des opacités: taille, forme et localisation pulmonaire. Certains pays, comme la Chine et le Japon, ont développé des systèmes analogues de description ou d’interprétation systématique des radiographies qui sont parfaitement adaptés à leurs propres besoins.
Classiquement, les petites opacités arrondies sont associées à l’extraction du charbon. Cependant, des données récentes indiquent que des opacités irrégulières peuvent également résulter d’une exposition aux poussières de charbon. Il n’est généralement pas possible de distinguer, sur les radiographies, les opacités de la PH de celles de la silicose. Il semble cependant que les opacités de plus grande taille (de type «r») sont plus souvent en rapport avec une silicose.
Il est important de noter qu’un grand nombre d’anomalies pathologiques liées à la pneumoconiose peuvent être présentes dans les poumons avant que l’on puisse les déceler sur les radiographies pulmonaires systématiques. C’est particulièrement vrai pour les dépôts maculaires, mais ce l’est de moins en moins au fur et à mesure de l’augmentation du nombre et de la taille des nodules. L’emphysème associé peut lui aussi gêner la visualisation des lésions sur les radiographies pulmonaires. La tomodensimétrie (TDM) — surtout la tomodensimétrie en haute résolution (TDM-HR) — peut permettre de visualiser des anomalies qui n’apparaissent pas encore nettement sur les clichés de routine; elle n’est cependant pas indispensable au diagnostic des maladies respiratoires des mineurs au cours des examens de routine et n’est pas indiquée pour leur surveillance médicale.
Le développement d’une PH est souvent cliniquement asymptomatique, bien qu’il traduise une rétention excessive de poussières dans les poumons. Cela ne signifie pas pour autant que l’inhalation de poussières de charbon est dénuée de risque, car on sait parfaitement aujourd’hui que d’autres maladies respiratoires peuvent résulter d’une exposition aux poussières. L’hypertension artérielle pulmonaire est plus fréquente chez les mineurs présentant une obstruction des voies respiratoires associée à une PH. De plus, une fois qu’une PH s’est développée, elle s’aggrave généralement, sauf en cas d’arrêt de l’exposition aux poussières; même dans ce cas, il arrive que la maladie continue d’évoluer. Elle peut également entraîner chez les mineurs un risque accru d’apparition d’une FMP cliniquement menaçante, à laquelle s’attache la probabilité d’une incapacité fonctionnelle ultérieure, d’une invalidité ou d’une mort prématurée.
L’apparition de la toute première anomalie de la PH, la macule de charbon, correspond aux effets du dépôt et de l’accumulation de poussières. Le stade suivant, à savoir le développement des nodules, résulte de la réaction inflammatoire et fibrosante des poumons aux poussières. On a beaucoup discuté du rôle des poussières siliceuses et non siliceuses dans cette réaction. D’une part, on sait que la poussière siliceuse est beaucoup plus toxique que la poussière de charbon. Mais, d’autre part, les études épidémiologiques ne sont pas parvenues à mettre en évidence une relation entre l’exposition à la silice et la prévalence ou l’incidence de la PH. En fait, il semble qu’il existe une relation pratiquement inverse: la fréquence de la maladie tend à être plus élevée là où les concentrations de silice sont plus faibles (par exemple, dans les mines d’anthracite). L’étude des caractéristiques des particules a récemment permis d’expliquer en partie ce paradoxe. Elle a montré en effet que ce n’est pas seulement la quantité de silice présente dans la poussière (mesurée classiquement par spectrométrie infrarouge ou diffraction des rayons X), mais aussi la biodisponibilité de la surface des particules de silice qui peuvent être en rapport avec la toxicité. Ainsi, un revêtement argileux (occlusion) peut entraîner des modifications importantes. Un autre facteur important en cours d’investigation est la charge de surface sous la forme de radicaux libres et les effets comparatifs des poussières siliceuses «fraîchement concassées» et «vieillies».
La prévalence de la PH chez les mineurs de fond varie avec la nature de leur activité, la durée du travail dans la mine et l’âge. Une étude des mineurs de charbon aux Etats-Unis a révélé qu’entre 1970 et 1972 25 à 40% environ d’entre eux présentaient de petites opacités arrondies de catégorie 1 ou supérieure après trente ans de travail ou plus dans les mines. Cette prévalence reflète l’exposition à des concentrations de poussières respirables égales ou supérieures à 6 mg/m3 chez les mineurs du front de taille avant cette époque. L’introduction d’une limite de 3 mg/m3 en 1969, ramenée à 2 mg/m3 en 1972, a entraîné une diminution de près de moitié de la prévalence de la maladie. Des réductions ont été notées par ailleurs, par exemple au Royaume-Uni et en Australie, à la suite des progrès enregistrés dans la lutte contre les poussières. Ces gains ont malheureusement été contrebalancés par des augmentations transitoires de la prévalence dans d’autres pays.
Un certain nombre d’études ont mis en évidence une relation exposition-réponse pour la prévalence ou l’incidence de la PH et l’exposition aux poussières. Elles ont montré que la principale variable de l’exposition aux poussières était l’exposition aux poussières mixtes que l’on rencontre dans les mines. Des études approfondies menées par des chercheurs britanniques ne sont pas parvenues à révéler une influence majeure de l’exposition à la silice au-dessous d’une teneur en silice inférieure à 5% environ. La qualité du charbon (teneur en carbone) est un autre élément pronostique important de la PH. Des études menées aux Etats-Unis, au Royaume-Uni, en Allemagne et dans d’autres pays ont nettement indiqué que la prévalence et l’incidence de la PH augmentent fortement avec la qualité du charbon et qu’elles sont significativement plus élevées dans les mines d’anthracite (charbon de qualité supérieure). Aucune autre variable environnementale n’exerce d’effet important sur le développement de la PH. L’âge des mineurs semble influer sur l’apparition de la maladie, le risque paraissant plus élevé chez les mineurs âgés. On ignore cependant si cela signifie que les mineurs âgés sont plus sensibles, s’il s’agit d’un effet du temps de résidence, ou si ce n’est qu’un simple artefact (l’effet de l’âge pourrait refléter une sous-estimation de l’exposition chez les mineurs âgés, par exemple). Le tabagisme ne semble pas augmenter le risque de survenue d’une PH.
D’autres études dans lesquelles des mineurs ont été suivis radiologiquement tous les cinq ans montrent que le risque de développement d’une FMP sur une période de cinq ans est nettement lié à la catégorie de PH déterminée sur la première radiographie pulmonaire. Comme le risque dans la catégorie 2 est beaucoup plus grand que dans la catégorie 1, il a paru sensé à une certaine époque d’empêcher autant que possible les mineurs de passer dans la catégorie 2. Cependant, dans la plupart des mines, les mineurs atteints d’une PH de catégorie 1 sont beaucoup plus nombreux que ceux présentant une PH de catégorie 2. Le risque moindre lié à la catégorie 1 par rapport à la catégorie 2 est donc contrebalancé par le nombre supérieur de mineurs de la catégorie 1. On voit donc que la prévention de toutes les catégories de pneumoconioses est indispensable.
Les mineurs, en tant que population, présentent un risque accru de mortalité à la suite d’une maladie respiratoire non maligne; il est certain que la mortalité, chez les mineurs atteints de PH, est légèrement augmentée par rapport à celle des mineurs sains du même âge. L’augmentation de la mortalité imputable à la PH est cependant moindre que celle observée chez les mineurs atteints de FMP (voir ci-après).
La seule protection véritable contre la PH est la réduction de l’exposition aux poussières, et, cela, dans toute la mesure du possible grâce à des techniques de suppression des poussières (ventilation, aspiration localisée, procédés par voie humide) plutôt que par le port d’appareils de protection respiratoire ou des mesures d’ordre organisationnel comme la rotation des travailleurs. On sait désormais que les mesures réglementaires instaurées dans les années soixante-dix dans certains pays pour réduire l’empoussièrement ont entraîné une importante diminution des cas de PH. Le transfert des travailleurs présentant des signes précoces de PH à un poste où l’empoussièrement est moins important est une mesure de prudence, mais on n’a pas pu démontrer dans les faits qu’elle ait contribué efficacement à la prévention de l’évolution de la maladie. C’est pourquoi la lutte contre les poussières doit rester la principale méthode de prévention de la maladie.
A une politique de prévention portant sur la réduction énergique et continue de l’empoussièrement, on peut adjoindre une surveillance médicale des mineurs. S’il s’avère que ceux-ci développent une maladie due aux poussières, les mesures visant à limiter leur exposition devraient être renforcées sur le lieu de travail; les mineurs atteints devraient être mutés dans des zones peu empoussiérées de la mine.
Bien que l’on ait essayé plusieurs types de traitement — parmi lesquels on peut citer l’inhalation de poudre d’aluminium et l’administration de tétrandrine — on ne connaît aucun traitement capable d’inverser efficacement ou de ralentir le processus de fibrose pulmonaire. A l’heure actuelle, surtout en Chine, mais aussi dans d’autres pays, le lavage pulmonaire total a été tenté afin de réduire la charge totale de poussières contenues dans les poumons. Bien que cette technique puisse entraîner une diminution importante de la quantité de poussières, on connaît mal pour l’instant ses risques, ses avantages et son rôle thérapeutique.
En tout état de cause, le traitement devrait être orienté vers la prévention des complications, l’optimisation des performances fonctionnelles et l’atténuation des troubles, que ceux-ci soient dus à une PH ou à une autre maladie respiratoire concomitante. En règle générale, les mineurs atteints d’une maladie respiratoire induite par la poussière devraient évaluer leur degré actuel d’exposition à la poussière et utiliser les ressources offertes par le gouvernement et les organisations syndicales pour trouver une solution permettant de réduire toutes les expositions respiratoires nocives. Chez les mineurs qui fument, l’arrêt du tabac est la première mesure à prendre dans le cadre de la limitation individuelle de l’exposition. On a proposé de prévenir les complications infectieuses des pneumopathies chroniques par la vaccination antipneumococcique et la vaccination antigrippale annuelle. On préconise également un diagnostic précoce en cas de symptômes évoquant une infection respiratoire, en s’attachant tout particulièrement à la détection d’une maladie mycobactérienne. Les traitements de la bronchite aiguë, du bronchospasme et de l’insuffisance cardiaque congestive chez les mineurs sont les mêmes que chez les patients indemnes de toute pathologie liée aux poussières.
La FMP, parfois appelée pneumoconiose compliquée, est diagnostiquée en cas d’apparition d’une ou de plusieurs lésions fibreuses de grande taille (dont la définition dépend du mode de détection) au sein d’un seul poumon ou des deux. Comme son nom l’indique, la FMP s’aggrave souvent avec le temps, même en l’absence de toute nouvelle exposition aux poussières. Elle peut entraîner souvent une invalidité et une mort prématurée.
Les lésions en cas de FMP peuvent être unilatérales ou bilatérales; elles se situent le plus souvent dans les lobes supérieurs et moyens des poumons. Ces lésions sont formées de collagène, de réticuline, de poussières de charbon et de macrophages chargés de poussières, tandis que leur centre peut contenir un liquide noir et parfois une caverne. D’après les normes anatomopathologiques américaines, les lésions des pièces opératoires ou d’autopsie doivent avoir une taille de 2 cm ou plus pour que l’on puisse parler de FMP.
On considère que les grandes opacités (10 mm) observées sur les radiographies, associées à des antécédents de forte exposition aux poussières de charbon, traduisent une FMP. Il convient cependant d’envisager d’autres affections: cancer du poumon, tuberculose et granulomes. Ces opacités s’observent généralement sur un arrière-plan de petites opacités, encore que l’on ait parfois noté le développement d’une FMP à partir d’une densité d’opacités de catégorie 0 sur une période de cinq ans.
Il convient d’évaluer soigneusement les possibilités diagnostiques dans le cas d’un mineur présentant de grandes opacités pulmonaires. Les difficultés diagnostiques sont minimes chez les mineurs cliniquement stables porteurs de lésions bilatérales (avec répartition caractéristique dans les lobes supérieurs) et ayant une PH préexistante non compliquée. En revanche, les mineurs présentant des troubles d’évolution progressive, des facteurs de risque relatifs à d’autres pathologies (tuberculose, par exemple) ou des manifestations cliniques atypiques devraient faire l’objet d’une investigation approfondie avant qu’on puisse conclure à une FMP.
Une dyspnée et d’autres symptômes respiratoires accompagnent souvent la FMP, mais ils ne sont pas forcément imputables à la maladie elle-même. L’insuffisance cardiaque congestive (secondaire à l’hypertension artérielle pulmonaire et au cœur pulmonaire) est une complication relativement courante.
En dépit des nombreuses recherches effectuées, la cause réelle du développement d’une FMP reste mal connue. Au fil des années, diverses hypothèses ont été proposées, mais aucune d’entre elles n’est vraiment satisfaisante. C’est ainsi que l’on a souvent attribué un rôle à la tuberculose, laquelle est en effet fréquemment présente chez les mineurs atteints de FMP, en particulier dans les pays en développement. On a cependant constaté que la FMP apparaissait chez les mineurs ne présentant pas de signes de tuberculose et l’on n’a pas noté de réactivité élevée à la tuberculine chez les mineurs atteints de pneumoconiose. Malgré les recherches, il n’a pas été possible d’obtenir une preuve valable de l’intervention du système immunitaire dans le développement de la FMP.
Comme pour la PH, la fréquence de la FMP a diminué dans les pays ayant édicté des réglementations et adopté des programmes stricts de lutte contre les poussières. Une étude portant sur des mineurs américains a révélé que 2% environ des mineurs de charbon de fond développaient une FMP après trente ans de travail ou plus (ce chiffre pourrait avoir été faussé par le départ de certains mineurs malades).
Les enquêtes relatives à la relation exposition-réponse dans le cas de la FMP ont montré que l’exposition aux poussières de charbon, la catégorie de la PH, la qualité du charbon et l’âge sont les principaux facteurs déterminants du développement de la maladie. Comme pour la PH, les études épidémiologiques ont montré l’absence d’effet majeur des poussières de silice. On a récemment découvert que, contrairement à ce que l’on croyait à une époque, la FMP ne se développe pas exclusivement sur un arrière-fond de petites opacités liées à une PH. Les mineurs dont les premières radiographies montrent une PH de catégorie 0 peuvent développer une FMP en cinq ans, le risque augmentant avec l’exposition cumulée aux poussières. Une FMP peut aussi apparaître après l’arrêt de l’exposition aux poussières.
La FMP entraîne une mortalité prématurée, le pronostic s’aggravant avec le stade de la maladie. Une étude récente a montré que chez les mineurs ayant une PH de catégorie C, le taux de survie était réduit des trois quarts en vingt-deux ans par rapport aux mineurs indemnes de toute pneumoconiose. Cet effet s’est vérifié dans toutes les tranches d’âge.
La prévention de l’exposition aux poussières est la seule façon de se prémunir contre la FMP. Comme le risque de FMP augmente fortement avec la catégorie de PH simple, il est possible de définir une stratégie de prévention secondaire de la FMP consistant à effectuer périodiquement des radiographies pulmonaires et à mettre fin ou à réduire l’exposition en cas de détection d’une PH simple. Bien que cette approche semble valable et ait été adoptée dans certaines juridictions, son efficacité n’a pas été validée systématiquement.
On ne connaît pas de traitement de la FMP. Les soins médicaux devraient viser l’amélioration de l’état clinique et des broncho-pneumopathies associées, tout en assurant une protection contre les complications infectieuses. Bien que la stabilité fonctionnelle puisse être plus difficile à maintenir chez les patients atteints de FMP, pour le reste, le traitement est le même que celui de la PH simple.
On dispose maintenant d’arguments cohérents et probants en faveur de l’existence d’une relation entre l’altération de la fonction pulmonaire et l’exposition aux poussières. Différents travaux menés dans plusieurs pays ont étudié l’influence de l’exposition aux poussières sur les valeurs absolues ou les variations transitoires des mesures de la fonction ventilatoire, telles que le volume expiratoire maximal seconde (VEMS), la capacité vitale (CV) et les débits expiratoires. Toutes ont montré que l’exposition aux poussières entraînait une altération de la fonction respiratoire; des résultats analogues ont été mis en évidence dans plusieurs études britanniques et américaines. Elle indiquent qu’en un an l’exposition aux poussières sur le front de taille du charbon induit en moyenne une altération fonctionnelle respiratoire équivalente à la consommation d’un demi-paquet de cigarettes par jour. Ces études ont aussi montré que les effets des poussières étaient variables et que, chez un mineur donné, ils pouvaient être comparables à ceux de la fumée de cigarette ou plus marqués, en particulier en cas d’antécédents d’exposition plus importante aux poussières.
Les effets de l’exposition aux poussières ont été mis en évidence tant chez des sujets n’ayant jamais fumé que chez des fumeurs. Rien n’indique que le tabagisme aggrave les effets de l’exposition aux poussières. Au contraire, les études ont généralement montré que l’effet était légèrement moins marqué chez les fumeurs, ce qui pourrait être dû à la sélection de travailleurs sains. Il est important de noter que la relation entre l’exposition aux poussières et l’altération ventilatoire semble être indépendante de la pneumoconiose; cela veut dire que la présence d’une pneumoconiose n’est pas indispensable à une altération de la fonction pulmonaire. En revanche, il semble plutôt que l’inhalation de poussières puisse agir de différentes façons, aboutissant à une pneumoconiose chez certains mineurs, à un syndrome obstructif chez d’autres et à de nombreux autres troubles chez d’autres encore. A la différence des mineurs atteints de PH isolée, ceux qui présentent des symptômes respiratoires ont une fonction pulmonaire significativement altérée après pondération en fonction de l’âge, du tabagisme, de l’exposition aux poussières et d’autres facteurs.
Des travaux récents sur l’altération de la fonction ventilatoire comportaient l’exploration de modifications longitudinales. Les résultats montrent qu’il peut y avoir une tendance non linéaire à l’altération avec le temps chez les nouveaux mineurs, une importante altération initiale étant suivie d’une altération plus modérée en cas de poursuite de l’exposition. De plus, il s’avère que les mineurs qui réagissent aux poussières devraient, s’ils le peuvent, se soustraire à toute exposition intense aux poussières.
Les symptômes respiratoires, tels que la toux productive, sont une conséquence fréquente du travail dans les mines de charbon, la plupart des études faisant ressortir une prévalence accrue par rapport aux populations témoins non exposées. En outre, la prévalence et l’incidence des symptômes respiratoires augmentent avec l’exposition cumulée aux poussières, compte tenu de l’âge et du tabagisme. La présence de symptômes semble être associée à une altération de la fonction pulmonaire plus grave que celle résultant de l’exposition aux poussières ou d’autres causes présumées, ce qui suggère que l’exposition aux poussières peut contribuer à l’apparition de certains processus pathologiques qui évoluent ensuite indépendamment de toute nouvelle exposition. Une relation entre la taille des ganglions péribronchiques et l’exposition aux poussières a été mise en évidence par l’anatomopathologie. On a constaté que la mortalité par bronchite et emphysème augmentait avec l’accroissement de l’exposition cumulée aux poussières.
Les études anatomopathologiques ont constamment montré une augmentation des lésions emphysémateuses chez les mineurs de charbon par rapport aux groupes témoins. De plus, on a noté que l’importance de l’emphysème était liée à la quantité de poussières dans les poumons et aux signes pathologiques de pneumoconiose. Il est également important de noter que la présence d’un emphysème est liée à l’exposition aux poussières et au pourcentage du VEMS théorique. Ces constatations concordent avec l’hypothèse selon laquelle l’exposition aux poussières peut induire un emphysème invalidant.
La forme d’emphysème la plus nettement associée à l’extraction du charbon est l’emphysème en foyer. Il consiste en des zones de distension des espaces aériens, d’une taille de 1 à 2 mm, à proximité des macules de poussières péribronchiolaires. On considère actuellement que l’emphysème résulte d’une destruction tissulaire plutôt que d’une distension ou d’une dilatation. En dehors de l’emphysème en foyer, il est certain que l’emphysème centro-acinaire a une origine professionnelle et que l’emphysème total (c’est-à-dire l’ensemble des divers types) présente une corrélation avec la durée du travail dans la mine, chez les sujets qui n’ont jamais fumé comme chez les fumeurs. Rien ne suggère une potentialisation de la relation exposition aux poussières-emphysème par le tabagisme. Par contre, certains faits évoquent une relation inverse entre la teneur en silice des poumons et la présence d’un emphysème.
La question de l’emphysème a fait l’objet de nombreuses controverses, certains affirmant que les biais de sélection et le tabagisme compliquent l’interprétation des études anatomopathologiques. Certains spécialistes considèrent que l’emphysème en foyer n’a qu’un retentissement minime sur la fonction pulmonaire. Les études anatomopathologiques entreprises depuis les années quatre-vingt ont tenu compte des critiques initiales et ont révélé que l’effet de l’exposition aux poussières peut être plus important pour la santé des mineurs qu’on ne le pensait jusque-là. Cette opinion est corroborée par la découverte récente d’une relation entre mortalité par bronchite et emphysème et exposition cumulée aux poussières.
Bien qu’associée surtout à des activités industrielles autres que l’extraction du charbon, la silicose peut aussi se produire chez les mineurs de charbon. Dans les chantiers souterrains, on l’observe très fréquemment chez certains travailleurs exerçant des tâches comportant classiquement une exposition à la silice pure. Il s’agit des mineurs qui percent des trous d’ancrage dans des toits souvent constitués de grès ou d’autres minéraux à teneur élevée en silice, des conducteurs d’engins mécanisés ou de convois exposés aux poussières générées par le sable placé sur les voies pour faciliter la traction, ainsi que des foreurs qui travaillent à l’avancement. Dans les mines de charbon des Etats-Unis exploitées à ciel ouvert, les foreurs sont exposés à un risque particulier, certains d’entre eux développant une silicose aiguë après quelques années d’exposition seulement. Des observations anatomopathologiques, comme on le verra ci-après, suggèrent que la silicose ne se limite pas aux mineurs de charbon exécutant les tâches énumérées plus haut, mais qu’elle peut affecter beaucoup d’autres catégories de travailleurs employés dans les mines de charbon.
Les nodules silicotiques observés chez les mineurs de charbon sont de même nature que ceux observés ailleurs; ils sont formés de volutes de collagène et de réticuline. Une importante étude sur autopsies a révélé que 13% environ des mineurs de charbon présentaient des nodules silicotiques pulmonaires. Bien qu’une activité (celle des conducteurs d’engins) ait été caractérisée par une prévalence beaucoup plus élevée des nodules silicotiques (25%), cette prévalence variait peu chez les mineurs occupant d’autres postes, ce qui paraît incriminer la silice présente dans les poussières mixtes que l’on rencontre dans les mines.
Il est difficile de bien distinguer, sur une radiographie, la silicose de la pneumoconiose du houilleur. Il semble cependant que les plus grandes des petites opacités (type «r») correspondent à une silicose.
La pneumoconiose rhumatoïde, dont une variante s’appelle syndrome de Caplan, désigne une maladie touchant des travailleurs exposés aux poussières dont les radiographies présentent de multiples opacités de grande taille. Sur le plan anatomopathologique, ces lésions ressemblent plutôt à des nodules rhumatoïdes qu’à des lésions de FMP et apparaissent souvent en peu de temps. On note le plus souvent la présence d’une arthrite évolutive et d’un facteur rhumatoïde circulant, sans toutefois que cette présence soit généralisée.
Les mineurs de charbon peuvent être exposés à un certain nombre de substances qui sont des agents cancérogènes potentiels. Parmi celles-ci, on note la silice et le benzo(a)pyrène. Rien n’atteste cependant formellement l’existence d’un nombre accru de décès par cancer du poumon chez les mineurs de charbon. On peut l’expliquer par le fait qu’on leur interdit de fumer en raison des risques d’incendie et d’explosion. Cependant, le fait qu’aucune relation exposition-réponse n’ait pu être mise en évidence entre le cancer du poumon et l’exposition aux poussières suggère que la poussière de charbon n’est pas une cause majeure de cancer du poumon dans l’industrie charbonnière.
L’Organisation mondiale de la santé (OMS) a recommandé une «limite provisoire d’exposition basée sur des critères sanitaires» fixée à 0,54 mg/m3 pour les poussières respirables des mines de charbon (contenant moins de 6% de particules respirables de quartz). L’OMS a pris pour critère un risque de 2‰ de contracter une FMP au cours de la vie professionnelle et recommande de tenir compte des facteurs environnementaux (qualité du charbon, pourcentage de quartz et taille des particules) pour fixer les limites d’exposition.
Dans les principaux pays producteurs de charbon, les limites actuelles sont basées sur la seule poussière de charbon (par exemple, 3,8 mg/m3 au Royaume-Uni; 5 mg/m3 en Australie et au Canada) ou sur le mélange charbon-silice (comme aux Etats-Unis: 2 mg/m3 quand la teneur en quartz est égale ou inférieure à 5%, ou 10 mg/m3/pour cent de SiO2, ou encore en Allemagne: (4 mg/m3 quand la teneur en quartz est égale ou inférieure à 5%, et 0,15 mg/m3 dans les autres cas), ou encore sur la limitation de la teneur en quartz pur (par exemple, la Pologne, avec une limite de 0,05 mg/m3).
Le terme amiante est utilisé pour décrire un groupe de minéraux fibreux naturels très répandus dans le monde sous forme de gisements de minerais ou d’affleurements rocheux. L’exploitation des propriétés de résistance à la chaleur et de souplesse de ces minéraux est très ancienne. Au IIIe siècle avant J.-C., par exemple, l’amiante servait à renforcer les poteries d’argile en Finlande. Les linceuls utilisés pour envelopper la dépouille mortelle des personnages célèbres étaient tissés en fibres d’amiante. Marco Polo, au retour de son voyage en Chine, a décrit un matériau magique qui permettrait de fabriquer des vêtements ininflammables. Au début du XIXe siècle, on dénombrait des gisements d’amiante dans plusieurs régions du monde (notamment les monts Oural, le nord de l’Italie, d’autres pays méditerranéens, l’Afrique du Sud et le Canada), mais leur exploitation commerciale n’a réellement commencé qu’à partir de 1850. A cette époque, la révolution industrielle non seulement créait la demande (pour l’isolation des machines à vapeur, par exemple), mais encourageait également la production de fibres d’amiante en permettant la mécanisation du processus d’extraction à partir de la roche mère. L’industrie moderne de l’amiante est née en Italie et au Royaume-Uni après 1860; elle a pris son essor au Québec (Canada) dans les années mille huit cent quatre-vingt avec l’exploitation d’importants gisements de chrysotile (amiante blanc). L’exploitation des grands gisements de chrysotile situés dans les monts Oural est restée limitée jusque dans les années vingt. A l’époque, le chrysotile entrait surtout dans la fabrication des tissus et des feutres, car ses fibres sont longues et fines. Au début du siècle, d’autres types de gisements ont été découverts et exploités comme les gisements de crocidolite (amiante bleu) (dans la partie nord-ouest de la province du Cap en Afrique du Sud; cette fibre résiste mieux à l’eau que le chrysotile et est mieux adaptée à une utilisation marine) ou les gisements d’amosite (amiante brun) (également en Afrique du Sud). Plus récemment, des gisements d’anthophyllite ont été exploités en Finlande de 1918 à 1966 (seule source commerciale importante de cette fibre), ainsi que des gisements de crocidolite en Australie occidentale, à Wittenoom, de 1937 à 1966.
Les amiantes sont classés en deux groupes: le groupe des serpentines, qui inclut le chrysotile, et le groupe des amphiboles, qui comprend la crocidolite, la trémolite, l’amosite et l’anthophyllite (voir figure 10.17). Dans la plupart des cas, la composition minérale des gisements est hétérogène, comme la majorité des formes commercialisées (Skinner, Roos et Frondel, 1988). Le chrysotile et les amiantes amphiboles diffèrent par leur structure cristallographique, ainsi que par leurs caractéristiques chimiques et de surface. Les propriétés physiques de leurs fibres sont également un autre paramètre de différenciation et sont exprimées habituellement par le rapport (ou l’aspect) longueur/diamètre. Enfin, les amiantes se distinguent selon le type d’utilisation commerciale et la classe à laquelle ils appartiennent. Ces différences se répercutent sur leur puissance biologique (les aspects en seront abordés dans les sections qui suivent).

La croissance de la production industrielle, illustrée dans la figure 10.18, était assez faible au début du siècle. A titre d’exemple, la production canadienne ne dépassait pas 91 000 tonnes métriques par an jusqu’en 1911 et 182 000 tonnes par an jusqu’en 1923. Juste après la première guerre mondiale, la production est restée constante, pour augmenter considérablement au moment de la seconde guerre mondiale. Par la suite, la production n’a cessé de croître (en particulier pendant la guerre froide) pour atteindre son maximum en 1976, avec 5 178 000 tonnes par an (Selikoff et Lee, 1978). Le déclin qui a suivi est principalement lié à la mise en évidence des effets pathologiques de l’amiante, sujet de préoccupation de plus en plus présent dans les pays d’Amérique du Nord et d’Europe. La production s’est alors maintenue aux environs de 3 600 000 tonnes par an jusqu’en 1986, pour continuer de diminuer ensuite dans les années quatre-vingt-dix. Durant les années quatre-vingt, le profil d’utilisation et les sources de fibres ont également changé: la demande a diminué en Europe et en Amérique du Nord avec l’introduction de matériaux de substitution dans diverses applications, tandis qu’elle a augmenté sur les continents africain, asiatique et sud-américain pour répondre à la demande croissante de matériaux bon marché et durables pour les travaux de construction et les réseaux d’alimentation en eau. En 1981, la Russie est devenue le premier producteur mondial, tandis que l’exploitation industrielle de gisements importants se développait en Chine et au Brésil. En 1980, on estimait que plus de 90 millions de tonnes d’amiante étaient extraites dans le monde, constituées à 90% de chrysotile dont 75% environ provenaient de quatre régions minières situées au Québec, en Afrique du Sud et dans le centre et le sud des monts Oural. Deux à 3% de la production mondiale étaient composés de crocidolite provenant du nord de la province du Cap et de l’Australie occidentale, tandis que 2 à 3% étaient constitués d’amosite et provenaient de la région orientale du Transvaal, en Afrique du Sud (Skinner, Ross et Frondel, 1988).
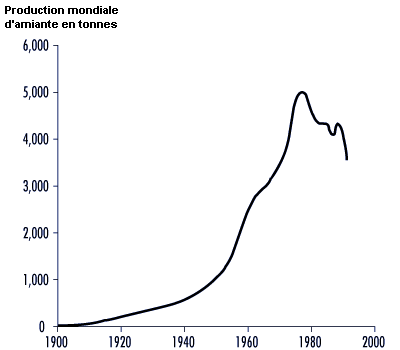
Comme la silice, l’amiante peut déclencher des réactions cicatricielles dans tous les tissus biologiques, qu’ils soient d’origine humaine ou animale. En outre, l’exposition à l’amiante provoque des réactions malignes, ce qui représente un sujet de préoccupation supplémentaire pour la santé humaine, mais aussi un nouveau défi scientifique en vue d’élucider les mécanismes de ses effets pathologiques. La première forme de maladie identifiée comme étant liée à l’amiante, caractérisée par une fibrose pulmonaire interstitielle diffuse, plus tard appelée asbestose, a été décrite au Royaume-Uni au début du siècle. Les premières observations de cancer pulmonaire associé à l’asbestose remontent aux années trente, mais la mise en évidence scientifique du rôle cancérogène de l’amiante est relativement récente. En 1960, l’apparition de mésothéliomes (cancers assez rares) chez un groupe de trente-trois personnes travaillant ou vivant dans la région minière de la partie nord-ouest de la province du Cap a permis de mettre en évidence l’association qui existe entre l’exposition à l’amiante et ce type de cancer; celui-ci se manifeste par un envahissement de la plèvre, c’est-à-dire de la membrane couvrant le poumon et bordant la paroi thoracique (Wagner, 1998). Dans les années soixante et soixante-dix, c’est pour lutter contre l’asbestose que des contrôles d’empoussièrement ont été instaurés et appliqués de façon de plus en plus rigoureuse dans de nombreux pays industriels. Le résultat en fut la réduction de la fréquence de cette affection; c’est à ce moment-là que l’atteinte de la plèvre révéla son importance et éveilla l’attention des médecins du fait qu’elle représentait la principale manifestation pathologique chez les travailleurs exposés à l’amiante. Le tableau 10.16 répertorie les pathologies reconnues actuellement comme imputables à l’amiante. Les maladies inscrites en caractères gras sont celles qui sont les plus fréquentes et dont le rapport de causalité a été le mieux établi (voir notes au bas du tableau 10.16). Les paragraphes qui suivent décrivent ces différentes pathologies.
|
Pathologie |
Organe(s) atteint(s) |
Types de maladies |
|
Non maligne |
Poumons |
Asbestose (fibrose interstitielle diffuse) |
|
Plèvre |
Plaques pleurales |
|
|
|
Peau |
Indurations cornées4 |
|
Maligne |
Poumons |
Cancer pulmonaire (tous types cellulaires) |
|
Plèvre |
Mésothéliome de la plèvre |
|
|
Autres cavités atteintes de mésothéliome |
Mésothéliome du péritoine, péricarde et scrotum (par ordre décroissant de fréquence) |
|
|
|
Tube digestif5 |
Cancer de l�estomac, de l�œsophage, du côlon, du rectum |
|
|
Autres6 |
Ovaire, vésicule biliaire, canaux biliaires, pancréas, reins |
1 Les pathologies indiquées en gras sont les plus fréquentes; ce sont aussi celles pour lesquelles un lien causal est bien établi ou généralement admis. 2 On pense que la fibrose des petites voies aériennes du poumon (intéressant plus particulièrement les bronchioles terminales et respiratoires) représente la première réponse du parenchyme pulmonaire à l�amiante (Wright et coll., 1992) qui évoluera vers une asbestose déclarée si l�exposition se prolonge ou est importante. Dans le cas contraire, la réponse pulmonaire peut rester circonscrite à ces régions (Becklake, 1991). 3 Les maladies chroniques des voies aériennes incluent la bronchite, la bronchopneumopathie chronique obstructive et l�emphysème. Elles peuvent toutes être rapportées à une exposition professionnelle à des irritants bronchiques. La relation de cause à effet est développée dans l�article �Occupational exposure and chronic airways disease� (Becklake, 1992). 4 En relation avec une manipulation directe de l�amiante. D�intérêt historique plutôt qu�actuel. 5 Toutes les études n�ont pas donné les mêmes résultats (Doll et Peto, 1987). La plupart des risques importants ont été décrits dans une cohorte de plus de 17 000 Américains et Canadiens travaillant dans le domaine de l�isolation à l�amiante (Seidman et Selikoff, 1990), suivis du 1er janvier 1967 au 31 décembre 1986, chez qui l�exposition avait été particulièrement forte.
Sources: Becklake, 1991; Becklake, 1992; Becklake, 1994; Doll et Peto, 1987; Seidman et Selikoff, 1990; Wright et coll., 1992.
Les principales sources d’amiante, les types de produits à base d’amiante et leurs utilisations les plus importantes sont présentés dans le tableau 10.17. Bien que nécessairement incomplet, ce tableau montre que:
|
Type de fibre |
Situation des principaux gisements |
Produits commerciaux ou utilisations |
|
Actinolite |
Contamine l�amosite et, plus rarement, les gisements de chrysotile, de talc et de vermiculite |
Absence d�exploitation commerciale en règle générale |
|
Amosite |
Afrique du Sud (nord du Transvaal)1 |
Utilisé principalement dans la fabrication de matériaux de couverture et d�isolation thermique ainsi que de l�amiante-ciment, surtout aux Etats-Unis2, mais également dans la plupart des produits répertoriés dans la rubrique �chrysotile� |
|
Anthophyllite |
Finlande1 |
Charge dans les industries du caoutchouc et des plastiques et dans l�industrie chimique |
|
Chrysotile |
Russie, Canada (Québec, Colombie-Britannique, Terre-Neuve), Chine (province du Szu-ch�uan ); pays méditerranéens (Italie, Grèce, Corse, Chypre); Afrique australe (Afrique du Sud, Zimbabwe, Swaziland); Brésil; gisements moins importants aux Etats-Unis (Vermont, Arizona, Californie) et au Japon |
Matériaux de construction (tuiles, bardeaux, plaques, gouttières, citernes, toitures, etc.) |
|
Crocidolite |
Afrique du Sud (nord-ouest de la province du Cap, est du Transvaal), Australie-Occidentale1 |
Utilisé principalement en association avec le ciment (en particulier pour les canalisations sous pression), mais également dans la plupart des produits cités ci-dessus |
|
Trémolite |
Italie, Corée et certaines îles du Pacifique; faible activité minière en Turquie et en Chine; contamine les roches encaissantes dans certaines mines d�amiante, de fer, de talc et de vermiculite; également rencontré dans les sols agricoles de la péninsule des Balkans et de la Turquie |
Utilisé comme charge dans le talc; n�est pas toujours éliminé lors du traitement du minerai, si bien qu�il peut apparaître dans les produits finis |
1 Cette liste n�a pas la prétention d�être exhaustive. Le lecteur est invité à consulter les sources citées, ainsi que d�autres chapitres de la présente Encyclopédie. 2 Usage abandonné à l�heure actuelle.
Sources: Asbestos Institute, 1995; Browne, 1994; Liddell et Miller, 1991; Selikoff et Lee, 1978; Skinner, Roos et Frondel, 1988.
On dénombre plus de 3 000 applications différentes de l’amiante, ce qui lui a valu son qualificatif de «minéral magique» dans les années soixante. En 1953, une industrie utilisait l’amiante sous forme brute dans plus de cinquante domaines, sans parler de son utilisation pour la fabrication des produits mentionnés dans le tableau 10.17. En 1972, la consommation d’amiante aux Etats-Unis était répartie de la façon suivante: construction (42%); garnitures de freins et autres systèmes de friction, feutres, emballages et joints (20%); revêtements pour sols (11%); papier (9%); isolation et textiles (3%); autres utilisations (15%) (Selikoff et Lee, 1978). En 1995, la répartition mondiale des utilisations industrielles de l’amiante s’était considérablement modifiée et présentait le profil suivant: amiante-ciment (84%); garnitures de freins et autres systèmes de friction (10%); textiles (3%); joints d’étanchéité thermique (2%); autres utilisations (1%) (Asbestos Institute, 1995).
L’exposition professionnelle, en particulier dans les pays industriels, a toujours été et reste la source la plus probable de l’exposition humaine (voir tableau 10.17 ainsi que les références bibliographiques et d’autres chapitres de la présente Encyclopédie qui contiennent des compléments d’information). Toutefois, des modifications ont été apportées aux processus de fabrication pour diminuer les dégagements de poussières dans les ateliers (Browne 1994; Selikoff et Lee, 1978). Dans les pays producteurs d’amiante, l’extraction des fibres a généralement lieu sur le carreau de la mine. La plupart des mines de chrysotile sont à ciel ouvert, alors que les mines d’amphiboles font généralement intervenir des méthodes d’extraction souterraine, générant plus de poussières. Pour être extraites de la roche mère, les fibres sont broyées, puis passées au crible. Ces techniques entraînaient un empoussiérage important jusqu’à l’introduction de procédés humides ou à la mise en place d’enceintes étanches au cours des années cinquante et soixante. La manipulation des déchets constituait également une autre source d’exposition humaine, tout comme le transport des sacs d’amiante, qu’il soit assuré par voie routière, ferroviaire ou maritime. Ce risque d’exposition a considérablement diminué depuis l’introduction de sacs hermétiques et l’utilisation de conteneurs scellés.
Les travailleurs devaient utiliser l’amiante brut pour tous les travaux de calfeutrage et de calorifugeage, en particulier dans l’industrie ferroviaire, l’industrie du bâtiment (pour isoler les murs, les plafonds et les conduits d’aération) et la construction navale (pour isoler les ponts et les cloisons). Certaines de ces applications ont été supprimées progressivement, voire interdites. Dans la fabrication d’amiante-ciment, l’exposition a lieu au moment de la réception et de l’ouverture des sacs d’amiante brut, du déversement des fibres dans les trémies des mélangeurs, ainsi que lors de l’usinage des produits finis et de l’évacuation des déchets. Pour la fabrication des panneaux de revêtement de sols en vinyle, l’amiante a été utilisé, en combinaison avec des résines organiques, comme agent de renforcement et comme charge. En Europe et aux Etats-Unis, il est désormais largement remplacé par les fibres organiques. Dans la fabrication des fils et des textiles, l’exposition aux fibres d’amiante a lieu lors de la réception, de la préparation, du mélange, du cardage, du filage, du tissage et du calandrage; ces opérations étaient réalisées à sec jusqu’à une époque récente et pouvaient donc entraîner des atmosphères très poussiéreuses. L’exposition aux poussières a considérablement diminué dans les usines modernes, grâce à l’utilisation de fibres humides pour les trois dernières étapes de fabrication: ces fibres sont formées par un processus d’extrusion à partir d’une suspension colloïdale d’amiante. Dans l’industrie du papier fossile, l’exposition se produit en général lors de la réception et de la préparation des mélanges initiaux et lors de la découpe des produits finis, qui contenaient de 30 à 90% d’amiante dans les années soixante-dix. Dans la fabrication des garnitures de freins et autres produits de friction (moulés à sec, matricés, tissés ou bobinés), l’exposition à l’amiante se produit généralement au cours de la manipulation initiale, du mélange et de la préparation du produit fini, qui contenait de 30 à 80% d’amiante dans les années soixante-dix. Dans l’industrie du bâtiment, avant le recours systématique à des hottes d’aspiration et à la ventilation (dès 1960), le débitage avec des scies mécaniques à grande vitesse, le perçage et le ponçage des éléments de toiture contenant de l’amiante provoquaient la mise en suspension de poussières contenant des fibres, à proximité de la zone respiratoire des opérateurs, notamment lorsque ces travaux étaient exécutés dans des espaces confinés (gratte-ciel en construction, par exemple). Après la seconde guerre mondiale, c’est la démolition et la rénovation des navires de guerre ou des bâtiments qui ont constitué une source importante d’exposition, en particulier lors de l’utilisation, de la dépose, du déflocage ou du remplacement des matériaux contenant de l’amiante, en raison surtout du manque de connaissances relatives à la composition de ces matériaux (on ne savait pas qu’ils contenaient de l’amiante) et de l’ignorance des effets néfastes de cette exposition pour la santé. Par la suite, dans les années quatre-vingt-dix, le risque a pu être diminué dans certains pays grâce à l’éducation des travailleurs, à l’amélioration des pratiques industrielles et à la protection individuelle. Dans les industries de construction des trains et des véhicules à moteur, l’exposition avait surtout pour origine la dépose et le remplacement des revêtements calorifuges des moteurs de locomotives ou des garnitures de freins dans les camions et les voitures. Un certain nombre d’observations chez des travailleurs exposés au risque de pathologies pleurales continuent d’attirer l’attention, bien qu’il s’agisse d’applications désormais abandonnées, comme l’utilisation de rubans d’amiante pour la fabrication des électrodes de soudage ou de tissus d’amiante pour le calorifugeage des fours ou l’entretien des systèmes de roulage souterrain dans les mines.
L’exposition à l’amiante des personnes qui n’utilisent ou ne manipulent pas directement ce matériau dans le cadre de leur travail, mais qui travaillent en revanche dans le même secteur que des personnes en contact direct avec l’amiante est appelée exposition passive. Il s’agit là d’une source importante d’exposition, non seulement dans les années passées, mais encore à l’heure actuelle pour les cas diagnostiqués dans les années quatre-vingt-dix. Les catégories professionnelles ainsi exposées sont les électriciens, les soudeurs et les charpentiers dans les secteurs du bâtiment et dans les chantiers navals, le personnel d’entretien dans les usines d’amiante, les monteurs, les personnes chargées de l’exploitation des centrales électriques, de l’entretien des navires et des chaudières (dont l’isolation thermique est réalisée à l’aide de matériaux à l’amiante), ainsi que les personnes travaillant à l’entretien des tours d’habitation d’après-guerre, période au cours de laquelle divers matériaux à base d’amiante étaient utilisés. Autrefois, l’exposition domestique était surtout imputable aux vêtements de travail chargés de poussières, secoués ou nettoyés à la maison: les poussières ainsi libérées se déposaient sur les tapis et les meubles et étaient remises en suspension dans l’air en raison des activités de la vie quotidienne. Les concentrations de fibres dans l’air pouvaient atteindre 10 fibres par millilitre (f/ml), soit dix fois plus que la limite d’exposition professionnelle préconisée par l’OMS (1989), fixée à 1,0 f/ml; les fibres avaient par ailleurs tendance à rester plusieurs jours en suspension dans l’air. Depuis les années soixante-dix, il est d’usage de laisser les vêtements de travail à l’atelier ou à l’usine, où ils sont nettoyés; cette mesure n’est malheureusement pas respectée partout. Une autre source d’exposition est liée à la contamination atmosphérique des lieux d’habitation proches d’une activité industrielle. Par exemple, les concentrations d’amiante en suspension dans l’air sont plus importantes au voisinage des mines et des usines d’amiante; ces concentrations dépendent des niveaux d’activité, du contrôle des émissions et des conditions atmosphériques. Etant donné le délai très long qui s’écoule avant l’apparition, par exemple, d’une pathologie pleurale due à l’amiante, ce type d’exposition passive est encore responsable de nouveaux cas. Dans les années soixante-dix et quatre-vingt, le public a progressivement pris conscience de la nocivité potentielle de l’amiante et de ses utilisations extensives dans les matériaux de construction moderne (en particulier sous forme friable pour le flocage des murs, des plafonds et des conduits de ventilation) et s’est inquiété du devenir de ces bâtiments, soumis à l’usure du temps, et de la possibilité d’un relargage des fibres dans l’air en quantité suffisante pour constituer un danger pour la santé des travailleurs du bâtiment (voir les estimations de risques ci-après). Les autres sources de contamination de l’air dans les zones urbaines sont la libération des fibres provenant des garnitures de freins et leur remise en circulation par le passage des véhicules (Bignon, Peto et Saracci, 1989).
Les sources non industrielles d’exposition environnementale sont la présence naturelle des fibres dans le sol, par exemple en Europe orientale et dans les affleurements de roches de la région méditerranéenne, y compris la Corse, Chypre, la Grèce et la Turquie (Bignon, Peto et Saracci, 1989). Une autre source d’exposition humaine résulte de l’utilisation de la trémolite pour le blanchiment des maisons et de la fabrication du stuc en Grèce et en Turquie, mais aussi en Nouvelle-Calédonie (Luce et coll., 1994). Dans certains villages de Turquie, on trouve également une fibre de zéolite, l’érionite, utilisée pour la fabrication du stuc et la construction des maisons, incriminée dans la formation de mésothéliomes. Enfin, l’exposition peut également provenir de l’eau de boisson contaminée naturellement: l’amiante étant très répandue dans les affleurements, la plupart des sources d’eau en contiennent, mais les taux les plus élevés se trouvent dans les régions minières (Skinner, Roos et Frondel, 1988).
Les fibres d’amiante s’alignent lorsqu’elles sont portées par un courant d’air. Leur capacité de pénétrer dans les espaces pulmonaires plus profonds dépend de leur dimension: les fibres d’un diamètre aérodynamique inférieur ou égal à 5 µm pénètrent à plus de 80%, mais ont une rétention inférieure de 10 à 20%. Les particules plus grosses peuvent entrer en collision les unes avec les autres au niveau du nez et des bifurcations des voies aériennes principales où elles tendent à se rassembler. Les particules ainsi déposées sont éliminées grâce à l’action des cellules ciliées et transportées vers l’extérieur grâce au mucus. Les différences individuelles face à ce qui semble être une exposition identique proviennent, du moins partiellement, des différences interindividuelles de pénétration et de rétention des fibres inhalées (Bégin, Cantin et Massé, 1989). Les particules plus petites se déposent au-delà des voies aériennes principales et sont phagocytées par les macrophages alvéolaires qui servent d’éboueurs et digèrent les particules étrangères. Les fibres longues, c’est-à-dire mesurant plus de 10 µm, sont souvent attaquées par plus d’un macrophage et sont donc plus susceptibles d’être recouvertes et de former le noyau d’un corps asbestosique, structure caractéristique mise en évidence dès le début des années mille neuf cent et reconnue comme marqueur de l’exposition à l’amiante (voir figure 10.19). On considère que l’enrobage des fibres fait partie des systèmes de défense du poumon pour les rendre inertes et non immunogènes. La formation de corps asbestosiques est plus probable à partir des fibres d’amphibole que de chrysotile et leur nombre dans les matériaux biologiques (expectoration, lavage broncho-alvéolaire, tissu pulmonaire) est un indicateur indirect de la charge du poumon. Les fibres enrobées peuvent persister des années dans le poumon et être retrouvées dans les crachats et le liquide de lavage broncho-alvéolaire trente ans après l’exposition. L’élimination des fibres non enrobées déposées dans le parenchyme pulmonaire s’effectue vers la périphérie du poumon et les régions sous-pleurales, puis vers les ganglions lymphatiques de la base du poumon. Les théories permettant d’expliquer les mécanismes par lesquels les fibres provoquent des réactions pleurales sont les suivantes:
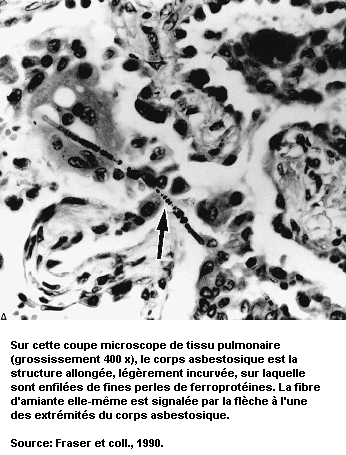
Pour expliquer la présence de mésothéliomes péritonéaux, on peut invoquer probablement aussi un flux rétrograde par l’intermédiaire du canal thoracique vers les ganglions lymphatiques abdominaux.
Les études effectuées chez l’animal indiquent que les premiers événements qui suivent la rétention d’amiante dans le poumon sont les suivants:
Ces réactions se retrouvent dans les substances biologiques récupérées dans le lavage broncho-alvéolaire chez l’humain et l’animal (Bégin, Cantin et Massé, 1989). La capacité biologique de fibrogenèse semble déterminée à la fois par les dimensions des fibres et leurs caractéristiques chimiques, lesquelles semblent, de même que les propriétés de surface, être importantes pour la cancérogenèse. Les fibres longues et fines sont plus actives que les courtes, même si l’activité de celles-ci n’est pas négligeable; les amphiboles sont plus actifs que le chrysotile, propriété attribuée à leur plus grande rémanence (Bégin, Cantin et Massé, 1989). Les fibres d’amiante peuvent également perturber le système immunitaire humain et modifier la population de lymphocytes circulants. Par exemple, les réactions immunitaires à médiation cellulaire en réponse à des antigènes cellulaires (comme ceux rencontrés dans un test tuberculinique) peuvent être mises en défaut (Browne, 1994). En outre, comme les fibres d’amiante semblent capables d’induire des anomalies chromosomiques, on suppose qu’elles peuvent également induire ou favoriser les cancers (Jaurand, Bignon et Brochard, 1993).
En pharmacologie et en toxicologie, la relation dose-réponse permet d’estimer la probabilité de survenue des effets souhaités ou le risque d’effets indésirables; la dose représente la quantité d’agent délivré à l’organe cible et restant en contact avec cet organe suffisamment longtemps pour provoquer une réaction. En médecine du travail, pour procéder à l’estimation des risques, on remplace la dose par d’autres paramètres permettant de quantifier ou qualifier l’exposition. Les études effectuées en milieu de travail permettent généralement de mettre en évidence des relations exposition-réponse, mais la mesure d’exposition la plus appropriée varie selon les maladies. Il peut sembler assez déconcertant de constater que même si les relations exposition-réponse sont différentes d’une catégorie professionnelle à l’autre, ces différences ne peuvent être expliquées qu’en partie par la fibre elle-même, la taille des particules et le procédé industriel employé. Ces relations exposition-réponse forment néanmoins la base scientifique pour l’évaluation des risques et l’établissement de niveaux d’exposition admissibles, initialement destinés à maîtriser l’asbestose (Selikoff et Lee, 1978). Comme la prévalence ou l’incidence de cette pathologie a diminué, on s’est davantage préoccupé de protéger la santé humaine contre les cancers dus à l’amiante. Au cours de ces dix dernières années, de nombreuses techniques ont été mises au point pour quantifier la charge en poussières des poumons ou la dose biologique, directement en termes de fibres par gramme de tissu pulmonaire sec. En outre, l’analyse aux rayons X à dispersion d’énergie permet de préciser la caractérisation de chaque fibre par type (Churg, 1991). Même si les résultats ne sont pas encore normalisés d’un laboratoire à l’autre, leur comparaison au sein d’un même laboratoire est utile et la mesure de la charge pulmonaire en fibres constitue désormais un nouvel outil pour l’évaluation des cas. En outre, l’application de ces techniques aux études épidémiologiques a pu:
L’asbestose est le nom donné à la pneumoconiose imputable à l’exposition aux poussières d’amiante. Le terme pneumoconiose est utilisé ici selon la définition donnée dans l’article «Les pneumoconioses: définitions» du présent chapitre; il désigne une pathologie se caractérisant par une «accumulation de poussières dans les poumons et des réactions tissulaires à la poussière». Dans le cas de l’asbestose, la réaction tissulaire est collagénique et provoque une altération définitive cicatricielle de l’architecture alvéolaire. Dès 1898, le rapport annuel de l’inspecteur en chef des fabriques du Royaume-Uni mentionnait les effets nocifs possibles de l’amiante sur la santé. Le rapport de 1899 détaillait le cas d’un homme ayant travaillé douze ans dans l’une des nouvelles usines textiles de Londres; son autopsie avait révélé une fibrose diffuse importante du poumon et la présence, à l’examen histologique des lames, de ce qui devait être appelé par la suite corps asbestosiques. Comme la fibrose pulmonaire est une pathologie rare, on a pensé que l’association devait être causale et le cas a été soumis en 1907 à la commission pour la réparation des maladies d’origine industrielle (Browne, 1994). En dépit de la publication de rapports de nature similaire rédigés par les inspecteurs du travail au Royaume-Uni, en Europe et au Canada dans les dix années qui ont suivi, le rôle de l’amiante dans la genèse de la maladie n’a été réellement reconnu qu’à partir d’une observation publiée dans le British Medical Journal, en 1927. Dans ce rapport, l’expression asbestose pulmonaire a d’abord été utilisée pour décrire cette pneumoconiose particulière, et des commentaires ont été présentés sur l’importance des réactions pleurales associées, à la différence, par exemple, de la silicose, principale pneumoconiose reconnue à l’époque (Selikoff et Lee, 1978). Dans les années trente, deux études majeures ont été réalisées dans l’industrie textile — l’une au Royaume-Uni, l’autre aux Etats-Unis — et ont démontré une relation exposition-réponse (et donc probablement causale) entre le niveau et la durée de l’exposition et les images radiologiques évocatrices de lésions dues à l’asbestose. Ces rapports ont servi de base pour les premières réglementations instituées au Royaume-Uni, promulguées en 1930, et les premières valeurs seuils pour l’amiante publiées par la Conférence américaine des hygiénistes industriels gouvernementaux (American Conference of Governmental Industrial Hygienists (ACGIH)), en 1938 (Selikoff et Lee, 1978).
Les lésions fibrotiques qui caractérisent l’asbestose sont la conséquence d’un processus inflammatoire dû à la présence des fibres retenues dans les poumons. La fibrose de l’asbestose est interstitielle, diffuse, a tendance à intéresser préférentiellement les lobes inférieurs et les zones périphériques et, dans les cas avancés, s’accompagne d’une destruction de l’architecture pulmonaire normale. Une fibrose de la plèvre adjacente est fréquente. Aucune donnée histologique de l’asbestose ne permet de la distinguer de la fibrose interstitielle due à d’autres causes, excepté la présence d’amiante dans les poumons soit sous forme de corps asbestosiques (visibles en microscopie optique), soit sous forme de fibres nues, généralement très fines et visibles en microscopie électronique seulement. Par conséquent, l’absence de corps asbestosiques dans les images obtenues en microscopie optique ne permet pas d’écarter une exposition à l’amiante ou un diagnostic d’asbestose. A l’autre extrémité du spectre de gravité de la maladie, la fibrose peut être circonscrite à quelques zones et affecter surtout les régions péribronchiolaires (voir figure 10.20), donnant lieu à ce qui a été appelé la maladie des petites voies aériennes due à l’amiante. Ici encore, hormis peut-être une implication plus importante des petites voies aériennes membraneuses, aucune lésion histologique ne distingue cette maladie des maladies des petites voies aériennes dues à d’autres causes (tabagisme ou exposition à d’autres poussières minérales), si ce n’est la présence d’amiante dans les poumons. La maladie des petites voies aériennes peut être la seule manifestation de la fibrose pulmonaire due à l’amiante ou peut coexister avec divers degrés de fibrose interstitielle, c’est-à-dire une asbestose (Wright et coll., 1992). L’évaluation de la sévérité de l’asbestose a fait l’objet de publications mettant en lumière toute une série de critères pris en considération (Craighead et coll., 1982). De façon générale, l’ampleur et l’intensité de la fibrose pulmonaire sont corrélées à la charge en poussières des poumons (Liddell et Miller, 1991).
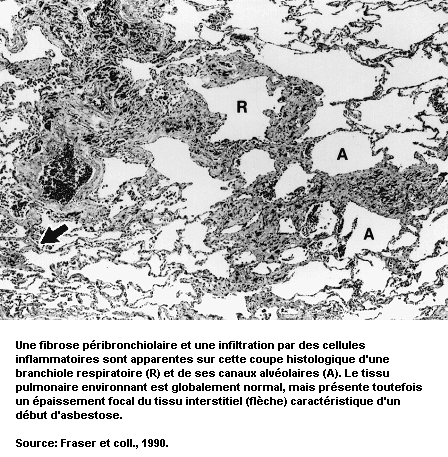
La dyspnée est le signe le plus précoce, le plus fréquent et le plus pénible de la maladie, ce qui a conduit à qualifier l’asbestose de maladie monosymptomatique (Selikoff et Lee, 1978). La dyspnée précède les autres symptômes, c’est-à-dire la toux sèche, souvent pénible, et l’oppression thoracique qui est, semble-t-il, associée aux réactions pleurales. A l’auscultation, on perçoit des râles inspiratoires tardifs ou crépitants, qui persistent après la toux, et qui siègent d’abord dans le creux axillaire et à la base des poumons, puis qui se généralisent avec l’évolution de la maladie; on pense qu’ils sont dus à l’ouverture explosive des voies aériennes qui se ferment à l’expiration. La présence de râles plus importants et de ronchi est souvent le signe d’une bronchite consécutive à un travail en milieu poussiéreux ou au tabagisme.
Traditionnellement, le seul outil diagnostique permettant d’établir la présence d’une asbestose était la radiographie thoracique, dont l’interprétation a été facilitée par la Classification radiologique du BIT (1980), qui classifie les petites opacités irrégulières caractéristiques de l’asbestose selon un continuum établi d’après la gravité de la maladie (décrite sur une échelle à 12 degrés allant de 0/– à 3/+) et son extension (caractérisée par le nombre des zones atteintes). Malgré les différences constatées entre les personnes qui interprètent les clichés — même chez les spécialistes — cette classification s’est révélée particulièrement utile dans les études épidémiologiques et a donc été employée cliniquement. Toutefois, jusqu’à 20% des sujets ayant une radiographie normale présentent des lésions caractéristiques de l’asbestose à la biopsie pulmonaire. En outre, la présence de petites opacités irrégulières de faible densité (c’est-à-dire de degré 1/0 sur l’échelle du BIT) n’est pas spécifique de l’asbestose mais peut être en rapport avec d’autres types d’exposition, comme la fumée de tabac (Browne, 1994). La tomodensitométrie (TDM) a révolutionné l’imagerie des maladies pulmonaires interstitielles, y compris l’asbestose, et la tomodensitométrie à haute résolution (TDM-HR) a augmenté la sensibilité de détection des pathologies interstitielles et pleurales (Fraser et coll., 1990). Les images caractéristiques de l’asbestose identifiées par la TDM-HR sont les épaississements interlobulaires (lignes septales) et intralobulaires (lignes non septales), les bandes parenchymateuses, les lignes courbes sous-pleurales et les opacités gravi-dépendantes sous-pleurales, les deux premières étant les plus caractéristiques de l’asbestose (Fraser et coll., 1990). La TDM-HR permet également d’identifier ces lésions dans les cas de déficit fonctionnel pulmonaire où les radiographies thoraciques ne sont pas concluantes. D’après la TDM-HR faite post mortem, la présence de lignes intralobulaires épaisses est corrélée à la fibrose péribronchique, et les lignes interlobulaires épaisses à la fibrose interstitielle (Fraser et coll., 1990). Jusqu’à présent, aucune méthode d’interprétation normalisée n’a été mise au point pour pouvoir utiliser la TDM-HR dans les pathologies dues à l’amiante. Outre son coût, le fait que l’appareil de tomodensitométrie soit installé à l’hôpital rend improbable son utilisation en routine pour la surveillance et les études épidémiologiques. Son rôle restera probablement limité aux cas individuels ou aux études planifiées destinées à traiter de problèmes spécifiques. La figure 10.21 illustre l’utilisation de l’imagerie thoracique pour établir le diagnostic de pneumopathie due à l’amiante; les cas présentés sont une asbestose, une pathologie pleurale due à l’amiante et un cancer bronchopulmonaire. La présence de grandes opacités, qui sont une complication des autres pneumoconioses, en particulier de la silicose, est inhabituelle dans l’asbestose et est généralement due à d’autres pathologies, comme le cancer pulmonaire (voir le cas décrit dans la figure 10.21) ou les atélectases rondes.
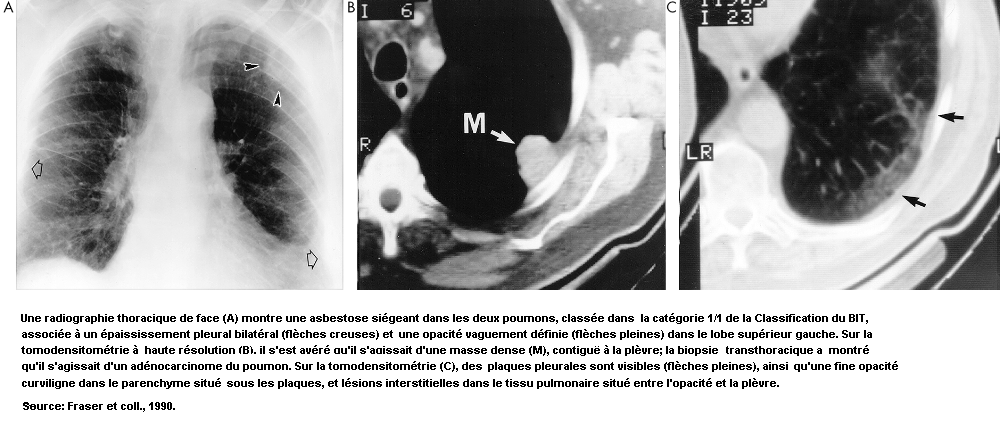
La fibrose pulmonaire interstitielle établie, consécutive à l’exposition à l’amiante, tout comme les fibroses pulmonaires dues à d’autres causes, est généralement, mais pas invariablement, associée à un trouble ventilatoire restrictif (Becklake, 1994). Elle se caractérise par une diminution des volumes pulmonaires, en particulier de la capacité vitale (CV), avec conservation du rapport VEMS/CVF% (volume expiratoire maximal seconde/capacité vitale forcée), une diminution de la compliance pulmonaire et des troubles des échanges gazeux. Une limitation ventilatoire avec baisse du rapport VEMS/CVF peut toutefois exister en réponse à un milieu professionnel poussiéreux ou au tabagisme. Au début d’une asbestose, lorsque les lésions pathologiques sont limitées à la fibrose péribronchiolaire et même avant l’apparition des petites opacités irrégulières à la radiographie thoracique, le seul signe de perturbation de la fonction respiratoire peut être un trouble des EFR, reflétant un dysfonctionnement des petites voies aériennes, comme le débit expiratoire médian maximal (DEM25-75). La réaction à l’effort peut également être perturbée dès le début de la maladie, avec une augmentation de la ventilation plus importante que celle requise pour répondre aux besoins accrus en oxygène (avec accélération de la fréquence respiratoire et respiration superficielle) et des troubles des échanges gazeux. Lorsque la maladie évolue, les échanges gazeux sont compromis pour des efforts de moins en moins intenses. Comme le travailleur exposé à l’amiante peut présenter un profil fonctionnel à la fois restrictif et obstructif, le médecin avisé doit interpréter les EFR pour ce qu’elles sont, une mesure de l’insuffisance respiratoire plutôt qu’une aide diagnostique. L’étude de la fonction pulmonaire, en particulier la mesure de capacité vitale, constitue un outil intéressant pour le suivi individuel des patients ou les études épidémiologiques, par exemple pour surveiller l’évolution de l’asbestose ou de la pathologie pleurale due à l’amiante après arrêt de l’exposition.
On utilise de plus en plus le lavage broncho-alvéolaire comme outil clinique pour étudier les pneumopathies dues à l’amiante afin:
Cet examen sert également à étudier les mécanismes pathogènes chez l’humain et l’animal (Bégin, Cantin et Massé, 1989). Enfin, la captation du gallium 67 permet de mesurer l’activité du processus pulmonaire, tandis que la présence d’anticorps antinucléaires sériques (AAS) et de facteurs rhumatoïdes (FR), qui reflètent l’état immunologique de l’individu, pourraient également influer sur la progression de la maladie ou expliquer les différences individuelles en réponse à ce qui semble être le même niveau et la même dose d’exposition.
La prévalence des signes radiologiques de l’asbestose dans les études effectuées en milieu professionnel varie considérablement et, comme on pouvait s’y attendre, ces différences sont liées à des différences de durée et d’intensité d’exposition plutôt qu’à des différences de lieux de travail. Toutefois, même si l’on tient compte de ces différences de lieux en limitant la comparaison des relations exposition-réponse aux études ayant fourni une estimation de l’exposition pour chaque membre de la cohorte, et si l’on se fonde sur l’historique du travail et les mesures d’hygiène industrielle, le risque est étroitement corrélé au type de fibre et au travail effectué (Liddell et Miller, 1991). Par exemple, une prévalence de 5% des petites opacités irrégulières (1/0 dans la Classification du BIT) résulte de l’exposition cumulée à environ 1 000 fibres/ml/année chez les mineurs de chrysotile du Québec, 400 fibres/ml/année chez les mineurs de chrysotile en Corse, et moins de 10 fibres/ml/année chez les mineurs de crocidolite d’Afrique du Sud et d’Australie. En revanche, chez les travailleurs du textile exposés au chrysotile du Québec, une exposition cumulée inférieure à 20 fibres/ml/année était à l’origine d’une prévalence de 5% de petites opacités irrégulières Les études de la charge pulmonaire en poussières montrent qu’il en va de même pour l’asbestose: chez vingt-neuf hommes travaillant dans des chantiers navals du Pacifique et présentant une asbestose associée surtout à l’amosite, la charge pulmonaire moyenne trouvée à l’autopsie était de 10 millions de fibres d’amosite par gramme de tissu pulmonaire sec, alors que la charge moyenne en chrysotile était de 30 millions de fibres par gramme de tissu pulmonaire sec chez vingt-trois mineurs et meuleurs de chrysotile au Québec (Becklake et Case, 1994). La taille des fibres n’explique pas complètement ces différences, ce qui suggère l’existence d’autres facteurs, spécifiques à chaque entreprise, y compris la présence d’autres polluants sur les lieux de travail.
L’asbestose peut rester stable ou évoluer, mais elle a peu de chances de régresser. En général, elle progresse avec l’âge, l’exposition cumulée, l’extension de la maladie existante; cette évolution est plus fréquente lorsque le crocidolite est l’agent incriminé. Les images radiologiques de l’asbestose peuvent évoluer ou apparaître longtemps après l’arrêt de l’exposition. Une détérioration de la fonction pulmonaire peut également se produire après arrêt de l’exposition (Liddell et Miller, 1991). Une question importante (à laquelle les études épidémiologiques n’apportent pas de réponse satisfaisante) est de savoir si le maintien de l’exposition augmente la probabilité de progression de la maladie lorsqu’il existe déjà des lésions radiologiques (Browne, 1994; Liddell et Miller, 1991). Dans certains pays, au Royaume-Uni par exemple, le nombre des demandes de réparation pour asbestose professionnelle a diminué ces dernières années, en rapport avec les mesures de prévention technique instaurées dès 1970 (Meredith et McDonald, 1994). Dans d’autres, comme en Allemagne (Gibbs, Valic et Browne, 1994), les taux d’asbestose continuent d’augmenter. Aux Etats-Unis, les taux de mortalité dus à l’asbestose par catégorie d’âge (reposant sur le fait que l’asbestose est mentionnée sur le certificat de décès comme cause du décès ou facteur contributif) pour la catégorie des plus de quinze ans a augmenté: ce taux était inférieur à 1 par million en 1960, supérieur à 2,5 en 1986 et égal à 3 en 1990 (USDHHS, 1994).
Le diagnostic clinique repose sur les trois volets suivants:
La radiographie thoracique reste la clé pour confirmer la présence de la maladie, complétée si possible en cas de doute par la TDM-HR. D’autres caractéristiques objectives sont la présence de râles crépitants aux bases. Les épreuves fonctionnelles respiratoires, avec épreuve d’effort, sont utiles pour déterminer la gêne fonctionnelle, étape indispensable à l’évaluation de la réparation. Cependant, comme ni la pathologie, ni les lésions radiologiques, ni les symptômes, ni les altérations de la fonction respiratoire ne sont caractéristiques d’une fibrose pulmonaire interstitielle due à l’asbestose, la mise en évidence de l’exposition est essentielle au diagnostic. En outre, le fait que les utilisateurs des nombreux produits à base d’amiante ignorent souvent même qu’ils en contiennent a rendu l’historique de l’exposition par l’interrogatoire plus difficile à retracer que prévu. Si cet interrogatoire n’est pas suffisant, l’identification de l’agent dans des échantillons biologiques (expectoration, lavage broncho-alvéolaire et éventuellement biopsie) peut corroborer l’exposition; une évaluation quantitative de la charge pulmonaire peut être établie à l’autopsie ou après exérèse pulmonaire. La mise en évidence de l’activité de la maladie (à partir d’une scintigraphie au gallium 67 ou d’un lavage broncho-alvéolaire) peut contribuer à estimer le pronostic, élément fondamental pour cette pathologie irréversible. Même en l’absence de preuves épidémiologiques tangibles du ralentissement de l’évolution après l’arrêt de l’exposition, il semble prudent et utile de décider d’arrêter le travail. Il ne s’agit toutefois pas d’une décision facile à prendre ou à recommander, surtout chez les travailleurs âgés qui risquent fort de ne pas retrouver d’emploi. Cependant, l’exposition devrait être impérativement interrompue si le lieu de travail n’est pas conforme aux normes en vigueur. Les critères relatifs au diagnostic de l’asbestose dans un cadre épidémiologique sont moins exigeants, en particulier dans les études transversales réalisées dans les milieux professionnels, qui incluent tous les travailleurs en assez bonne santé pour travailler. Ces études traitent généralement plutôt des relations de causalité et font souvent appel à des marqueurs qui indiquent la présence d’une atteinte minime, reposant soit sur le niveau de la fonction pulmonaire, soit sur des images radiologiques pathologiques. En revanche, en médecine médico-légale, les critères de diagnostic sont beaucoup plus stricts et varient selon les systèmes administratifs et juridiques en vigueur dans chaque pays.
Les premières descriptions de l’asbestose mentionnent que la fibrose de la plèvre viscérale participe au processus pathologique (voir «L’anatomopathologie» ci-dessus). Dans les années trente, on a également décrit la présence de plaques pleurales circonscrites, souvent calcifiées, dans la plèvre pariétale (qui borde la paroi thoracique et couvre la surface du diaphragme), apparaissant après une exposition environnementale non professionnelle. Une étude réalisée en 1955 dans une usine allemande rapportait une prévalence de 5% de lésions pleurales à la radiographie thoracique, attirant ainsi l’attention sur le fait que la pathologie pleurale pouvait être la première manifestation de l’exposition, voire la seule. Les réactions pleurales viscéropariétales, qui comprennent la fibrose pleurale diffuse, l’épanchement pleural bénin (décrit pour la première fois dans les années soixante) et des atélectases rondes (décrites pour la première fois dans les années quatre-vingt), sont actuellement toutes considérées comme des réactions corrélées les unes aux autres, mais se distinguant des plaques pleurales d’un point de vue anatomopathologique, pathogénétique et clinique. Dans les juridictions où les taux de prévalence ou d’incidence de l’asbestose diminuent, les manifestations pleurales, qui sont en constante augmentation dans les enquêtes, constituent de plus en plus l’élément révélateur de l’exposition passée et le motif de consultation.
Les plaques pleurales sont des lésions lisses, surélevées, irrégulières et blanches couvertes de mésothélium, localisées au niveau de la plèvre pariétale ou du diaphragme (voir figure 10.22). Leur taille est variable, elles sont souvent multiples et elles ont tendance à se calcifier avec l’âge (Browne, 1994). Seule une faible proportion des plaques détectées à l’autopsie sont visibles à la radiographie thoracique, mais la plupart peuvent être décelées par la TDM-HR. En l’absence de fibrose pulmonaire, les plaques pleurales peuvent être asymptomatiques et n’être détectées que lors des radiographies systématiques de dépistage. Toutefois, les études réalisées dans les milieux professionnels montrent invariablement qu’elles sont associées à une insuffisance de la fonction respiratoire, modeste mais mesurable, atteignant surtout la CV et la CVF (Ernst et Zejda, 1991). Des enquêtes radiologiques effectuées aux Etats-Unis ont mis en évidence des taux de 1% chez les hommes sans exposition connue, et de 2,3% si l’on inclut les hommes des populations urbaines soumis à une exposition professionnelle. Ces pourcentages sont plus élevés dans les collectivités proches des industries de l’amiante ou qui font un grand usage de produits dérivés, alors que dans certaines catégories professionnelles, comme les tôliers, les poseurs de matériaux isolants, les plombiers et les ouvriers des chemins de fer, les taux peuvent dépasser 50%. Dans une enquête finlandaise réalisée en 1994 à partir d’autopsies effectuées chez 288 hommes âgés de 35 à 69 ans, décédés brutalement, on a détecté des plaques pleurales dans 58% des cas, leur présence tendant à augmenter avec l’âge, la probabilité d’exposition (d’après l’anamnèse), la concentration de fibres d’amiante dans le tissu pulmonaire et le tabagisme (Karjalainen et coll., 1994). On a estimé à 24% la fraction étiologique des plaques imputable à une charge pulmonaire à 0,1 million de fibres par gramme de tissu pulmonaire (cette valeur est considérée comme sous-évaluée). Les études de charge pulmonaire en poussières corroborent également l’existence d’un gradient de fibres qui provoque des réactions pleurales d’intensité proportionnelle. On a trouvé une charge pulmonaire moyenne de 1,4 million de fibres par gramme de tissu pulmonaire chez 103 hommes exposés à l’amosite travaillant dans des chantiers navals du Pacifique; tous présentaient des plaques pleurales, alors que la charge était respectivement de 15,5 et 75 millions de fibres par gramme de tissu pulmonaire, pour le chrysotile et la trémolite, chez 63 mineurs et meuleurs de chrysotile du Québec examinés de la même façon (Becklake et Case, 1994).
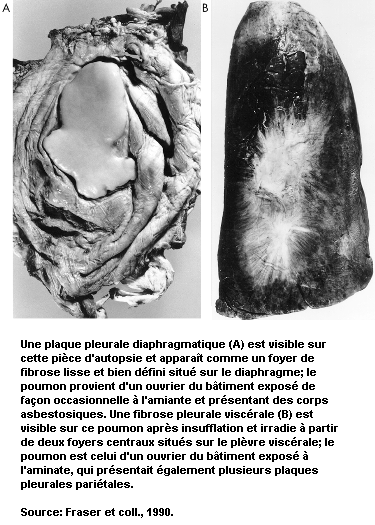
Si les aspects anatomopathologiques et pathogéniques des différentes formes de réactions viscéropariétales dues à l’amiante sont presque certainement corrélés, les manifestations cliniques et la symptomatologie sont différentes. Chez certains sujets, une réaction pleurale aiguë exsudative due à l’amiante peut se produire et se manifester par un épanchement pleural, sans signe pathologique préalable. Chez d’autres, la maladie se manifeste par une exacerbation de la gravité et de l’extension de réactions pleurales préexistantes. Ces épanchements pleuraux sont qualifiés de bénins, par opposition aux épanchements associés aux mésothéliomes malins. Les épanchements pleuraux bénins apparaissent typiquement dix à quinze ans après la première exposition (ou après une exposition antérieure limitée) qui a eu lieu chez des individus âgés de vingt à trente ans. Ces manifestations pleurales sont généralement transitoires, mais peuvent récidiver; elles peuvent intéresser un seul poumon ou les deux, de façon simultanée ou séquentielle. Elles peuvent être silencieuses ou symptomatiques, avec sensation d’oppression thoracique ou de douleur pleurale et de dyspnée. Le liquide pleural contient des leucocytes, souvent du sang, et il est riche en albumine; il renferme rarement des corps asbestosiques ou des fibres, qui peuvent toutefois être mis en évidence à la biopsie de la plèvre ou du poumon sous-jacent. La plupart des épanchements pleuraux bénins régressent spontanément mais, chez un faible pourcentage de patients, ils peuvent évoluer vers un épaississement pleural diffus (de l’ordre de 10% dans une série) (voir figure 10.22), avec ou sans développement d’une fibrose pulmonaire. Les réactions pleurales locales peuvent également se circonscrire et piéger le tissu pulmonaire, causant des lésions bien définies appelées atélectasie par enroulement ou pseudo-tumeur, car elles peuvent avoir l’aspect d’un cancer pulmonaire à la radiographie. Contrairement aux plaques pleurales, qui sont rarement symptomatiques, les réactions pleurales viscéropariétales s’accompagnent généralement d’une dyspnée et d’une atteinte de la fonction respiratoire, surtout en cas de comblement de l’angle costo-phrénique. Dans une étude, le déficit moyen de la CVF était de 0,07 l en cas d’atteinte isolée de la paroi thoracique et de 0,50 l en cas de comblement de l’angle costo-phrénique (Ernst et Zejda, 1991). Comme cela a déjà été mentionné, la répartition et les déterminants des réactions pleurales varient considérablement selon les catégories professionnelles et la prévalence augmente selon les paramètres suivants:
Au cours des années trente, de nombreux travaux publiés en Allemagne, aux Etats-Unis et au Royaume-Uni ont concerné des cas cliniques de cancer broncho-pulmonaire (pathologie à l’époque moins courante qu’aujourd’hui) constatés chez des travailleurs de l’amiante dont la plupart présentaient aussi une asbestose de gravité variable. En 1947, le rapport annuel de l’inspecteur en chef des fabriques du Royaume-Uni fournissait d’autres données en faveur de l’association de ces deux pathologies, puisqu’il mentionnait qu’un cancer broncho-pulmonaire était décrit dans 13,2% des décès de sujets de sexe masculin dus à l’asbestose entre 1924 et 1946, et dans seulement 1,3% des décès dus à la silicose. La première étude portant sur l’hypothèse de causalité était une étude de mortalité sur cohorte réalisée dans une importante usine textile du Royaume-Uni (Doll, 1955); il s’agit de l’une des premières études orientées vers les catégories professionnelles. En 1980, après qu’au moins huit études de ce type, réalisées dans huit milieux professionnels distincts, eurent confirmé la relation exposition-réponse, l’association a été considérée comme causale (McDonald et McDonald, 1987).
En l’absence d’autres pathologies dues à l’amiante, les caractéristiques cliniques et les critères diagnostiques du cancer broncho-pulmonaire dû à l’amiante ne sont pas différents de ceux des cancers broncho-pulmonaires d’autres origines. Initialement, le cancer broncho-pulmonaire dû à l’amiante était considéré comme cicatriciel, comparable aux formes cancéreuses observées dans d’autres fibroses pulmonaires diffuses, comme la sclérodermie. Les caractéristiques invoquées en faveur de cette hypothèse étaient la localisation aux lobes pulmonaires inférieurs (siège d’une asbestose généralement plus importante), des localisations parfois multiples et une prépondérance des adénocarcinomes dans certaines séries. Toutefois, dans la plupart des études réalisées en milieu professionnel, la distribution des types cellulaires n’est pas différente de celle observée dans les études concernant des populations non exposées à l’amiante, ce qui suggère que l’amiante peut être un agent cancérogène en soi, conclusion à laquelle est parvenu le Centre international de recherche sur le cancer (OMS, CIRC, 1982). La plupart des cancers broncho-pulmonaires dus à l’amiante, mais pas tous, apparaissent en association avec une asbestose radiologique (voir ci-après).
Les études de cohortes confirment que le risque de cancer broncho-pulmonaire augmente avec l’exposition — même si le taux proportionnel d’augmentation pour chaque fibre par millilitre par année d’exposition est variable — et dépend du type de fibre et du procédé de fabrication employé (Health Effects Institute — Asbestos Research, 1991). Ainsi, en ce qui concerne les expositions au chrysotile, le taux augmentait de 0,01 à 0,17% dans les secteurs de l’extraction, du meulage et de la fabrication des produits de friction, et de 1,1 à 2,8% dans l’industrie textile, tandis qu’en ce qui concernait l’exposition aux produits d’isolation à base d’amosite et aux ciments à base de mélanges de fibres les taux pouvaient s’élever à 4,3 et 6,7% (Nicholson, 1991). Les études de cohortes réalisées chez les travailleurs de l’amiante confirment également que le risque de cancer est démontrable pour les non-fumeurs et qu’il augmente (selon une allure exponentielle plutôt que linéaire) avec le tabagisme (McDonald et McDonald, 1987). Le risque relatif de cancer broncho-pulmonaire diminue à l’arrêt de l’exposition, mais la réduction de ce risque est plus lente que celle observée après cessation du tabagisme. Les études de la charge pulmonaire en poussières confirment également l’existence d’un gradient de fibres dans la genèse du cancer broncho-pulmonaire: on a trouvé une charge pulmonaire moyenne de 1,1 million de fibres d’amosite par gramme de tissu pulmonaire sec chez trente-deux hommes travaillant dans des chantiers navals du Pacifique, alors que la charge était de 13 millions de fibres de chrysotile par gramme de tissu pulmonaire chez trente-six mineurs du Québec (Becklake et Case, 1994).
Dans l’étude de 1955 réalisée sur des sujets autopsiés, les causes de décès ont été recherchées chez 102 employés de l’usine de textiles en amiante du Royaume-Uni mentionnée plus haut (Doll, 1955): un cancer broncho-pulmonaire a été trouvé chez 18 sujets, dont 15 présentaient également une asbestose. Tous les sujets présentant l’association asbestose/cancer broncho-pulmonaire avaient travaillé pendant au moins neuf ans avant 1931, date d’entrée en vigueur de la réglementation nationale sur l’amiante. Ces observations suggéraient que lorsque les niveaux d’exposition diminuaient, le risque de décès dû à l’asbestose diminuait aussi et les travailleurs vivaient assez longtemps pour développer un cancer. Dans la plupart des études réalisées dans les milieux professionnels, les travailleurs plus âgés comptant de nombreuses années de service présentaient à l’autopsie des signes anatomopathologiques d’asbestose (ou de maladie des petites voies aériennes due à l’amiante), et, cela, même en l’absence de lésions décelables lors des dépistages radiologiques (McDonald et McDonald, 1987). Plusieurs études de cohortes (mais pas toutes) sont compatibles avec l’idée que toutes les augmentations des cas de cancer broncho-pulmonaire observés dans les populations exposées à l’amiante ne sont pas corrélées à une asbestose. Les mécanismes pathogéniques responsables du cancer broncho-pulmonaire chez les individus exposés à l’amiante sont certainement multiples et dépendent des localisations et des dépôts de fibres. On considère, par exemple, que les fibres longues et fines, déposées préférentiellement au niveau des bifurcations des voies aériennes, sont plus concentrées et agissent comme des inducteurs du processus de cancérogenèse par l’intermédiaire de lésions chromosomiques. L’exposition continue aux fibres d’amiante ou à la fumée de tabac joue probablement un rôle promoteur dans ce processus (Lippman, 1994). Ces cancers sont généralement de type épidermoïde. En revanche, en cas de fibrose, la cancérogenèse résulte plus probablement du processus fibreux et les cancers sont plus généralement de type adénocarcinomateux.
Si les facteurs étiologiques de l’augmentation du risque de cancer peuvent être établis pour les populations exposées, l’agent causal est difficile à déceler dans les cas individuels. La responsabilité de l’amiante dans le développement éventuel d’un cancer est naturellement plus probable et plus crédible chez un sujet atteint d’asbestose qui n’a jamais fumé que chez un sujet exposé qui ne présente pas d’asbestose mais qui fume. Mais cette responsabilité est difficile à modéliser. Les mesures de charge pulmonaire en poussières peuvent compléter un examen clinique approfondi, mais chaque cas doit être évalué selon ses caractéristiques propres (Becklake, 1994).
Les mésothéliomes malins apparaissent dans les cavités séreuses de l’organisme. Environ deux tiers d’entre eux sont situés dans la plèvre et un cinquième dans le péritoine, tandis que le péricarde et la muqueuse vaginale sont beaucoup moins affectés (McDonald et McDonald, 1991). Comme les cellules mésothéliales ont un potentiel évolutif diversifié, les caractéristiques histologiques des tumeurs mésothéliales sont variables; dans la plupart des cas, les formes épithéliales, sarcomateuses et mixtes représentent respectivement 50%, 30% et 10% des cas. Le diagnostic de cette tumeur rare n’est pas facile, même pour un anatomopathologiste expérimenté et il n’est confirmé que chez un faible pourcentage des cas soumis à l’analyse, souvent moins de 50% de ceux-ci. Diverses techniques cytologiques et immuno-histochimiques ont été mises au point pour établir un diagnostic différentiel entre les mésothéliomes malins et les autres diagnostics cliniques possibles, c’est-à-dire le cancer secondaire ou l’hyperplasie mésothéliale réactive; on attend beaucoup de ce domaine qui fait l’objet de recherches actives, mais les résultats ne sont pas encore concluants (Jaurand, Bignon et Brochard, 1993). Pour toutes ces raisons, la confirmation des cas aux fins d’enquêtes épidémiologiques n’est pas aisée et souvent incomplète, même si l’on se fonde sur les registres des cancers. En outre, cette confirmation doit être faite par un groupe d’experts sur la base de critères anatomopathologiques bien précis afin de garantir la comparabilité des critères pour l’inscription dans les registres.
La douleur est le symptôme principal. Quand il s’agit de tumeurs pleurales, la douleur débute dans le thorax ou les épaules et peut être intense. Par la suite, une dyspnée apparaît, accompagnée d’un épanchement pleural ou d’un envahissement progressif du poumon par la tumeur et d’une perte de poids. Dans le cas de tumeurs péritonéales, la douleur abdominale s’accompagne généralement d’œdème. Les caractéristiques radiographiques sont illustrées à la figure 10.23. L’évolution clinique est généralement rapide; les temps de survie médians étaient de six mois en 1973 et de huit en 1993: ils ont donc peu évolué au cours de ces vingt dernières années, malgré une prise de conscience plus développée du public et du monde médical grâce à laquelle on peut poser un diagnostic plus précoce de la maladie et malgré les progrès technologiques et une plus large palette de choix thérapeutiques.
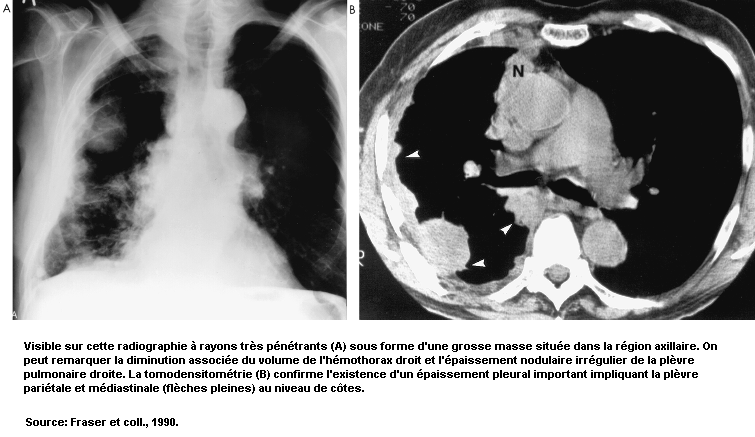
Au cours des quinze années qui ont suivi le rapport de 1960 concernant une série de cas de mésothéliomes observés dans la région nord-ouest de la province du Cap en Afrique du Sud (Wagner, 1998), des rapports internationaux ont confirmé le caractère professionnel de l’affection. Ces rapports provenaient d’Europe (Allemagne, France, Pays-Bas, Royaume-Uni), des Etats-Unis (Illinois, New Jersey, Pennsylvanie) et d’Australie; il s’agissait également d’études cas-témoins réalisées au Royaume-Uni (quatre villes), en Italie, aux Pays-Bas et en Suède, aux Etats-Unis et au Canada. Dans ces études, les odds-ratios (rapports de cotes) étaient compris entre 2 et 9. En Europe en particulier, l’association avec les activités professionnelles des chantiers navals était marquée. En outre, d’après des études de mortalité proportionnelle effectuées dans des cohortes exposées à l’amiante, le risque était associé au type de fibre et au procédé de production, les taux de mésothéliomes variant de 0,3% dans les mines de chrysotile à 1% dans la fabrication de produits à base de chrysotile, contre 3,4% pour les amphiboles et 8,6% lorsqu’il s’agissait d’une exposition à un mélange de fibres pour isolation (McDonald et McDonald, 1991). Des gradients de fibres comparables ont été mis en évidence dans les études de mortalité sur cohortes qui constituent de bons indices de l’incidence, étant donné les temps de survie très courts pour ce type de tumeurs. Ces études montrent également que le temps de latence est plus long si l’exposition concerne le chrysotile plutôt que les amphiboles. La distribution géographique de l’incidence a été établie sur la base des taux, par âge et par sexe, observés au Canada entre 1966 et 1972, taux qui ont permis de calculer les valeurs attendues (McDonald et McDonald, 1991); les rapports des valeurs observées aux valeurs attendues étaient de 0,8 pour les Etats-Unis (1972); 1,1 pour la Suède (de 1958 à 1967); 1,3 pour la Finlande (de 1965 à 1969); 1,7 pour le Royaume-Uni (de 1967 à 1968); et 2,1 pour les Pays-Bas (de 1969 à 1971). Même si des facteurs d’ordre technique expliquent probablement en partie les écarts observés, les résultats suggèrent une plus forte fréquence en Europe qu’en Amérique du Nord.
Les variations selon l’âge et le sexe de la fréquence des mésothéliomes ont été utilisées comme mesure du retentissement de l’exposition à l’amiante sur la santé des populations. Les meilleures estimations relatives aux pourcentages globaux dans les pays industriels, avant 1950, sont inférieures à 1,0 par million pour les hommes et les femmes (McDonald et McDonald, 1993). Par la suite, ces pourcentages ont augmenté de façon constante chez l’homme, ce qui n’est pas le cas pour la femme. Ainsi, les pourcentages respectifs rapportés au million chez l’homme et la femme étaient de 11,0 et de moins de 2,0 aux Etats-Unis en 1982; de 14,7 et 7,0 au Danemark pour la période 1975-1980; de 15,3 et 3,2 au Royaume-Uni pour la période 1980-1983; et de 20,9 et 3,6 aux Pays-Bas pour la période 1978-1987. Des pourcentages plus élevés chez l’homme et la femme, mais excluant toutefois les sujets jeunes, ont été rapportés dans les pays de mines de crocidolite: les chiffres respectifs étaient de 28,9 et 4,7 en Australie (sujets de plus de 20 ans) en 1986, contre 32,9 et 8,9 chez les Blancs d’Afrique du Sud (de plus de 15 ans) en 1988 (Health Effects Institute — Asbestos Research, 1991). Les taux plus élevés constatés chez l’homme sont probablement liés à l’exposition professionnelle; ils devraient donc être stationnaires ou diminuer après la période d’«incubation» de vingt à trente ans suivant l’introduction des mesures de sécurité et de prévention sur les lieux de travail et la diminution consécutive des niveaux d’exposition professionnelle dans la plupart des pays industriels dans les années soixante-dix. Dans les pays où les taux augmentent chez la femme, cette augmentation reflète la présence croissante des femmes dans les professions exposées, ou encore la contamination de l’air de plus en plus importante dans l’environnement ou les espaces intérieurs en zone urbaine (McDonald, 1985).
En matière de risque de mésothéliome, les facteurs environnementaux sont nettement prédominants. L’exposition à l’amiante arrive en tête, bien que l’apparition de la maladie dans certains groupes familiaux suggère que des facteurs génétiques puissent jouer un rôle. Tous les types d’amiante ont été impliqués dans l’induction des mésothéliomes, y compris l’anthophyllite, citée pour la première fois dans un rapport finlandais (Meurman, Pukkala et Hakama, 1994). Cependant, les résultats des études de mortalité proportionnelle et sur cohortes, ainsi que les études de charge pulmonaire suggèrent le rôle d’un gradient de fibres dans le déclenchement des mésothéliomes: le risque est plus important lorsque les expositions concernent principalement les amphiboles ou les mélanges amphiboles/chrysotile que lorsqu’elles impliquent surtout le chrysotile. En outre, on trouve des différences selon les catégories professionnelles pour la même fibre et pour ce qui semble être le même niveau d’exposition; ces différences demeurent mystérieuses, même si la taille des fibres peut être un élément d’explication.
Le rôle de la trémolite a été largement débattu; le débat a été suscité par la preuve de sa biopersistance dans le tissu pulmonaire (d’origine animale ou humaine), plus importante que celle du chrysotile. Une hypothèse plausible est que les nombreuses fibres courtes qui atteignent les voies aériennes périphériques et les alvéoles sont éliminées par les ganglions lymphatiques sous-pleuraux où elles se collectent. Leur aptitude à produire des mésothéliomes dépend de leur biopersistance au contact des surfaces pleurales (Lippmann, 1995). Dans les études humaines, les taux de mésothéliome sont plus faibles dans les populations professionnellement exposées au chrysotile relativement peu contaminé par la trémolite (dans les mines du Zimbabwe, par exemple) que dans celles exposées au chrysotile contaminé par la trémolite (comme dans les mines du Québec); ces résultats ont été retrouvés chez l’animal (Lippmann, 1995). De même, dans une analyse multifactorielle réalisée à partir d’une étude cas-témoins au Canada (McDonald et coll., 1989), les résultats suggèrent que la plupart des mésothéliomes, si ce n’est tous, pouvaient être expliqués par la charge pulmonaire en fibres de trémolite. Enfin, une analyse récente de mortalité réalisée sur une cohorte de plus de 10 000 mineurs et meuleurs de chrysotile au Québec entre 1890 et 1920 et poursuivie jusqu’en 1988 (McDonald et McDonald, 1995) corrobore ce résultat: sur près de 7 300 décès, les 37 décès dus au mésothéliome étaient concentrés dans certaines mines de la région de Thetford; cependant, la charge pulmonaire de 88 membres de la cohorte provenant des mêmes mines n’était pas différente de celle observée chez les mineurs d’autres mines en termes de fibres de chrysotile, mais différait en termes de charge en trémolite (McDonald et coll., 1993).
Ce qui a été appelé la question de la trémolite constitue peut-être à l’heure actuelle le débat scientifique le plus important; il a d’ailleurs de nombreuses implications en ce qui concerne la santé publique. Fait important, dans toutes les séries et juridictions, un certain nombre de cas se produisent sans qu’il soit fait mention d’une exposition à l’amiante, et ce ne sont souvent que les études de charge pulmonaire qui mettent en évidence une exposition environnementale ou professionnelle antérieure. D’autres expositions professionnelles ont été incriminées dans le développement des mésothéliomes, comme les travaux dans les mines de talc, de vermiculite et, peut-être, de mica; dans ces cas précis, toutefois, les gisements contenaient également de la trémolite et d’autres fibres (Bignon, Peto et Saracci, 1989). Pour comprendre la pathogénèse des mésothéliomes, il importe donc de continuer à rechercher toutes les expositions possibles, professionnelles ou non, aux différents types de fibres, (organiques ou non), et d’autres agents.
Cette rubrique concerne généralement la bronchite chronique et la broncho-pneumopathie chronique obstructive — qui peuvent toutes deux être diagnostiquées cliniquement — , ainsi que l’emphysème qui ne pouvait l’être jusqu’ici que par un examen anatomopathologique des poumons (Becklake, 1992). La mortalité et la morbidité ont augmenté au cours des dernières décennies dans la plupart des pays industriels; le tabagisme en est une cause majeure. Toutefois, les pneumoconioses étant en régression dans la plupart des industries, il était naturel, après avoir pris en compte le rôle dominant joué par le tabagisme, d’incriminer l’exposition professionnelle dans la genèse des affections chroniques des voies aériennes. Il a été démontré que les différentes formes d’affections chroniques des voies aériennes étaient associées au travail dans les professions en milieu empoussiéré, en particulier lorsque l’amiante constituait une part importante des poussières contaminant le lieu de travail (Ernst et Zejda, 1991). On pense que c’est la charge totale de polluants, plutôt que l’exposition à un agent polluant particulier — la poussière d’amiante, dans le cas présent — qui intervient dans ces affections de façon comparable au tabagisme. En ce qui concerne le tabagisme, on compte en termes de charge d’exposition totale (paquets-années) et non en termes d’exposition à l’un des 4 000 constituants de la fumée de cigarette (la relation entre les expositions professionnelles et les affections chroniques des voies aériennes est abordée ailleurs dans ce volume).
Dans plusieurs des premières études de cohortes portant sur des travailleurs exposés à l’amiante, la mortalité totale imputable au cancer dépassait les chiffres attendus, calculés d’après les registres nationaux ou locaux. Le cancer broncho-pulmonaire était le principal responsable de cette augmentation, mais d’autres cancers étaient impliqués: cancer gastro-intestinal, laryngé et ovarien, par ordre de fréquence. En ce qui concernait les cancers gastro-intestinaux (cancer de l’œsophage, de l’estomac, du côlon et du rectum) décrits dans les cohortes de travailleurs, l’exposition était probablement due à la déglutition des expectorations chargées d’amiante provenant des grosses bronches; il en allait de même autrefois (avant la mise en œuvre de mesures de protection contre l’exposition sur les lieux de restauration), alors qu’existait un risque de contamination directe des aliments dans les entreprises ne disposant pas de cantine séparée. Les ganglions lymphatiques drainant les poumons pouvaient également constituer une source, par un flux rétrograde dans le canal thoracique (voir ci-dessus la section «Le devenir des fibres inhalées»). Toutefois, comme les différentes cohortes étudiées n’ont pas montré la même relation entre l’exposition et l’atteinte pulmonaire et que parfois l’association n’existait pas du tout, l’existence d’un rapport de causalité entre l’exposition professionnelle et l’exposition à l’amiante a suscité quelque scepticisme (Doll et Peto, 1987; Liddell et Miller, 1991).
Le cancer du larynx est bien moins fréquent que le cancer gastro-intestinal ou le cancer broncho-pulmonaire. Dès les années soixante-dix, on a évoqué une association entre le cancer du larynx et l’exposition à l’amiante. Comme pour le cancer broncho-pulmonaire, l’un des principaux risques et l’une des causes majeures du cancer laryngé est le tabagisme. Ce type de cancer est également fortement corrélé à la consommation d’alcool. Etant donné sa localisation (le larynx est exposé, à l’instar des poumons, à tous les polluants en suspension dans l’air) et le fait qu’il est tapissé par le même épithélium que celui des grosses bronches, il est tout à fait plausible d’un point de vue biologique que le cancer du larynx résulte de l’exposition à l’amiante. Toutefois, les données dont on dispose actuellement ne sont pas homogènes, même dans les études sur grandes cohortes, comme celle concernant les mineurs de chrysotile du Québec et de Balangero (Italie), probablement parce qu’il s’agit d’un cancer rare; il est difficile pour cette raison de mettre en évidence un rapport de causalité pour cette association (Liddell et Miller, 1991), et, cela, malgré sa plausibilité biologique. On a noté une augmentation des cancers ovariens supérieure aux chiffres attendus dans trois études de cohortes (OMS, 1989). La plupart des cas peuvent être expliqués par des erreurs de diagnostic, en particulier dans les cas de cancers diagnostiqués comme étant des mésothéliomes péritonéaux (Doll et Peto, 1987).
La prévention des pneumoconioses de tous types (y compris l’asbestose) a été assurée jusqu’ici par les mesures classiques ci-après:
Les niveaux d’exposition admissibles ont été initialement fixés pour prévenir l’asbestose; ils reposaient sur les mesures de concentrations exprimées en millions de particules par m3; les méthodes utilisées étaient les mêmes que dans le cas de la silicose. L’intérêt biologique s’étant concentré sur les fibres (en particulier celles qui sont longues et fines) dans la genèse de l’asbestose, des méthodes plus appropriées pour leur identification et leur mesure dans l’air ont été mises au point, si bien que l’attention portée aux fibres plus courtes, particulièrement abondantes sur les lieux de travail, s’est estompée. Le rapport morphologique (longueur/diamètre) de la plupart des particules de chrysotile est compris entre 5/1 et 20/1 et peut atteindre jusqu’à 50/1, alors que pour la plupart des particules d’amphibole (y compris les fragments de clivage) ce rapport est inférieur à 3/1. L’introduction de filtres à membranes pour permettre la numération des particules dans les échantillons d’air prélevés a conduit à une définition arbitraire, tant sur le plan de l’hygiène industrielle que sur le plan médical, stipulant qu’une fibre est une particule mesurant au moins 5 µm de long, moins de 3 µm d’épaisseur, avec un rapport longueur/largeur supérieur ou égal à 3/1. Cette définition, utilisée dans la plupart des études de relations exposition-réponse, constitue la base scientifique des normes environnementales.
Cette définition a été utilisée, par exemple, dans une réunion tenue sous l’égide de l’Organisation mondiale de la santé (1989) pour proposer des limites d’exposition professionnelle; elle a été adoptée par des organismes tels que l’Administration de la sécurité et de la santé au travail (Occupational Safety and Health Administration (OSHA)) aux Etats-Unis. Elle permet surtout d’effectuer des comparaisons. La réunion de l’OMS, présidée par sir Richard Doll, tout en reconnaissant que la limite d’exposition professionnelle d’un pays ne peut être fixée que par les instances nationales concernées, recommandait aux pays ayant des limites élevées de prendre des mesures urgentes pour ramener les niveaux d’exposition professionnelle individuelle à 2 f/ml (moyenne pondérée sur huit heures de travail) et incitait tous les pays à descendre aussi rapidement que possible à 1 f/ml (moyenne pondérée sur huit heures de travail), si cela n’était déjà le cas. Avec le recul des cas d’asbestose dans certains pays industriels et les préoccupations concernant les cancers liés à l’amiante, on se pose désormais la question de savoir si les mêmes paramètres servant à définir une fibre — c’est-à-dire une particule mesurant au moins 5 µm de long, moins de 3 µm d’épaisseur, avec un rapport longueur/largeur supérieur ou égal à 3/1 — peuvent s’appliquer efficacement à la lutte contre la cancérogenèse (Browne, 1994). La théorie actuelle de la cancérogenèse d’origine asbestosique implique les fibres courtes aussi bien que les longues (Lippmann, 1995). De plus, l’existence d’un gradient de fibres dans le déclenchement du mésothéliome et du cancer broncho-pulmonaire et, à un moindre degré, de l’asbestose, étant établie, il semblerait justifié de fixer les niveaux d’exposition admissibles en fonction du type de fibre. Certains pays ont résolu le problème en interdisant l’utilisation (et donc l’importation) de crocidolite et en fixant un seuil plus restrictif pour l’amosite, à savoir 0,1 f/l (McDonald et McDonald, 1987).
Les limites d’exposition admissibles correspondent à l’hypothèse, fondée sur l’ensemble des données disponibles, selon laquelle la santé humaine sera préservée si l’exposition ne dépasse pas ces limites. Leur révision, lorsqu’elle a lieu, est invariablement orientée vers des mesures plus sévères (voir le paragraphe qui précède). Néanmoins, malgré le respect des mesures de prévention sur les lieux de travail, des cas de maladie continuent d’apparaître, pour des raisons de sensibilité personnelle (taux de rétention des fibres supérieur à la moyenne, par exemple) ou du fait d’une prévention insuffisante en rapport avec certaines activités ou certains procédés de fabrication. L’application de mesures techniques, de méthodes de travail, ainsi que le recours à des matériaux de remplacement (décrits ailleurs dans le présent chapitre) sont désormais mis en œuvre à l’échelle mondiale (Gibbs, Valic et Browne, 1994) dans les grandes entreprises à l’initiative, notamment, des employeurs et des syndicats. Selon une étude mondiale sur les industries intéressées réalisée en 1986, 83% des sites de production (mines et usines d’extraction) respectent la norme de 1 f/ml; cela représente 13 499 travailleurs dans 6 pays. Cette norme est également respectée dans 96% des 167 cimenteries recensées dans 23 pays, 71% des 40 usines textiles totalisant 2 000 travailleurs dans 7 pays, et dans 97% des 64 usines de fabrication de matériaux de friction comptant 10 190 travailleurs dans 10 pays (Bouige, 1990). Toutefois, une proportion non négligeable d’entreprises appartenant à ces mêmes industries ne respectent pas la réglementation en vigueur; tous les pays, par ailleurs, n’ont pas participé à cette étude. Enfin, les bienfaits de ces mesures pour la santé ne sont statistiquement mis en évidence que dans certains pays (voir ci-dessus «Le diagnostic et le traitement»). Dans les travaux de déflocage et les petites entreprises mettant en œuvre de l’amiante ou des matériaux contenant de l’amiante, les mesures prises pour combattre le danger sont loin d’être couronnées de succès, même dans les pays industriels.
La radiographie thoracique est le principal outil de surveillance de l’asbestose, tandis que les registres des cancers et les statistiques nationales sont les instruments d’observation des cancers dus à l’amiante. En 1952, le BIT avait pris une initiative louable en vue de la surveillance à l’échelle internationale des progrès réalisés dans la lutte contre les poussières dans les mines, les galeries et les carrières, sous forme de rapports (fournis sur une base volontaire par les gouvernements) concernant principalement l’extraction du charbon et des roches dures, sans exclure l’extraction de l’amiante. Malheureusement, le suivi a laissé à désirer; le dernier rapport, reposant sur des données de 1973-1977, a été publié en 1985 (BIT, 1985). Plusieurs pays présentent des données de mortalité et de morbidité au niveau national, un excellent exemple étant le rapport sur la surveillance des maladies pulmonaires d’origine professionnelle pour les Etats-Unis (USDHSS, 1994). Ces divers rapports donnent des informations qui permettent d’interpréter les tendances et d’évaluer l’efficacité des mesures de prévention dans chaque pays. Les grandes entreprises devraient établir leurs propres statistiques de surveillance (elles le font d’ailleurs souvent), à l’instar de certains syndicats. Concernant la surveillance dans les entreprises plus petites, il peut s’avérer nécessaire de recourir à des études spécifiques à des intervalles appropriés. D’autres informations proviennent de programmes comme Surveillance of Work-related Respiratory Diseases (SWORD) au Royaume-Uni, qui recueille les données fournies régulièrement par un échantillon national de pneumologues et de médecins du travail (Meredith et McDonald, 1994), ou de rapports émanant des organismes chargés de la réparation des maladies professionnelles (qui ne donnent cependant pas toujours d’informations sur les travailleurs exposés au risque).
L’étiquetage obligatoire des produits incriminés, ainsi que l’éducation des travailleurs et du grand public sont autant d’outils efficaces pour la prévention. Alors que, dans le passé, l’information circulait par le biais des organisations de travailleurs, des organes de direction et des programmes d’éducation gérés par les syndicats, il sera possible à l’avenir d’exploiter les moyens électroniques d’information pour mettre à la disposition des intéressés toutes les bases de données existantes en matière de technologie et de médecine.
En 1988, le Congrès des Etats-Unis a demandé que l’on examine les risques potentiels pour la santé associés au travail dans les immeubles où sont présents des matériaux contenant de l’amiante (Health Effects Institute — Asbestos Research, 1991). Les résultats des nombreuses analyses d’échantillons d’air intérieur effectuées en Europe, aux Etats-Unis et au Canada ont permis d’estimer le risque encouru. Ainsi, le risque de décès prématuré dû à un cancer pour toute une vie a été estimé, dans les écoles, à 1 par million pour les sujets exposés pendant quinze ans (et, cela, pour des concentrations estimées de 0,0005 à 0,005 f/ml), et à 4 par million pour les sujets exposés pendant vingt ans dans des bâtiments à usage de bureaux (pour des concentrations estimées de 0,0002 à 0,002 f/ml). Par comparaison, le risque pour une exposition professionnelle à 0,1 f/ml (en conformité avec la limite imposée par l’OSHA pour une période de vingt ans) est estimé à 2 000 par million de personnes exposées.
Les mesures effectuées dans l’eau potable des collectivités urbaines présentent des écarts considérables: les concentrations de fibre sont soit indétectables, soit très élevées, puisqu’elles s’échelonnent entre 0,7 million f/l dans le Connecticut, aux Etats-Unis, et 1,1 million à 1,3 milliard f/l dans les régions minières du Québec (Bignon, Peto et Saracci, 1989). Une autre source de contamination peut également provenir des canalisations en amiante-ciment qui assurent la majorité de l’alimentation en eau des villes, partout dans le monde. Toutefois, un groupe de travail a revu la situation en 1987 et, sans en minimiser les risques potentiels, n’a pas considéré que cette ingestion d’amiante représentait «l’un des risques les plus importants de santé publique» (USDHHS, 1987), opinion qui concorde avec les remarques d’une monographie du CIRC (OMS) concernant l’exposition non professionnelle aux fibres minérales (Bignon, Peto et Saracci, 1989).
La première moitié du XXe siècle a été caractérisée par ce que l’on peut qualifier de négligence grave à l’égard des problèmes de santé liés à l’amiante. Avant la seconde guerre mondiale, les raisons de ce manque d’intérêt ne sont pas claires: les bases scientifiques de la prévention étaient à disposition, mais il manquait sans doute la volonté d’agir et le militantisme des travailleurs. Après la guerre, les pressions exercées par l’urbanisation pour répondre à la croissance rapide de la population mondiale ont prévalu; jointes peut-être à la fascination d’une nouvelle ère industrielle et d’un minéral «magique», elles ont détourné l’attention du danger. Après la première Conférence internationale sur les effets biologiques de l’amiante, en 1964 (Selikoff et Churg, 1965), les pathologies liées à l’amiante sont devenues une cause célèbre, non seulement par elles-mêmes, mais également parce qu’elles ont marqué le début d’une période de confrontation entre les employeurs et les travailleurs au sujet du droit des travailleurs à connaître les risques de leur métier, les mesures de prévention appropriées et les prestations financières en cas de préjudice subi. D’une manière générale, on peut dire que dans les pays ayant un régime de réparation des lésions qui ne sont pas imputables au travailleur, les maladies liées à l’amiante ont été dûment reconnues et prises en charge. Dans les pays où l’on applique la notion de responsabilité des produits et où les recours collectifs en justice sont plus courants, des travailleurs malades (et leurs avocats) ont obtenu des dommages-intérêts substantiels, tandis que d’autres ont été laissés sans ressources et n’ont reçu aucune aide. S’il est improbable que le besoin en fibres diminue dans nos sociétés, l’importance des fibres minérales par rapport aux autres fibres est toutefois susceptible de décroître. Des changements ont déjà eu lieu (voir ci-dessus «Les autres sources d’exposition»). Même si les techniques actuelles permettent de diminuer les expositions professionnelles, il demeure des chantiers et des ateliers où la réglementation est ignorée. Eu égard à l’état actuel des connaissances, aux facilités de communications internationales et grâce aussi à l’étiquetage des produits, à l’éducation des travailleurs et à la volonté des industriels, il devrait être possible d’utiliser ce minéral pour la fabrication de produits peu onéreux et durables, et, cela, à l’échelle mondiale et sans compromettre la santé des travailleurs, des fabricants, des utilisateurs ou du public en général.
Peu après la première guerre mondiale, un chercheur, Karl Schoeter, s’employait à mettre au point un matériau capable de remplacer le diamant dans les filières servant à l’étirage des fils et a fait breveter à Berlin un procédé de frittage (agglomération sous pression suivie d’un chauffage à 1 500 °C) à partir d’un mélange de poudre fine de carbure de tungstène contenant 10% de cobalt et dont le but était de produire un «métal dur». Les principales caractéristiques de ce fritté sont son extrême dureté, à peine inférieure à celle du diamant, et le maintien de ses propriétés mécaniques à haute température. Ces caractéristiques le rendent parfaitement adapté à l’étirage du métal, à la confection d’inserts soudés et d’outils à haute vitesse pour l’usinage des métaux, de la pierre et du bois, ainsi qu’à la fabrication de composants présentant une résistance élevée à l’usure et à la chaleur dans les secteurs de la mécanique, de l’aéronautique et de la balistique. L’utilisation des métaux durs est en plein essor dans le monde entier. En 1927, Krupp a créé les outils de coupe «widia» (de l’allemand «wie Diamant» — comme du diamant), nom encore utilisé aujourd’hui pour désigner les outils à plaquettes de métal dur.
Le frittage reste la technique de base pour la production des métaux durs: les procédés ont été améliorés grâce à l’introduction d’autres carbures métalliques — carbure de titane (TiC) et carbure de tantale (TaC) — et grâce au traitement des inserts amovibles en métal dur par l’adjonction d’une ou de plusieurs couches de nitrure de titane ou d’oxyde d’aluminium et d’autres composés très durs appliqués par déposition chimique ou physique en phase gazeuse (procédés CVD (Chemical vapour deposition) et PVD (Physical Vapour Deposition)). Les inserts soudés ne peuvent pas être plaqués, mais doivent être régulièrement affûtés à l’aide d’une meule diamantée (voir figures 10.24 et 10.25).
Le métal dur fritté est formé de particules de carbure métallique incorporées dans une matrice au cobalt qui fond au cours du frittage, entraînant une interaction et comblant tous les interstices. Le cobalt joue par conséquent le rôle de matériau agglomérant d’une structure dotée des caractéristiques des cermets (voir figures 10.26, 10.27 et 10.28).


Le frittage utilise des poudres très fines de carbure métallique (diamètre moyen de 1 à 9 µm) et de poudre de cobalt (diamètre moyen de 1 à 4 µm) qui sont mélangées, traitées avec une solution de paraffine, matricées, déparaffinées à faible température, préfrittées à 700-750 °C et enfin frittées à 1 500 °C (Brookes, 1992).
Lorsque le frittage s’effectue avec des méthodes inappropriées et une hygiène industrielle laissant à désirer, les poudres mises en œuvre peuvent polluer l’atmosphère et les travailleurs sont donc exposés à l’inhalation de poussières de carbure métallique et de cobalt. En dehors de la production primaire, d’autres activités peuvent exposer les travailleurs au risque d’inhalation d’aérosols de métaux durs. L’affûtage des inserts soudés sur les outils se fait normalement à sec sur des meules diamantées, mais plus souvent encore en refroidissant et en lubrifiant les meules au moyen de fluides divers, ce qui entraîne dans le premier cas la formation de poussières sèches et, dans le second, de brouillards formés de très fines gouttelettes contenant des particules métalliques. Les particules de métaux durs entrent également dans la composition des couches antiusure appliquées sur des surfaces en acier par des méthodes (revêtement par jet de plasura, notamment) reposant sur l’association d’une vaporisation de poudre et d’un arc électrique ou d’une explosion contrôlée d’un mélange gazeux porté à haute température. L’arc électrique ou le mélange explosif de gaz entraînent la fusion des particules métalliques et assurent leur impact sur les surfaces à traiter.
Les premières observations concernant les pathologies des métaux durs ont été décrites en Allemagne dans les années quarante. Ces descriptions faisaient mention de fibroses pulmonaires progressives diffuses appelées «Hartmetallungenfibrosen». Au cours des vingt années qui ont suivi, des cas analogues ont été observés et décrits dans tous les pays industriels. Les travailleurs atteints étaient, dans la majorité des cas, employés au frittage. Dès 1970, plusieurs études relèvent que la pathologie pulmonaire est due à l’inhalation de particules de métaux durs. Celle-ci n’atteint que les sujets présentant une susceptibilité individuelle et se manifeste par les symptômes suivants:
Ces affections ne frappent pas seulement les travailleurs chargés du frittage, mais toute personne susceptible d’inhaler un aérosol contenant des particules de métaux durs, en particulier de cobalt. Elles sont dues principalement, et peut-être même exclusivement, au cobalt (Co).
La définition de ces pathologies englobe désormais tout un groupe d’affections touchant l’appareil respiratoire, de gravité clinique et de pronostic différents, mais ayant en commun une réactivité individuelle variable au facteur étiologique, à savoir au cobalt.
Des données épidémiologiques et expérimentales plus récentes confirment le rôle causal du cobalt en ce qui concerne les symptômes aigus des voies respiratoires supérieures (rhinite, asthme) et les symptômes subaigus et chroniques du parenchyme bronchique (alvéolite fibrosante et fibrose interstitielle chronique).
Le mécanisme pathogène repose sur l’induction d’une réaction immunologique d’hypersensibilité au cobalt: en réalité, peu de sujets présentent une pathologie à la suite de courtes expositions à des concentrations relativement faibles de cobalt, voire après des expositions plus longues et plus intenses. Les concentrations de cobalt dans les échantillons biologiques (sang, urine, peau) ne sont pas significativement différentes entre sujets malades et sujets sains. Il n’y a aucune corrélation dose-réponse au niveau tissulaire. On a mis en évidence des anticorps spécifiques (immunoglobulines IgE et IgG) dirigés contre un composé cobalt-albumine chez les asthmatiques, et le test épicutané au cobalt est positif chez les sujets présentant une alvéolite ou une fibrose. Les aspects cytologiques de l’alvéolite giganto-cellulaire sont compatibles avec une réaction immunologique, et les symptômes aigus et subaigus ont tendance à régresser lorsque les sujets sont soustraits à l’exposition au Co (Parkes, 1994).
La base immunologique de l’hypersensibilité au Co n’a pas été, jusqu’ici, expliquée de façon satisfaisante; il n’est donc pas possi-ble d’identifier un marqueur fiable de la susceptibilité individuelle.
Des pathologies identiques à celles rencontrées chez les sujets exposés aux métaux durs ont également été observées chez les diamantaires qui utilisent des disques formés de microdiamants cimentés avec du Co et qui n’inhalent donc que du Co et des particules de diamant.
On n’a pas encore démontré si le Co pur (à l’exclusion de toute autre particule inhalée) est capable seul de produire une pathologie, en particulier une fibrose interstitielle diffuse; les particules inhalées avec le Co peuvent avoir un effet synergique ou modulateur. Les études expérimentales semblent démontrer que la réactivité biologique à un mélange de particules de Co et de tungstène est plus forte que celle due au Co seul. On ne doit donc pas s’attendre à des manifestations pathologiques importantes chez les personnes travaillant dans le secteur de la production de poudre de Co pure (Science of the Total Environment, 1994).
Les symptômes cliniques de la pathologie des métaux durs qui, d’après les connaissances étiopathogéniques actuelles, devraient être plus précisément appelées «maladies du cobalt» sont, comme cela a déjà été mentionné, aiguës, subaiguës ou chroniques.
Les symptômes aigus se manifestent par une irritation respiratoire spécifique (rhinite, laryngo-trachéite, œdème pulmonaire) et sont dus à l’exposition à de fortes concentrations de poudre ou de fumées de Co; on ne les observe qu’exceptionnellement. L’asthme est en revanche plus fréquent. Il apparaît chez 5 à 10% des travailleurs exposés à des concentrations de cobalt de 0,05 mg/m3, correspondant à la valeur seuil (Threshold Limit Value (TLV)) américaine. Les symptômes d’oppression thoracique accompagnés de dyspnée et de toux ont tendance à apparaître à la fin de la journée de travail ou pendant la nuit. Le diagnostic d’asthme bronchique allergique professionnel dû au cobalt peut être suspecté sur la base de l’anamnèse; il sera confirmé par un test de provocation bronchique spécifique qui détermine l’apparition d’une réponse bronchospastique immédiate, retardée ou mixte. Les épreuves fonctionnelles respiratoires réalisées au début et à la fin de la journée de travail peuvent contribuer au diagnostic. Les symptômes asthmatiques dus au cobalt ont tendance à disparaître lorsque le sujet est soustrait à l’exposition mais, comme pour les autres formes d’asthme allergique professionnel, les symptômes peuvent devenir chroniques et irréversibles lorsque l’exposition se poursuit pendant plusieurs années. Les sujets fortement bronchoréactifs peuvent présenter des symptômes asthmatiques d’origine non allergique, avec une réponse non spécifique à l’inhalation de cobalt et d’autres poudres irritantes. Chez un fort pourcentage des cas présentant un asthme bronchique, une réaction spécifique IgE médiée, dirigée contre un composé humain Co-séroalbumine, a été observée. Les images radiologiques ne varient pas: on ne trouve que rarement des formes mixtes d’asthme et d’alvéolite, avec anomalies radiologiques caractéristiques de l’alvéolite. Le traitement par bronchodilatateurs et l’arrêt immédiat de l’exposition professionnelle apportent une guérison complète pour les cas d’apparition récente, non encore chroniques.
Les symptômes subaigus et chroniques sont l’alvéolite fibrosante et la fibrose interstitielle progressive et diffuse (FIPD). L’expérience clinique semble indiquer que le passage de l’alvéolite à la fibrose interstitielle est un processus qui évolue progressivement et lentement. On peut trouver des cas d’alvéolite initiale pure, réversible à l’arrêt de l’exposition associée à l’administration d’une corticothérapie, ou des cas comportant déjà une composante fibrotique qui peut être améliorée sans guérir complètement à l’arrêt de l’exposition, même avec un traitement supplémentaire. Enfin, dans certains cas, la FIPD irréversible prédomine: cette éventualité est assez rare chez les travailleurs exposés, en tout cas beaucoup moins fréquente que l’allergie asthmatique.
L’alvéolite est désormais facile à étudier d’un point de vue cytologique grâce au lavage broncho-alvéolaire (LBA); elle se caractérise par une augmentation importante du nombre total de cellules, qui sont essentiellement des macrophages, avec des cellules géantes multinucléées nombreuses et l’aspect typique de cellules géantes à corps étranger, contenant parfois des inclusions cytoplasmiques (voir figure 10.29); une augmentation absolue ou relative des lymphocytes est fréquente, avec une diminution du rapport CD4/ CD8, associées à une augmentation importante des éosinophiles et des mastocytes. Plus rarement, l’alvéolite reste lymphocytaire et le rapport CD4/CD8 est inversé, comme cela se produit dans les pneumopathies d’hypersensibilité.
Les sujets présentant une alvéolite décrivent une dyspnée liée à la fatigue, une perte de poids et une toux sèche. Une crépitation est présente dans la partie inférieure du poumon avec altération fonctionnelle de type restrictif et opacités radiologiques arrondies ou irrégulières. Le test épicutané au cobalt est positif dans la majorité des cas. Chez les sujets sensibles, l’alvéolite est révélée après une période d’exposition professionnelle relativement courte, de un an à quelques années. Dans sa phase initiale, cette forme est réversible et peut même guérir complètement si le sujet est soustrait à l’exposition; les résultats sont meilleurs si cette mesure est associée à une corticothérapie.
Le développement d’une fibrose interstitielle diffuse aggrave les symptômes cliniques et accentue la dyspnée qui apparaît après un effort minime et même au repos. On assiste à une aggravation de l’insuffisance ventilatoire restrictive, en rapport avec une diminution de la diffusion alvéolo-capillaire, et à l’apparition d’opacités de type linéaire et d’images radiographiques en nid d’abeilles (voir figure 10.30). L’examen histologique est typique d’une alvéolite fibrosante de «type mural».
L’évolution est rapidement progressive; les traitements sont inefficaces et le pronostic douteux. L’un des cas diagnostiqués par un auteur a même nécessité une transplantation pulmonaire.
Le diagnostic professionnel repose sur l’anamnèse, la cytologie du LBA et le résultat du test épicutané au cobalt.
La prévention de la maladie des métaux durs, ou plus précisément de la maladie du cobalt, relève surtout de la technique. Il s’agit de protéger les travailleurs en éliminant la poudre, les fumées ou les brouillards grâce à une ventilation efficace des lieux de travail. En effet, le manque de connaissances concernant les facteurs qui déterminent l’hypersensibilité individuelle au cobalt rend impossible l’identification des sujets sensibles et tous les efforts devraient être entrepris pour diminuer les concentrations de poussières dans l’atmosphère.
Le nombre des personnes à risque est sous-estimé, car de nombreuses opérations d’affûtage sont effectuées dans de petits établissements ou par des artisans. Dans ces ateliers, la valeur seuil américaine de 0,05 mg/m3 est souvent dépassée. On peut également s’interroger sur l’intérêt de cette valeur, puisque le rôle de la relation dose-effet sur les mécanismes pathologiques et l’hypersensibilité n’a pas été complètement élucidé.
La surveillance courante devrait être assez précise pour identifier les pathologies dues au cobalt à un stade précoce. Un questionnaire annuel, destiné principalement à dépister les symptômes passagers, devrait être rempli, et un examen médical être pratiqué, comprenant des épreuves fonctionnelles respiratoires et tous autres examens appropriés. Puisqu’une bonne corrélation a été démontrée entre les concentrations de cobalt dans le milieu professionnel et l’excrétion urinaire du métal, on peut effectuer des cobalturies (CoU) deux fois par an à partir d’échantillons prélevés à la fin de la semaine de travail. Lorsque l’exposition atteint la valeur seuil, l’indice d’exposition biologique est estimé égal à 30 µg de Co/litre d’urine.
Les examens médicaux d’embauche sont destinés à rechercher la présence éventuelle d’une pathologie respiratoire préexistante et d’une hyperréactivité bronchique; ils sont utiles pour l’orientation professionnelle des travailleurs. Par ailleurs, les tests à la méthacholine sont un indicateur précieux d’hyperréactivité bronchique non spécifique et peuvent servir dans certains cas.
Il est fortement recommandé de normaliser sur le plan international les méthodes de surveillance environnementale et médicale des travailleurs exposés au cobalt.
Cet article est consacré aux pneumoconioses dues aux poussières de substances non fibreuses spécifiques. Chaque substance fera l’objet d’un bref exposé concernant ses caractéristiques minéralogiques, son importance commerciale et la pathologie pulmonaire qu’elle peut provoquer chez les travailleurs exposés.
L’aluminium est un métal léger dont les différentes formes — aluminium métal et alliages — ont de nombreuses applications commerciales (Abramson et coll., 1989; Kilburn et Warshaw, 1992; Kongerud et coll., 1994.). Les minerais qui contiennent de l’aluminium, c’est-à-dire principalement la bauxite et la cryolithe, sont composés d’associations d’aluminium et d’oxygène, de fluor et de fer. La contamination des minerais d’aluminium par la silice est très courante. L’alumine (Al2O3) est extraite de la bauxite et doit être traitée pour être utilisée comme abrasif ou catalyseur. L’aluminium métal est obtenu à partir de l’alumine par réduction électrolytique en présence de fluorure. L’électrolyse du mélange est réalisée à une température d’environ 1 000 °C avec des électrodes de carbone placées dans des creusets. L’aluminium est ensuite coulé en lingots. Dans les salles des fours, l’exposition aux poussières, fumées et gaz libérés par les divers produits présents (carbone, alumine, fluorures, dioxyde de soufre, monoxyde de carbone et hydrocarbures aromatiques) est particulièrement importante au cours du craquage de la croûte et des autres opérations de maintenance. De nombreux produits sont fabriqués à partir de plaques, de flocons, de granules et de fonte d’aluminium — ce qui se traduit par un potentiel d’expositions professionnelles considérable. L’aluminium métal et ses alliages sont utilisés dans les industries aéronautique, navale et automobile, pour la fabrication de conteneurs et d’appareils électriques ou mécaniques et dans diverses autres applications. L’aluminium en petites particules est utilisé dans les peintures, les explosifs et les dispositifs incendiaires. Pour maintenir la séparation des particules, on ajoute des huiles minérales et de la stéarine; la toxicité pulmonaire marquée des flocons d’aluminium est, semble-t-il, associée à la présence de ces huiles minérales.
Une inhalation de poussières et de fumées d’aluminium peut se produire lors de l’extraction, du traitement, de la fabrication et de l’utilisation finale des produits contenant de l’aluminium. Quel que soit le type d’exposition, elle peut provoquer une fibrose pulmonaire qui devient symptomatique et visible à la radiographie. La maladie de Shaver est une pneumoconiose grave rencontrée chez les travailleurs employés à la fabrication des abrasifs à base d’alumine; elle est responsable de nombreux décès. Les lobes supérieurs du poumon sont les plus souvent atteints et l’apparition d’un pneumothorax constitue une complication fréquente. La teneur en dioxyde de silicium est élevée dans les halles d’extraction de l’aluminium, ainsi que dans les poumons des travailleurs autopsiés, ce qui suggère une participation éventuelle de la silice au tableau clinique de cette maladie. On observe aussi, dans certains cas, des concentrations élevées de particules d’oxyde d’aluminium. Les poumons peuvent parfois présenter des bulles et un épaississement pleural. La fibrose est diffuse et comporte des zones inflammatoires à l’intérieur des poumons et des ganglions lymphatiques associés.
Les poudres d’aluminium entrent dans la fabrication des explosifs. De nombreux cas de fibrose grave et progressive ont été décrits chez les travailleurs employés à cette fabrication. Des atteintes pulmonaires ont également été observées chez les travailleurs occupés au soudage ou au polissage de l’aluminium et à l’ensachage des litières pour chats contenant du silicate d’aluminium (alunite). Toutefois, on constate des variations importantes dans les rapports concernant les pathologies dues à l’aluminium. Chez les travailleurs employés à la réduction de l’aluminium, les études épidémiologiques montrent une faible prévalence de pneumoconiose et une légère altération de la fonction respiratoire. Dans l’industrie, les composés d’alumine peuvent être présents sous diverses formes; d’après les études réalisées chez l’animal, leur toxicité pulmonaire est aussi différente. La présence de silice et d’autres poussières peut également contribuer à cette toxicité variable, tout comme les substances utilisées pour l’enrobage des particules d’aluminium. Enfin, des facteurs immunologiques joueraient également un rôle: on a mis en évidence, chez un travailleur ayant développé une maladie pulmonaire granulomateuse après avoir été exposé à des oxydes d’aluminium et à l’aluminium métal, une transformation lymphocytaire sérique.
Un syndrome asthmatique a souvent été décrit chez les travailleurs exposés aux fumées d’aluminium dans les halles d’extraction. On a incriminé les fluorures qui se dégagent des cuves d’électrolyse, mais l’agent ou les agents responsables du syndrome asthmatique n’ont pu être déterminés. Comme pour les autres asthmes d’origine professionnelle, les symptômes apparaissent souvent quatre à douze heures après l’exposition et se manifestent par une toux, une dyspnée, une oppression thoracique et une respiration sifflante. On observe parfois également une réaction immédiate. Le développement de ce type d’asthme ne semble pas être lié à des facteurs de risque comme l’atopie ou les antécédents familiaux. Après arrêt de l’exposition, les symptômes disparaissent dans la plupart des cas; cependant, deux tiers des travailleurs atteints présentent une hyperréactivité bronchique non spécifique persistante et, chez certains, la symptomatologie et l’hypersensibilité des voies aériennes persistent des années après l’arrêt de l’exposition. Le pronostic semble meilleur chez les sujets soustraits immédiatement aux facteurs déclenchants lorsque les symptômes asthmatiques deviennent manifestes. Toutefois, la maladie évolue parfois vers une obstruction définitive des voies aériennes.
Des électrodes de carbone sont utilisées dans l’électrolyse de l’aluminium et des substances que l’on sait être cancérogènes pour l’humain ont été identifiées dans les halles d’électrolyse. Plusieurs études de mortalité ont révélé un taux anormal de cancer du poumon chez les travailleurs exposés de l’industrie de l’aluminium.
Les gisements de diatomite résultent de l’accrétion des squelettes d’organismes microscopiques (Cooper et Jacobson, 1977; Checkoway et coll., 1993). Certains gisements contiennent jusqu’à 90% de silice libre. La terre à diatomées peut être utilisée dans les fonderies et entrer dans la confection des filtres, des abrasifs, des lubrifiants et des explosifs. Les travailleurs exposés peuvent développer des lésions pulmonaires caractéristiques d’une pneumoconiose simple ou compliquée. L’exploitation minière, l’extraction et le traitement de la terre à diatomées sont accompagnés d’un risque de mortalité (par pathologies respiratoires non malignes ou par cancers pulmonaires) corrélé à l’importance de l’exposition, ainsi qu’à la présence de silice cristalline.
En dehors du charbon, les deux formes courantes de carbone élémentaire sont le graphite (carbone cristallin) et le noir de carbone (Hanoa, 1983; Petsonk et coll., 1988). Le graphite est utilisé pour la fabrication des crayons en mine de plomb, la lubrification des moules de fonderie, les peintures, les électrodes, les batteries sèches et les creusets de métallurgie. Réduit en poudre fine, il possède des propriétés lubrifiantes. Quant au noir de carbone, c’est une forme partiellement décomposée utilisée dans la fabrication des pneus, des pigments, des matières plastiques, des encres et d’autres produits encore. Le noir de carbone est fabriqué à partir de combustibles fossiles par des procédés faisant intervenir une combustion partielle et une décomposition thermique.
L’inhalation de carbone et des poussières qui lui sont associées est susceptible de se produire au cours de l’extraction et du broyage du graphite naturel et au cours de la fabrication du graphite synthétique; celui-ci est produit par chauffage du charbon ou du coke de pétrole et ne contient généralement pas de silice libre.
L’exposition au graphite, naturel ou synthétique, peut provoquer une pneumoconiose. Les images radiologiques sont comparables à celles des mineurs de charbon. Plusieurs cas symptomatiques graves avec fibrose pulmonaire massive ont été décrits dans le passé, en rapport surtout avec la fabrication des électrodes de carbone utilisées en métallurgie. Des observations récentes ont montré que ce type de pathologie se rencontre en cas d’exposition à des mélanges de poussières.
La gilsonite — connue également sous le nom de uintahite — est un hydrocarbure solidifié (Keimig et coll., 1987) dont il existe quelques filons dans l’ouest des Etats-Unis. Il sert actuellement à la fabrication de joints d’étanchéité pour automobiles, d’encres, de peintures et de vernis émail. Il entre aussi dans la composition des ciments et des fluides de forage des puits de pétrole et sert d’additif dans les moules de sable utilisés en fonderie. C’est aussi un constituant de l’asphalte, de certains types de panneaux de construction et des explosifs; il est employé pour la production du graphite qui sert de modérateur et de réflecteur dans les réacteurs nucléaires. L’exposition aux poussières de gilsonite provoque de la toux et de l’expectoration. Un dépistage effectué chez 99 travailleurs a révélé des images radiologiques de pneumoconiose chez cinq d’entre eux. En revanche, cette exposition ne semble pas provoquer d’anomalie de la fonction pulmonaire.
Le gypse est un sulfate de calcium hydraté (CaSO4·2H2O) (Oakes et coll., 1982). Il entre dans la composition des panneaux de plâtre, du plâtre de Paris et du ciment Portland. Il existe plusieurs formes de minerais, souvent associés à d’autres minéraux comme le quartz. Une pneumoconiose, attribuée à une contamination par la silice, a parfois été observée chez les mineurs de gypse. L’exposition aux poussières de gypse ne s’accompagne pas d’anomalies ventilatoires.
Les huiles minérales entrent dans la composition de fluides utilisés comme produits de refroidissement, huiles de coupe et lubrifiants (Cullen et coll., 1981). De nombreux produits commerciaux et diverses denrées alimentaires contiennent des huiles végétales. Celles-ci sont susceptibles d’être dispersées dans l’air sous forme de brouillards et d’être inhalées lors de l’usinage de métaux lubrifiés ou au cours de la vaporisation d’huile à des fins de nettoyage ou de lubrification. Les mesures effectuées dans les ateliers de construction mécanique ont mis en évidence des concentrations d’huile dans l’air pouvant atteindre 9 mg/m3. Une étude évoque la possibilité d’une exposition lors de la combustion des graisses animales et végétales en espace clos.
Les travailleurs exposés aux brouillards d’huile développent parfois une pneumonie lipidique, semblable à celle observée chez les patients ayant inspiré des gouttes nasales d’huiles minérales ou d’autres substances huileuses. Ces pathologies s’accompagnent de toux et de dyspnée, de crépitations pulmonaires inspiratoires et de troubles de la fonction pulmonaire généralement bénins. Quelques cas de modifications radiologiques plus importantes et de troubles plus sévères de la fonction pulmonaire ont été décrits. L’exposition aux huiles minérales a également été associée dans plusieurs études à une augmentation du risque de cancer des voies respiratoires.
Le ciment Portland est composé de silicates de calcium hydratés, d’oxyde d’aluminium, d’oxyde de magnésium, d’oxyde de fer, de sulfate de calcium, d’argile, de schiste et de sable (Abrons et coll., 1988; Yang et coll., 1993). Le mélange est broyé et calciné à haute température avec ajout de gypse. Ce ciment a de nombreuses applications dans le bâtiment et les travaux publics.
La silicose semble être le risque le plus important chez les travailleurs en contact avec le ciment Portland, suivie des pneumoconioses à poussières mixtes (autrefois, on ajoutait de l’amiante au ciment pour améliorer ses propriétés). Les radiographies thoraciques anormales montrent de petites opacités arrondies ou irrégulières et des lésions pleurales. Parfois, l’inhalation des poussières de ciment provoque une protéinose alvéolaire pulmonaire. Certaines études ont également montré des lésions en rapport avec une obstruction des voies aériennes.
Les métaux des terres rares ou lanthanides sont des éléments dont les propriétés chimiques sont très voisines. Leur nombre ou numéro atomique est compris entre 57 et 71. Le lanthane (nombre atomique 57), le cérium (58) et le néodyme (60) sont les plus courants de la série. Les autres éléments sont le praséodyme (59), le prométhium (61), le samarium (62), l’europium (63), le gadolinium (64), le terbium (65), le dysprosium (66), l’holmium (67), l’erbium (68), le thulium (69), l’ytterbium (70) et le lutétium (71) (Hussain, Dick et Kaplan, 1980; Sabbioni, Pietra et Gaglione, 1982; Vocaturo, Colombo et Zanoni, 1983; Sulotto, Romano et Berra, 1986; Waring et Watling, 1990; Deng et coll., 1991). Ces éléments se rencontrent naturellement dans les sables de monazite, dont ils sont extraits. Ils sont utilisés, alliés à d’autres métaux, comme abrasifs pour le polissage des miroirs et des lentilles, dans la fabrication des céramiques réfractaires, des feux d’artifice et des pierres à briquet. Dans l’industrie électronique, ils sont utilisés dans le soudage électrique et dans divers composants: cathodes luminescentes pour la télévision, écrans de radiographie, lasers, appareils à micro-ondes, isolants, condensateurs et semi-conducteurs.
Les lanthanides entrent également dans la fabrication des électrodes de charbon des lampes à arc utilisées dans l’imprimerie, la photogravure et la lithographie ou des projecteurs et des lampes d’éclairage utilisés en particulier dans l’industrie cinématographique avant l’avènement des lampes à argon et à xénon. Les oxydes des terres rares sont incorporés dans le cœur des électrodes de charbon pour stabiliser le faisceau de l’arc. Les fumées émises par les lampes à arc sont constituées d’un mélange de substances gazeuses et particulaires composé d’environ 65% d’oxydes de lanthanides, de 10% de fluorures, de carbone imbrûlé et d’impuretés.
Les pneumoconioses des travailleurs exposés aux métaux des terres rares se caractérisent principalement par la présence d’infiltrats nodulaires bilatéraux sur les radiographies du thorax. Il s’agit d’une fibrose interstitielle accompagnée soit d’une accumulation de fines particules de poussières granulaires, soit de lésions granulomateuses.
Le retentissement sur la fonction pulmonaire est variable et peut se caractériser par un syndrome restrictif ou mixte. Toutefois, la gamme des pathologies pulmonaires liées à l’inhalation des lanthanides reste à définir, car les données concernant le tableau et l’évolution de la maladie, ainsi que les modifications histologiques, sont encore rares.
Le cas isolé d’un cancer pulmonaire suggère que les isotopes des lanthanides pourraient être aussi cancérogènes, en raison peut-être des rayonnements ionisants émis par les radio-isotopes naturels de ces éléments.
Les couches sédimentaires sont formées par différents processus physico-chimiques: désagrégation des roches, érosion, déplacement, déposition et diagenèse. Les gisements peuvent être classés en deux catégories: les roches sédimentaires détritiques, correspondant à l’accumulation mécanique de débris d’érosion, et les roches sédimentaires physico-chimiques, qui correspondent à des carbonates, des coquilles de squelettes organiques et des dépôts salins. Les sédiments de carbonates, de sulfates et d’halogénures fournissent des minéraux relativement purs cristallisés à partir de solutions enrichies. La plupart des matériaux sédimentaires sont très solubles, si bien qu’ils sont rapidement éliminés des poumons et ne sont en général que faiblement pathogènes. En revanche, les travailleurs exposés à certains composés sédimentaires, en particulier de nature détritique, peuvent présenter des lésions de type pneumoconiotique.
Le minerai de phosphate, Ca5(F,Cl)(PO4)3, est utilisé pour la production d’engrais, de compléments alimentaires, de dentifrices, d’agents de conservation, de détergents, de pesticides, de raticides et d’explosifs (Dutton et coll., 1993). L’extraction et le traitement du minerai peuvent être à l’origine de divers types d’expositions irritantes. Les études réalisées chez les travailleurs des mines de phosphates ont montré une augmentation de la symptomatologie irritative (toux, expectoration), ainsi que des images radiographiques de pneumoconiose, mais sans signe réel d’altération de la fonction pulmonaire.
Le schiste est un mélange de substances organiques composé principalement de carbone, d’hydrogène, d’oxygène, de soufre et d’azote (Rom, Lee et Craft, 1981; Seaton et coll., 1981). La composante minérale (le kérogène) est présente en fortes concentrations dans les schistes bitumineux, roches sédimentaires stratifiées de couleur gris-brun dont on peut extraire par distillation une huile minérale semblable au pétrole. En Ecosse, l’huile de schiste est utilisée comme source d’énergie depuis 1850. Des gisements importants existent aux Etats-Unis, en Ecosse et en Estonie. Les poussières présentes dans l’atmosphère des mines de schiste souterraines sont relativement finement dispersées puisqu’elles sont composées à 80% de particules inférieures à 2 µm.
La pneumoconiose due aux poussières de schiste est appelée schistose. Les poussières créent une réaction granulomateuse et fibrotique dans les poumons. Cette pneumoconiose est comparable cliniquement à la pneumoconiose des houilleurs et à la silicose; elle peut évoluer vers une fibrose massive même après rupture avec le milieu de travail.
Au point de vue anatomopathologique, les poumons présentent des déformations vasculaires et bronchiques, avec un épaississement irrégulier des septa interalvéolaires et interlobulaires. Outre la fibrose interstitielle, ils présentent parfois un élargissement des hiles lié au transport des particules de schiste et au développement ultérieur de lésions sclérotiques bien définies au niveau des ganglions lymphatiques hilaires.
Les travailleurs de l’industrie du schiste ont deux fois et demie plus de bronchites chroniques que les témoins du même âge. Les effets de l’exposition aux poussières de schiste sur la fonction pulmonaire n’ont pas été étudiés de façon systématique.
L’ardoise est une roche métamorphique composée de divers minéraux, argiles et substances carbonées (McDermott et coll., 1978). Les constituants principaux de l’ardoise sont la muscovite, le chlorite, la calcite et le quartz, ainsi que le graphite, la magnétite et le rutile. Ils ont subi une métamorphose pour former une roche cristalline dense, résistante mais facilement séparable par clivage; ces propriétés expliquent l’importance économique de l’ardoise. Utilisée généralement pour la couverture des toits, elle sert également à la fabrication de revêtements, de carrelages, de panneaux, d’appuis de fenêtres, de tableaux noirs, de crayons, de tables de billard et de paillasses de laboratoires. L’ardoise concassée est utilisée pour la construction des routes et des courts de tennis. Les paillettes ont un pouvoir couvrant utilisé dans la fabrication des imitations d’ardoise.
L’existence d’une pneumoconiose a été décrite chez un tiers des travailleurs étudiés dans l’industrie de l’ardoise du nord du pays de Galles et chez 54% des fabricants de crayons d’ardoise en Inde. Les images radiographiques pulmonaires sont variables chez les ardoisiers. La pneumoconiose présente parfois des aspects caractéristiques de la silicose lorsque les ardoises et les roches encaissantes ont une teneur élevée en quartz. La prévalence des symptômes respiratoires est élevée chez les ardoisiers, et la proportion de travailleurs symptomatiques augmente avec la gravité de la pneumoconiose, indépendamment du tabagisme. Dans les cas graves, le volume expiratoire maximal seconde (VEMS) et la capacité vitale (CV) sont souvent diminués.
Les poumons des mineurs exposés aux poussières d’ardoise révèlent des régions circonscrites de fibrose périvasculaire et péribronchique, évoluant vers la formation de macules et une fibrose interstitielle majeure. Les lésions typiques sont constituées de macules fibrotiques de configurations variables, intimement associées aux petits vaisseaux pulmonaires.
Le talc est un silicate de magnésium; il existe sous plusieurs formes (Vallyathan et Craighead, 1981; Wegman et coll., 1982; Stille et Tabershaw, 1982; Wergeland, Andersen et Baerheim, 1990; Gibbs, Pooley et Griffith, 1992).
Les gisements de talc sont souvent contaminés par d’autres minéraux, en particulier la trémolite, fibreuse ou non fibreuse, et le quartz. De ce fait, les manifestations pathologiques pulmonaires constatées chez les travailleurs au contact du talc peuvent être en rapport soit avec le talc lui-même, soit avec les autres minéraux associés.
La production de talc est surtout importante en Australie, en Autriche, en Chine, en France et aux Etats-Unis. Le talc entre dans la composition de plusieurs centaines de produits: peintures, produits pharmaceutiques, cosmétiques, céramiques, pneus, papiers, etc.
L’exposition au talc est à l’origine d’images radiographiques caractérisées par des opacités parenchymateuses arrondies ou irrégulières diffuses et des anomalies pleurales. Selon le type d’exposition, ces opacités peuvent être liées au talc lui-même ou à la présence de polluants au sein du talc. L’exposition au talc s’accompagne de toux, de dyspnée et d’expectoration. Les épreuves fonctionnelles respiratoires sont caractéristiques d’une obstruction des voies aériennes. L’anatomopathologie révèle diverses formes de fibrose pulmonaire, avec présence de lésions granulomateuses, de corps ferrugineux et de macrophages chargés de poussières rassemblés autour des bronchioles respiratoires avec des faisceaux de collagène. L’examen minéralogique du tissu pulmonaire des travailleurs du talc donne des résultats variables et peut révéler la présence de silice, de mica ou d’un mélange de silicates.
Les gisements de talc pouvant être associés à l’amiante et à d’autres fibres, il n’est pas surprenant de constater une augmentation du risque de cancer broncho-pulmonaire chez les mineurs et les travailleurs chargés de l’extraction du talc. Des études sur les travailleurs exposés au talc sans association de fibres d’amiante ont montré une tendance à l’augmentation de la mortalité liée à des pathologies respiratoires non malignes (silicose, silico-tuberculose, emphysème et pneumonie) sans élévation du risque de cancer broncho-pulmonaire.
L’exposition aux laques pour cheveux peut avoir lieu à domicile ou dans les salons de coiffure (Rom, 1992b). Les mesures effectuées dans les instituts de beauté indiquent la possibilité d’une exposition à des aérosols respirables. Plusieurs observations ont incriminé la laque dans l’apparition d’une pneumopathie — la thésaurismose — chez les sujets fortement exposés. Les symptômes cliniques relevés dans ces observations sont généralement bénins et disparaissent à l’arrêt de l’exposition. L’étude histologique montre généralement un processus granulomateux dans le tissu pulmonaire et une hypertrophie des ganglions lymphatiques hilaires, avec épaississement des parois alvéolaires et présence de nombreux macrophages granulaires dans les espaces aériens. Les macromolécules présentes dans les laques, y compris les laques en feuille et la polyvinylpyrrolidone, pourraient être les agents potentiels de la maladie. Toutefois, contrairement aux observations cliniques rapportées, l’augmentation des images radiographiques parenchymateuses pulmonaires observées dans les études radiologiques systématiques réalisées chez des coiffeurs n’a pu être corrélée de façon concluante avec l’exposition à la laque. Bien que les résultats de ces études ne permettent pas de tirer des conclusions définitives, il semble que l’apparition d’une pathologie pulmonaire importante en rapport avec l’exposition à la laque capillaire ne soit pas habituelle.
On regroupe sous le terme de broncho-pneumopathies chroniques non spécifiques (BPCNS) tous les troubles respiratoires chroniques qui se manifestent par une dyspnée, une toux, une expectoration et une atteinte fonctionnelle respiratoire d’importance variable. Initialement, la définition de la BPCNS, acceptée lors du Symposium Ciba en 1959, incluait la bronchite chronique, l’emphysème et l’asthme. Par la suite, la terminologie diagnostique de la bronchite chronique a été redéfinie en fonction d’un concept selon lequel la limitation invalidante du débit respiratoire représente le stade ultime d’un processus évolutif qui commence par une expectoration bénigne due à l’inhalation prolongée ou récidivante de produits irritants pour les bronches (c’est l’«hypothèse britannique»). Cette notion a été remise en question en 1977 et, depuis, l’hypersécrétion et l’obstruction des voies aériennes sont considérées comme des processus indépendants. L’autre hypothèse, appelée «hypothèse hollandaise», tout en reconnaissant le rôle du tabagisme et de la pollution de l’air dans l’étiologie de la limitation chronique du débit respiratoire, souligne le rôle fondamental et éventuellement causal de l’hypersensibilité de l’hôte qui se manifeste, par exemple, par une tendance asthmatique. Les études ultérieures ont montré que ces deux hypothèses peuvent contribuer à la compréhension de l’histoire naturelle des atteintes chroniques des voies respiratoires. Même si l’on admet généralement que la valeur pronostique du syndrome hypersécrétoire est insignifiante, des études récentes ont montré une association significative entre les troubles hypersécrétoires et l’augmentation du risque de limitation de la ventilation et de la mortalité respiratoire.
Actuellement, le sigle BPCNS associe deux catégories majeures de pathologies respiratoires chroniques: l’asthme, abordé dans un précédent article de ce chapitre, et les broncho-pneumopathies chroniques obstructives (BPCO).
Dans un document publié par la Société américaine de chirurgie thoracique (American Thoracic Society (ATS)) en 1987, la BPCO est définie comme une pathologie caractérisée par des anomalies des épreuves fonctionnelles respiratoires, surtout expiratoires, et ne se modifiant pas de façon importante au cours de périodes d’observation de plusieurs mois. Prenant en compte les causes fonctionnelles et structurelles de la limitation de la ventilation, la définition inclut la bronchite chronique, l’emphysème et les pathologies des voies respiratoires périphériques. La caractéristique commune à toutes les BPCO est la présence de lésions physiopathologiques marquées, se manifestant principalement par une limitation ventilatoire chronique (LVC), de sévérité variable, mais toujours présente.
La bronchite chronique est définie comme un trouble de l’appareil respiratoire se caractérisant par une toux persistante et productive, due à une hypersécrétion de mucus dans les voies aériennes. A des fins épidémiologiques, le diagnostic de bronchite chronique repose sur un questionnaire normalisé MRC (Medical Research Council, 1960) ou ATS concernant la symptomatologie respiratoire. La bronchite chronique est définie par une toux productive pendant au moins trois mois par an pendant deux années successives.
L’emphysème est défini comme une lésion anatomique du poumon se caractérisant par un élargissement anormal des espaces aériens situés au-delà des bronchioles terminales, accompagné d’une destruction de l’architecture acinaire. L’emphysème coexiste souvent avec une bronchite chronique.
L’expression maladie des voies respiratoires périphériques ou maladie des petites voies aériennes est utilisée pour décrire les lésions des voies aériennes inférieures à 2 ou 3 mm de diamètre. Cette partie de l’arbre bronchique présente souvent une inflammation, une obstruction et une production excessive de mucus dans des maladies comme la bronchite chronique ou l’emphysème. Les données anatomopathologiques montrent des lésions structurelles locales qui peuvent représenter un stade précoce de l’évolution des broncho-pneumopathies chroniques, si bien qu’à la fin des années soixante et dans les années soixante-dix on a mis au point des épreuves fonctionnelles spécifiquement conçues pour examiner les propriétés physiologiques de ces voies aériennes périphériques. Par conséquent, l’expression maladie des voies respiratoires périphériques désigne généralement des lésions structurelles ou un déficit fonctionnel.
Les BPCO se caractérisent par une LVC, indiquant une augmentation des résistances pulmonaires et un ralentissement du débit ventilatoire au cours de l’expiration forcée. Pour définir la LVC et ses corollaires clinique et physiopathologique, deux critères diagnostiques sont importants. Premièrement, la maladie doit avoir une évolution chronique; les premières recommandations de 1958 exigeaient d’ailleurs la présence d’une LVC pendant plus d’un an pour répondre aux critères diagnostiques. Le cadre temporel suggéré récemment est moins rigoureux puisqu’il est de trois mois. Dans le domaine des LVC liées au travail, l’examen spirométrique standard fournit des données suffisantes pour détecter une LVC, basées sur la diminution du volume expiratoire maximal seconde (VEMS) ou du rapport VEMS/capacité vitale forcée (CVF).
Généralement, on diagnostique une LVC lorsque le VEMS est inférieur à 80% de la valeur théorique. Conformément à la classification fonctionnelle des LVC recommandée par l’ATS, l’insuffisance est:
Lorsque l’insuffisance est évaluée par le rapport VEMS/CVF, elle est considérée comme bénigne si le rapport est compris entre 60 et 74%, modérée si le rapport est compris entre 41 et 59%, et sévère si le rapport est inférieur ou égal à 40%.
Toutes les études montrent que les BPCO constituent un problème courant dans de nombreux pays. Leur prévalence est plus élevée chez les hommes que chez les femmes et augmente avec l’âge. La bronchite chronique, forme diagnostique bien standardisée des BPCO, est deux à trois fois plus fréquente chez l’homme que chez la femme: les études à grande échelle montrent que 10 à 20% des hommes adultes de la population générale répondent aux critères diagnostiques de bronchite chronique (voir tableau 10.18). La maladie est beaucoup plus répandue chez les fumeurs, hommes ou femmes. La relation entre la BPCO et le travail est abordée ci-après.
|
Pays |
Année |
Population étudiée |
Hommes |
Femmes |
||||
|
Tabac (%) |
BC (%) |
BPCO/LVC (%) |
Tabac (%) |
BC (%) |
BPCO/LVC (%) |
|||
|
Etats-Unis |
1978 |
4 699 |
56,6 |
16,5 |
n.r. |
36,2 |
5,9 |
n.r. |
|
Etats-Unis |
1982 |
2 540 |
52,8 |
13,0 |
5,2 |
32,2 |
4,1 |
2,5 |
|
Royaume-Uni |
1961 |
1 569 |
n.r. |
17,0 |
n.r. |
n.r. |
8,0 |
n.r. |
|
Italie |
1988 |
3 289 |
49,2 |
13,1 |
n.r. |
26,9 |
2,8 |
n.r. |
|
Pologne |
1986 |
4 335 |
59,6 |
24,2 |
8,5 |
26,7 |
10,4 |
4,9 |
|
Népal |
1984 |
2 826 |
78,3 |
17,6 |
n.r. |
58,9 |
18,9 |
n.r. |
|
Japon |
1977 |
22 590 |
n.r. |
5,8 |
n.r. |
n.r. |
3,1 |
n.r. |
|
Australie |
1968 |
3 331 |
n.r. |
6,3 |
n.r. |
n.r. |
2,4 |
n.r. |
Légende: Tabac = tabagisme. BC = bronchite chronique. BPCO/LVC = broncho-pneumopathie chronique obstructive/limitation ventilatoire chronique. n.r. = non rapporté.
Modifié avec l�aimable autorisation de Woolcock, 1989.
Les BPCO sont des maladies à étiologie multifactorielle qui dépendent de nombreux facteurs de risque, liés à l’hôte et à l’environnement. Le rôle de l’exposition professionnelle a été reconnu à la suite de plusieurs études épidémiologiques publiées entre 1984 et 1988. On a confirmé récemment que le tabagisme et les expositions professionnelles ont des effets indépendants, d’après les résultats des études publiées de 1966 à 1991. Le tableau 10.19 résume l’état actuel des connaissances sur l’étiologie multifactorielle des BPCO.
|
Facteur lié à |
Etabli |
Probable |
|
Hôte |
Sexe |
Atopie |
|
Environnement |
Tabagisme (actif) |
Tabagisme (passif) |
Avec l�aimable autorisation de Becklake et coll., 1988.
L’apparition d’une bronchite chronique dans une catégorie professionnelle donnée peut être le signe d’une exposition à des agents irritants sur le lieu de travail. On a montré que l’exposition à des poussières industrielles avait un effet significatif sur le développement des bronchites chroniques chez les mineurs de charbon et chez les travailleurs de la sidérurgie, de l’industrie textile, du bâtiment et de l’agriculture. De façon générale, les environnements fortement empoussiérés sont associés à une prévalence plus élevée des symptômes d’hypersécrétion chronique. Les études de prévalence sont néanmoins soumises à «l’effet du travailleur en bonne santé», un biais qui se traduit par une sous-estimation du retentissement sur la santé des expositions professionnelles dangereuses. A ce titre, les données sur l’incidence de la maladie sont plus concluantes, quoique plus rares. Dans certaines activités professionnelles, le taux d’incidence de la bronchite chronique est élevé: il atteint 197-276/10 000 chez les agriculteurs, 380/10 000 chez les travailleurs de la construction mécanique et 724/10 000 chez les mineurs et les carriers, contre 108/10 000 chez les employés de bureau.
Ce profil particulier, ainsi que la participation active du tabagisme, corrobore la notion selon laquelle l’inhalation chronique d’agents irritants respiratoires aboutit à la bronchite chronique, qui représente une réponse commune.
Il semble que l’effet délétère des poussières inhalées soit de produire une inflammation chronique non spécifique de la paroi bronchique. Ce type de réponse inflammatoire a d’ailleurs été documenté chez des travailleurs exposés à des poussières organiques et à leurs constituants, comme, par exemple, les céréales et leurs endotoxines, responsables d’une inflammation neutrophile. Le rôle de la sensibilité individuelle ne peut pas être écarté; les facteurs connus en rapport avec l’hôte sont la présence d’antécédents d’infection respiratoire, l’efficacité des mécanismes d’élimination et des facteurs génétiques encore mal déterminés, tandis que le tabagisme reste la cause environnementale prépondérante.
La contribution des expositions professionnelles à l’étiologie de l’emphysème n’est pas encore bien comprise. D’après les observations expérimentales, les facteurs généralement admis sont les oxydes d’azote, l’ozone et le cadmium. Les données épidémiologiques obtenues dans le milieu professionnel sont moins convaincantes et peuvent être difficiles à rassembler, car les niveaux d’exposition sont généralement faibles, tandis que le tabagisme a un effet prédominant. Ce facteur est particulièrement important dans le cas de la pathologie dite de l’emphysème centro-acinaire. L’autre forme de la maladie, l’emphysème panacinaire, est considérée comme héréditaire et corrélée à un déficit en alpha1-antitrypsine.
Une inflammation bronchiolaire et péribronchiolaire, accompagnée d’un rétrécissement progressif du segment atteint de l’arbre bronchique (maladie des voies respiratoires périphériques ou bronchiolite constrictive), peut parfois être observée à un moment quelconque de l’évolution de la maladie. Dans le milieu professionnel, la maladie fait généralement suite à une lésion pulmonaire aiguë liée à l’inhalation de vapeurs toxiques (dioxyde de soufre, ammoniac, chlore et oxydes d’azote). Toutefois, l’épidémiologie professionnelle relative à la bronchiolite constrictive n’est pas claire. Apparemment, les stades précoces sont difficiles à identifier en raison de la symptomatologie non spécifique et des limites des procédures diagnostiques. La maladie peut passer inaperçue jusqu’à l’apparition d’une symptomatologie patente et d’une insuffisance respiratoire objective (limitation chronique du débit respiratoire). Les cas observés à la suite d’accidents industriels sont mieux connus.
Il n’est pas rare de trouver des cas de LVC dans différents groupes professionnels; sa prévalence peut être plus grande chez les travailleurs manuels que chez les employés de bureau, comme l’ont montré des études contrôlées. Les premiers travaux portant sur l’association de la limitation chronique de la ventilation et de l’exposition professionnelle n’ont pas été concluants en raison de l’étiologie complexe de la LVC, notamment l’effet du tabagisme et des facteurs de risque liés à l’hôte. L’épidémiologie professionnelle actuelle, qui a recours à des protocoles plus spécifiques et à une modélisation des relations exposition-réponse, a permis de mettre en évidence une association entre la capacité ventilatoire et l’exposition aux poussières d’origine minérale ou organique, aux fumées et aux gaz.
Des études longitudinales réalisées chez des travailleurs exposés à des poussières minérales et organiques, à des fumées ou à des gaz montrent que les expositions professionnelles sont associées à une diminution de la fonction pulmonaire. Les résultats résumés dans le tableau 10.20 font ressortir un effet significatif des expositions aux poussières dans les mines de charbon et de fer, l’industrie de l’amiante-ciment, les aciéries et les fonderies, ainsi que l’industrie du papier. La plupart des expositions sont composées de poussières et de fumées (hydrocarbures non halogénés, peintures, résines et vernis) ainsi que de gaz (dioxyde de soufre ou oxydes d’azote). D’après les résultats d’une étude exhaustive limitée aux travaux les plus significatifs concernant les BPCO et l’exposition professionnelle aux poussières, on peut estimer que sur 1 000 mineurs de charbon non fumeurs, 80 seront susceptibles de présenter une diminution d’au moins 20% de leur VEMS après trente-cinq ans de travail dans une atmosphère accusant une concentration moyenne de poussières respirables de 2 mg/m3, alors que dans les mines d’or, les non-fumeurs pourront avoir un risque trois fois plus élevé.
|
Pays (année) |
Sujets et expositions |
Examen de référence |
Diminution moyenne de la fonction pulmonaire en un an* |
|||
|
|
NE |
E |
NF |
F |
||
|
Royaume-Uni (1982) |
1 677 mineurs de charbon |
VEMS ml |
37 |
41 (moyenne) |
37 |
48 |
|
Etats-Unis (1985) |
1 072 mineurs de charbon |
VEMS ml |
40 |
47 |
40 |
49 |
|
Italie (1984) |
65 travailleurs dans l�industrie de l�amiante-ciment |
VEMS ml |
9 |
49 |
Non communiqué |
Non communiqué |
|
Suède (1985) |
70 travailleurs dans l�industrie de l�amiante-ciment |
VEMS % |
4,2 |
9,2 |
3,7 |
9,4 |
|
France (1986) |
871 mineurs de fer |
VEMS % |
6 |
8 |
5 |
7 |
|
France (1979) |
159 travailleurs de l�industrie de l�acier |
VEMS % |
0,6 |
7,4 |
Non communiqué |
Non communiqué |
|
Canada (1984) |
179 mineurs et travailleurs de fonderie |
VEMS/CVF % |
1,6 |
3,1 |
2,0 |
3,4 |
|
France (1982) |
556 travailleurs en usine |
VEMS ml |
42 |
50 |
40 |
48 |
|
Finlande (1982) |
659 travailleurs de l�industrie du papier |
VEMS ml |
Pas d�effet |
Pas d�effet |
37 |
49 |
|
Canada (1987) |
972 mineurs et travailleurs de fonderie |
VEMS ml |
— |
69 (fours de grillage de minerais) |
41 |
54 |
* Le tableau indique la diminution annuelle moyenne de la fonction pulmonaire chez les personnes exposées (E) par rapport aux non exposées (NE), de même que chez les fumeurs (F) par rapport aux non-fumeurs (NF). Les effets indépendants du tabagisme (F) ou de l�exposition se sont révélés non significatifs dans les analyses effectuées par les auteurs dans toutes les études (sauf pour la Finlande).
Modifié avec l�aimable autorisation de Becklake, 1989.
Certaines études effectuées chez les céréaliers montrent les effets de l’exposition professionnelle aux poussières organiques sur les modifications longitudinales de la fonction pulmonaire. Bien que limités par le nombre et la durée du suivi, les résultats font ressortir une relation indépendante entre le tabagisme et la diminution annuelle de la fonction respiratoire (par rapport à l’exposition aux poussières de céréales).
Le trouble physiopathologique central des BPCO est une limitation ventilatoire chronique. Ce trouble est dû au rétrécissement des voies respiratoires — mécanisme complexe dans la genèse de la bronchite chronique — tandis que dans l’emphysème, l’obstruction des voies respiratoires est principalement due à une faible rétraction élastique du tissu pulmonaire. Les deux mécanismes coexistent souvent.
Les lésions structurelles et fonctionnelles observées dans la bronchite chronique incluent une hypertrophie et une hyperplasie des glandes sous-muqueuses associées à une hypersécrétion de mucus. L’inflammation conduit à une hyperplasie de la musculature lisse et à une hypertrophie des muqueuses. L’hypersécrétion muqueuse et le rétrécissement des voies aériennes favorisent les infections bactériennes et virales de l’arbre respiratoire, ce qui peut également augmenter l’obstruction des voies aériennes.
La limitation ventilatoire de l’emphysème est en rapport avec la diminution de la rétraction élastique, conséquence d’une destruction des fibres d’élastine et d’un collapsus de la paroi bronchiolaire lié à la compliance pulmonaire élevée. La destruction des fibres d’élastine est probablement due à un déséquilibre du système protéolyse-antiprotéolyse, par un processus également appelé protéases-antiprotéases. L’alpha1-antitrypsine est une protéase très puissante qui inhibe l’effet de l’élastase sur les alvéoles humaines. Les neutrophiles et les macrophages qui libèrent l’élastase s’accumulent en réponse aux médiateurs inflammatoires locaux et à l’inhalation de divers agents irritants respiratoires, en particulier la fumée de tabac. Les autres inhibiteurs sont moins puissants; il s’agit de l’alpha2-macroglobuline et de l’inhibiteur de l’élastase à faible poids moléculaire, libérés par les glandes sous-muqueuses.
Récemment, on a évoqué la possibilité d’un déficit en antioxydants comme mécanisme pathogène de l’emphysème. Selon cette hypothèse, les agents oxydants, s’ils ne sont pas inhibés par des antioxydants, peuvent provoquer, dans le tissu pulmonaire, des lésions conduisant à l’emphysème. Les oxydants connus incluent des facteurs exogènes (ozone, chlore, oxydes d’azote et fumée de tabac) et des facteurs endogènes, comme les radicaux libres. Les facteurs antioxydants les plus importants sont des antioxydants naturels (comme les vitamines E et C, la catalase, la superoxyde dysmutase, le glutathion, la céruloplasmine) et des antioxydants synthétiques (comme la N-acétylcystéine et l’allopurinol). Des données de plus en plus nombreuses montrent qu’il y a une synergie entre les déficits en antioxydants et les déficits en inhibiteurs de protéases dans la pathogenèse de l’emphysème.
D’un point de vue anatomopathologique, la bronchite chronique se caractérise par une hypertrophie et une hyperplasie des glandes sous-muqueuses au niveau des grosses voies aériennes. Par conséquent, le rapport entre l’épaisseur de la glande bronchique et l’épaisseur de la paroi bronchique (appelé index de Reid) augmente. Les autres anomalies ou pathologies sont la métaplasie de l’épithélium ciliaire, l’hyperplasie de la musculature lisse et la présence d’infiltrats de neutrophiles et de lymphocytes. Les modifications observées dans les grosses bronches sont souvent accompagnées d’anomalies dans les petites bronchioles.
Les lésions anatomopathologiques constatées dans les petites bronchioles illustrent les différents degrés du processus inflammatoire qui touche les parois des voies aériennes. Après l’introduction du concept de maladie des petites voies aériennes, on s’est intéressé à la morphologie des différents segments bronchiolaires. L’étude histologique des bronchioles muqueuses, étendue ultérieurement aux bronchioles respiratoires, montre une inflammation de la paroi, une fibrose, une hypertrophie musculaire, des dépôts pigmentaires, des cellules caliciformes et une métaplasie squameuse, ainsi que la présence de macrophages intraluminaires. Les lésions anatomopathologiques décrites ci-dessus ont été appelées «maladies des voies aériennes induites par les poussières minérales». Ce segment de l’arbre respiratoire présente aussi un autre type de lésion, l’alvéolite fibrosante péribronchiolaire, qui représente la première réaction du tissu pulmonaire à l’inhalation de poussières minérales.
Les lésions anatomopathologiques de l’emphysème peuvent être classées en deux catégories: l’emphysème centro-acinaire et l’emphysème panacinaire. Dans la première entité, les lésions sont limitées au centre de l’acinus, tandis qu’elles intéressent toutes les structures de l’acinus dans l’emphysème panacinaire. Bien que l’on pense que l’emphysème panacinaire reflète un déficit héréditaire en inhibiteurs de protéases, les deux formes d’emphysème peuvent coexister. Dans tous les cas, les bronchioles terminales présentent des signes d’inflammation et les espaces aériens distaux sont anormalement élargis. La destruction structurelle intéresse les alvéoles et les capillaires et peut conduire à la formation de grands espaces aériens (emphysème bulleux). L’emphysème centro-acinaire a tendance à être localisé aux lobes pulmonaires supérieurs, tandis que l’emphysème panacinaire est généralement situé dans les lobes inférieurs.
Les deux symptômes majeurs de la bronchique chronique sont la toux chronique et l’expectoration, tandis que l’emphysème se caractérise par la présence d’une dyspnée (difficultés respiratoires). A un stade avancé, les symptômes d’expectoration chronique et de dyspnée coexistent généralement. L’apparition et la progression de la dyspnée suggèrent le développement d’une limitation ventilatoire chronique. Selon les symptômes et l’état physiologique, les manifestations cliniques de la bronchite chronique peuvent revêtir trois formes: simple, mucopurulente et obstructive.
Dans la bronchite chronique, l’auscultation thoracique peut être normale, mais dans les cas avancés, on constate parfois un allongement du temps d’expiration, des sifflements et des râles à l’expiration. En outre, la bronchite chronique avancée s’accompagne souvent de cyanose.
Le diagnostic clinique d’emphysème est difficile au stade précoce de la maladie; la dyspnée en est parfois la seule manifestation. Lorsque l’emphysème est plus évolué, le patient peut présenter un thorax en tonneau et des signes d’hyperventilation qui auront pour conséquence un tympanisme, une diminution de la course du diaphragme et du murmure vésiculaire. La cyanose est rare.
Le diagnostic différentiel entre bronchite chronique et emphysème peut être difficile, car les facteurs étiologiques sont comparables (en particulier l’effet du tabagisme), ainsi que les manifestations cliniques, surtout si la limitation ventilatoire chronique domine. Le tableau 10.21 indique certaines caractéristiques qui peuvent contribuer au diagnostic. La forme évoluée des BPCO peut être de deux types extrêmes, selon que c’est la bronchite chronique (type «blue bloater», bleu et bouffi) ou l’emphysème qui prédomine (type «pink puffer», rose et essoufflé).
|
Signes/symptômes |
Bronchite prédominante |
Emphysème prédominant |
|
Masse corporelle |
Augmentée |
Diminuée |
|
Cyanose |
Fréquente |
Rare |
|
Toux |
Symptôme prédominant |
Intermittente |
|
Expectoration |
Forte |
Rare |
|
Dyspnée |
Généralement marquée à l�effort |
Symptôme prédominant |
|
Murmure vésiculaire |
Normal ou légèrement diminué, bruits surajoutés |
Diminué |
|
Cœur pulmonaire |
Fréquent |
Rare |
|
Infections respiratoires |
Fréquentes |
Rares |
La radiologie thoracique a une valeur diagnostique limitée dans la bronchite chronique et les premiers stades d’emphysème. En revanche, un emphysème évolué a une image radiologique caractéristique avec augmentation de la transparence radiologique (distension thoracique). La tomodensitométrie permet de préciser la localisation et l’importance des lésions emphysémateuses et de différencier les emphysèmes centro-acinaire et panacinaire.
Les épreuves fonctionnelles respiratoires ont un rôle bien établi pour l’évaluation diagnostique des BPCO (voir tableau 10.22). L’évaluation fonctionnelle de la bronchite chronique et de l’emphysème comprend une série de mesures importantes, comme la capacité résiduelle fonctionnelle (CRF), le volume résiduel (VR), la capacité pulmonaire totale (CPT), le VEMS et le rapport VEMS/CV, la résistance des voies aériennes, la compliance statique, la rétraction élastique, les gaz du sang (PaO2, PaCO2) et la capacité de diffusion du monoxyde de carbone (DLCO).
|
Epreuves fonctionnelles respiratoires |
Bronchite prédominante |
Emphysème prédominant |
|
VR, CRF, CPT |
Normaux ou légèrement augmentés |
Fortement augmentés |
|
VEMS, VEMS/CV |
Diminués |
Diminués |
|
Raé |
Fortement augmentée |
Légèrement augmentée |
|
Cst |
Normale |
Fortement augmentée |
|
Pél |
Normale |
Fortement augmentée |
|
PaO2 |
Fortement augmentée |
Légèrement diminuée |
|
PaCO2 |
Augmentée |
Normale |
|
DLCO |
Normale ou légèrement diminuée |
Diminuée |
VR = volume résiduel; CRF = capacité résiduelle fonctionnelle; CPT = capacité pulmonaire totale; VEMS = volume expiratoire maximal seconde; CV = capacité vitale; Raé = résistance des voies aériennes; Cst = compliance statique; Pél = force de recul élastique pulmonaire; PaO2 et PaCO2 = gaz du sang; DLCO = capacité de diffusion du monoxyde de carbone (facteur de transfert).
Il n’est pas possible d’établir un diagnostic clinique de la maladie des petites voies aériennes. Très souvent, celle-ci accompagne une bronchite chronique ou un emphysème ou précède même les manifestations cliniques de ces deux types de BPCO. Les formes isolées de maladie des voies aériennes périphériques peuvent être étudiées par les épreuves fonctionnelles respiratoires, mais l’état fonctionnel des voies aériennes périphériques est en général difficile à évaluer. Cette partie de l’arbre bronchique participe pour moins de 20% à la résistance ventilatoire totale, et l’on considère que les lésions bénignes isolées ne peuvent être détectées par la spirométrique traditionnelle. Il existe des méthodes plus sensibles, conçues spécifiquement pour mesurer la fonction des voies aériennes périphériques et qui portent plus particulièrement sur l’évaluation des paramètres ci-après: débit expiratoire à 25 et 75% de la CVF (DEM25-75), débit à faibles volumes pulmonaires (DEM50, DEM25), courbe de rinçage à l’azote au cours d’une respiration unique, capacité de fermeture et compliance en fonction de la fréquence. De façon générale, on pense que ces épreuves ont une faible spécificité. D’un point de vue théorique, les DEM25-75 et DEM50-25 reflètent les mécanismes limitant le calibre, tandis que le rinçage à l’azote est plus spécifique des propriétés mécaniques des espaces aériens; ce sont les premiers indices qui sont utilisés plus souvent en épidémiologie professionnelle.
Les différences fondamentales entre bronchite chronique et emphysème sont présentées aux tableaux 10.21 et 10.22. Toutefois, dans certains cas individuels, le diagnostic différentiel est malaisé et parfois impossible à établir de façon satisfaisante. Dans certains cas, il est également difficile de faire la différence entre une BPCO et un asthme. En pratique, l’asthme et la BPCO ne sont pas des entités clairement différenciées mais ont tendance à se chevaucher. Dans l’asthme, l’obstruction des voies aériennes est généralement intermittente, tandis que dans la BPCO, elle est constante. L’évolution de la limitation ventilatoire est plus variable dans l’asthme que dans la BPCO.
Le traitement clinique des BPCO implique l’arrêt du tabac, mesure simple la plus efficace. L’exposition professionnelle aux agents irritants respiratoires devrait être interrompue ou évitée. Le traitement clinique devrait viser en premier lieu la prévention des infections respiratoires et comprendre une vaccination régulière contre la grippe. L’administration de bronchodilatateurs se justifie chez les patients présentant une limitation ventilatoire importante et devrait inclure des agonistes beta2-adrénergiques et des anticholinergiques administrés en monothérapie ou en association, de préférence sous forme d’aérosols. La théophylline continue à être utilisée, bien que son rôle dans le traitement des BPCO soit controversé. La corticothérapie au long cours peut être efficace dans certains cas. L’hypersécrétion bronchique est souvent enrayée grâce aux médicaments muco-actifs agissant sur la production de mucus, la structure du mucus ou l’élimination mucocilliaire. L’évaluation des effets du traitement mucolytique est difficile à réaliser, car ces médicaments ne sont pas utilisés en monothérapie dans les BPCO. Les patients présentant une hypoxémie (PaO2 ≥ 55 mm Hg) nécessitent une oxygénothérapie au long cours, traitement facilité par l’accès à des oxygénateurs portables. Un traitement supplétif avec de l alpha1-antitrypsine peut être envisagé dans les emphysèmes avec déficit en alpha1-antitrypsine confirmé (phénotype PiZZ). L’effet des produits antioxydants (comme la vitamine E et la vitamine C) sur l’évolution de l’emphysème est encore à l’étude.
La prévention des BPCO commence avec les campagnes contre le tabac s’adressant à la fois à la population en général et aux groupes professionnels à haut risque en particulier. En milieu professionnel, la prévention et la limitation des expositions aux agents irritants respiratoires sont essentiels et devraient toujours constituer une priorité. Ces activités devraient viser la réduction de la pollution de l’air en deçà des limites d’exposition admissibles. Etant donné que de nombreux polluants en suspension dans l’air ne sont pas soumis à une réglementation, tout effort destiné à réduire l’exposition se justifie. Dans les cas où il est impossible d’atteindre les résultats escomptés, le port d’un appareil de protection respiratoire s’impose pour diminuer le risque.
La prévention médicale des BPCO en milieu professionnel comprend deux étapes importantes: un programme de surveillance médicale respiratoire et un programme d’information à l’intention du personnel.
Le programme médical de surveillance respiratoire comporte une évaluation de l’état de santé du sujet sous l’angle respiratoire. Il débute par un examen initial (anamnèse, examen physique, radiographie thoracique, épreuves fonctionnelles respiratoires normalisées) et se poursuit par des examens réguliers pendant toute la période d’activité. Il permet d’évaluer l’état de santé respiratoire basal des travailleurs (et d’identifier les personnes présentant des insuffisances respiratoires subjectives ou objectives) avant l’embauche, et de détecter les premiers signes ultérieurs d’insuffisance respiratoire au cours de la surveillance régulière. Toute anomalie devrait entraîner le retrait de l’exposition et une évaluation diagnostique par un pneumologue.
Le programme d’information pour le personnel devrait reposer sur une reconnaissance fiable des risques respiratoires en milieu du travail et devrait être conçu par des professionnels de la santé, des hygiénistes industriels, des ingénieurs de sécurité et la direction. Il devrait fournir aux travailleurs toutes les données nécessaires concernant les risques respiratoires sur les lieux de travail, les effets respiratoires potentiels des expositions et la réglementation en vigueur. Il devrait également inciter les travailleurs à respecter les mesures de sécurité et souligner les bienfaits d’un mode de vie sain.
L’utilisation des fibres artificielles a augmenté, en particulier depuis les restrictions imposées à l’usage de l’amiante. La nocivité potentielle des fibres artificielles est encore à l’étude. Le présent article donne un aperçu général de leur toxicité potentielle et des différents types de fibres produites — répertoriées dans le tableau 10.23 — et fait le bilan des études récentes sur les effets de ces fibres sur la santé.
|
Fibres artificielles |
Oxyde d�aluminium |
|
|
Fibres artificielles vitreuses |
Fibre de verre |
Laine de verre |
|
|
Laine minérale |
Laine de roche |
|
|
Fibre céramique réfractaire |
|
Les principaux facteurs impliqués dans la toxicité potentielle des fibres artificielles sont:
De façon générale, ce sont les fibres longues et fines (mais de taille respirable), capables de résister à l’action du temps, qui peuvent être les plus nocives si elles atteignent les poumons en concentration suffisante. D’après les études par inhalation à court terme réalisées chez l’animal, l’inflammation, la cytotoxicité, l’altération de la fonction macrocytaire et la biopersistance sont autant de manifestations de la toxicité des fibres. Le potentiel cancérogène est plus probablement corrélé à des lésions de l’ADN cellulaire, dues à la formation de radicaux libres et de facteurs clastogènes ou à une mauvaise ségrégation chromosomique lors de la mitose cellulaire, ces phénomènes pouvant être isolés ou associés. Les fibres respirables mesurent moins de 3 à 3,5 µm de diamètre et ont une longueur inférieure à 200 µm. Selon «l’hypothèse Stanton», le potentiel cancérogène des fibres (déterminé par les études d’implantations intrapleurales chez l’animal) est corrélé à leurs dimensions (le risque est plus élevé si les fibres mesurent moins de 0,25 µm de diamètre et plus de 8 µm de longueur) et à leur durabilité (Stanton et coll., 1981). Or, les fibres minérales naturelles, comme les fibres d’amiante, ont une structure polycristalline ayant tendance à se cliver selon des plans longitudinaux, ce qui crée des fibres plus fines d’un rapport longueur/largeur plus élevé et d’une plus grande toxicité. En revanche, la grande majorité des fibres artificielles sont non cristallines ou amorphes et se clivent perpendiculairement à leur axe longitudinal pour former des fibres plus courtes. Il s’agit là d’une différence fondamentale entre l’amiante et les silicates fibreux non asbestosiques, d’une part, et les fibres artificielles, d’autre part. La longévité des dépôts de fibres dans le poumon dépend de la capacité du poumon de les éliminer, ainsi que des propriétés physiques et chimiques de ces fibres. La durabilité des fibres artificielles, en revanche, dépend des transformations qu’elles subissent en cours de fabrication, en vue de leur utilisation finale; elle peut aussi être modifiée par l’adjonction de stabilisateurs tels que l’alumine. En raison de la très grande diversité des propriétés chimiques et physiques des fibres artificielles, l’évaluation de leur potentiel toxique ne peut être réalisée qu’au cas par cas.
La toxicité des fibres d’oxyde d’aluminium cristallines a été évoquée dans un cas de fibrose pulmonaire observé chez un travailleur employé pendant dix-neuf ans dans une fonderie d’aluminium (Jederlinic et coll., 1990). Chez ce sujet, la radiographie thoracique a mis en évidence un tableau de fibrose interstitielle. L’analyse du tissu pulmonaire en microscopie électronique a révélé la présence de 1,3 x 109 fibres cristallines par gramme de tissu pulmonaire sec, soit dix fois plus que le nombre de fibres d’amiante trouvées dans le tissu pulmonaire de mineurs travaillant dans des mines de chrysotile et présentant une asbestose. D’autres études sont nécessaires pour déterminer le rôle des fibres d’oxyde d’aluminium cristallines (voir figure 10.31) dans la pathogenèse de la fibrose pulmonaire. Cette observation suggère toutefois que la formation et la propagation des fibres sont possibles lorsque les conditions environnementales le permettent, par exemple lorsqu’une zone où sont présents des matériaux en fusion est parcourue par un courant d’air intense. Si l’on suspecte une pneumoconiose professionnelle induite par les fibres, on devrait recourir à la microscopie en contraste de phase ou à la microscopie électronique avec analyse aux rayons X à dispersion d’énergie pour mettre en évidence la présence des fibres dans les échantillons d’air et de tissu pulmonaire.

Les fibres de brai carbonifère, la rayonne (viscose) ou les fibres de polyacrylonitrile forment des fibres de carbone amorphe si elles sont chauffées à 1 200 °C; si elles sont chauffées à des températures supérieures à 200 °C, elles forment des fibres de graphite cristallin (voir figure 10.32). Des résines de liaison peuvent être ajoutées pour augmenter la cohésion et la résistance mécanique et permettre le moulage et l’usinage du matériau composite. De façon générale, les fibres de carbone ou de graphite ont un diamètre compris entre 7 et 10 µm, mais leurs dimensions varient selon les procédés de fabrication et les manipulations qu’elles subissent. Les plastiques renforcés par des fibres de carbone ou de graphite sont utilisés dans les industries aéronautique et automobile et dans la fabrication d’articles de sport. L’exposition aux particules respirables de carbone ou de graphite peut avoir lieu pendant les phases de fabrication et au cours des opérations mécaniques ultérieures. Le chauffage des composites à 900-1100 °C peut aussi libérer de petites quantités de fibres respirables. Les connaissances actuelles concernant ces fibres ne permettent pas de donner une réponse définitive à la question de leur potentiel toxique. L’injection intratrachéale de différentes poussières de fibres de graphite chez le rat a donné des résultats hétérogènes; trois des échantillons de poussières étudiés ont produit une toxicité minimale, alors que dans deux cas on a noté un effet cytotoxique important sur les macrophages alvéolaires et des différences dans le nombre total de cellules récupérées à partir du poumon (Martin, Meyer et Luchtel, 1989). Des effets clastogènes ont été observés dans les études de mutagénicité réalisées avec des fibres à base de brai, mais non avec des fibres de carbone à base de polyacrylonitrile. Une étude conduite sur dix ans chez des personnes employées à la fabrication de fibres de carbone (fibres de 8 à 10 µm de diamètre) n’a pas révélé d’anomalies (Jones, Jones et Lyle, 1982). Dans l’état actuel des connaissances, on recommande par conséquent de ne pas dépasser une limite d’exposition fixée à 1 fibre/ml (f/ml) pour les fibres de carbone ou de graphite de taille respirable, et de maintenir le niveau des particules de composites en dessous des normes actuelles préconisées pour les poussières nocives.

Les fibres aramides (Kevlar) ont environ 12 µm de diamètre, et les fibrilles enrubannées à leur surface mesurent moins de 1 µm de largeur (voir figure 10.33). Ces fibrilles se séparent partiellement des fibres et se nouent avec d’autres fibrilles pour former des amas de taille non respirable. Les fibres Kevlar se caractérisent par une thermorésistance et une résistance à la traction élevées. Leurs utilisations sont multiples: elles peuvent servir d’agents de renforcement dans les plastiques, tissus et caoutchoucs et comme matériau de friction dans les garnitures de freins. La concentration moyenne pondérée de fibrilles admissible sur huit heures est comprise entre 0,01 et 0,4 f/ml (Merriman, 1989). Lors de l’utilisation de fibres Kevlar dans les matériaux de friction, de très faibles quantités de fibres se retrouvent dans les poussières. Les seuls effets pathologiques actuellement connus ont été mis en évidence dans des études sur l’animal. Ainsi, des tests d’inhalation effectués chez le rat pendant un à deux ans, avec des expositions de 25, 100 et 400 f/ml de fibrilles, ont révélé une bronchiolarisation alvéolaire qui était fonction de la dose administrée. Aux niveaux d’exposition élevés, on notait également la présence d’une fibrose minime et des lésions fibrotiques dans les canaux alvéolaires. La fibrose pourrait s’expliquer par la surcharge des mécanismes d’élimination pulmonaire. Un type de tumeur spécifique au rat — l’épithélioma kératinisant kystique — est apparu chez quelques-uns des animaux étudiés (Lee et coll., 1988). Les études d’inhalation à court terme toujours chez le rat ont montré que les fibrilles ne demeurent que peu de temps dans le tissu pulmonaire et sont rapidement éliminées (Warheit et coll., 1992). On ne dispose actuellement d’aucun résultat concernant les effets de l’exposition aux fibres aramides chez l’humain. En raison de la faible biopersistance et de la structure physique de ces fibres, il est toutefois probable que les risques pour la santé restent minimes si l’on n’excède pas une concentration de fibrilles de 0,5 f/ml, ce qui est actuellement le cas dans les applications commerciales.
Le carbure de silicium (carborundum) est un matériau très répandu, abrasif et réfractaire, fabriqué à partir de silice et de carbone à une température de 2 400 °C. Fibres et barbes (whiskers) de carbure de silicium — voir figure 10.34 (Harper et coll., 1995) — peuvent prendre naissance au cours de la fabrication de cristaux de carbure de silicium ou être produits directement sous forme de fibres polycristallines ou de whiskers monocristallins. Les fibres mesurent généralement moins de 1 à 2 µm de diamètre et ont une longueur comprise entre 3 et 30 µm. Les barbes ont un diamètre moyen de 0,5 µm et une longueur moyenne de 10 µm. L’incorporation de fibres et de barbes de carbure de silicium permet de renforcer des produits comme les stratifiés à matrice métallique, les produits céramiques ou leurs constituants. L’exposition aux fibres et aux barbes peut avoir lieu pendant la fabrication et parfois aussi au cours de l’usinage et de la finition des produits. Ainsi, la manipulation de matériaux recyclés peut conduire à des expositions à court terme de l’ordre de 5 f/ml. L’usinage des composites à matrice métallique ou céramique produit des concentrations moyennes pondérées sur huit heures qui sont respectivement de 0,031 f/ml et 0,76 f/ml (Scansetti, Piolatto et Botta, 1992; Bye, 1985).


Les données existantes provenant des études réalisées chez l’animal et chez l’humain indiquent un potentiel fibrogène établi et cancérogène possible. Les études réalisées in vitro sur des cultures de cellules de souris avec des barbes de carbure de silicium ont révélé une cytotoxicité égale ou supérieure à celle résultant de l’amiante crocidolite (Johnson et coll., 1992; Vaughan et coll., 1991). Chez le rat, une étude d’inhalation subaiguë a montré la présence d’une hyperplasie adénomateuse persistante des poumons (Lapin et coll., 1991). Les tests d’inhalation réalisés chez le mouton avec des poussières de carbure de silicium ont révélé que ces particules sont inertes. Toutefois, l’exposition aux fibres de carbure de silicium provoque une alvéolite fibrosante et une augmentation de la prolifération des fibroblastes (Bégin et coll., 1989). Les études faites sur des échantillons de tissu pulmonaire provenant de personnes travaillant dans la fabrication du carbure de silicium ont révélé la présence de nodules silicotiques et de corps ferrugineux et ont montré que les fibres de carbure de silicium ont une durabilité importante et peuvent se trouver en concentrations élevées dans le parenchyme pulmonaire. Les radiographies thoraciques font apparaître des lésions nodulaires et interstitielles irrégulières ainsi que des plaques pleurales.
Les fibres et les barbes de carbure de silicium ont une taille respirable, une durabilité importante et un potentiel fibrogène établi dans le tissu pulmonaire. Un fabricant de barbes de carbure de silicium a fixé à 0,2 f/ml la concentration moyenne admissible pondérée sur huit heures (Beaumont, 1991). Il s’agit là d’une recommandation prudente reposant sur les informations actuellement disponibles.
Les fibres artificielles vitreuses (FAV) sont généralement classées de la façon suivante:
Le processus de fabrication commence avec la fusion des matières premières suivie d’un refroidissement rapide qui provoque la production de fibres non cristallines (ou vitreuses). Certains processus de fabrication permettent des variations importantes de la taille des fibres, la limite inférieure étant voisine de 1 µm de diamètre (voir figure 10.35). Il est également possible d’ajouter des stabilisateurs (comme Al2O3, TiO2 et ZnO) et des modificateurs (tels que MgO, Li2O, BaO, CaO, Na2O et K2O) pour changer les propriétés chimiques et physiques, telles que la résistance à la traction, l’élasticité, la durabilité et la résistivité thermique.

La fibre de verre est fabriquée à partir de dioxyde de silicium et de stabilisateurs et modificateurs introduits en concentrations variables. Généralement, la laine de verre s’obtient par un processus rotatoire produisant des fibres discontinues de 3 à 15 µm de diamètre moyen, avec des variations de diamètre inférieures ou égales à 1 µm. Les fibres de laine de verre sont liées, le plus souvent à des résines phénol-formaldéhyde, puis soumises à un processus de polymérisation thermique. Il est également possible d’ajouter, selon le type de procédé, d’autres agents comme des lubrifiants ou des mouillants. La production de fils de verre continus provoque moins de variations du diamètre moyen des fibres que celle de la laine de verre ou des fibres de verre à usage spécifique. En effet, ces fils mesurent de 3 à 25 µm de diamètre, tandis que les fibres de verre à usage spécifique, produites par étirage à la flamme, mesurent moins de 3 µm.
La production de laine de laitier et de laine de roche fait appel à la fusion et à la formation de fibres à partir de scories provenant respectivement de minerais métalliques et de roches ignées. Le procédé de fabrication comprend un processus de centrifugation sur turbine qui produit des fibres discontinues de 3,5 à 7 µm de diamètre moyen, calibre correspondant à la gamme des fibres respirables. La laine minérale peut être fabriquée avec ou sans liant, selon les applications auxquelles on la destine.
La fibre céramique réfractaire est fabriquée par un processus de centrifugation sur turbine ou par un processus de fabrication de fibres sur jet de vapeur, à partir de matériaux en fusion: argile de kaolin, mélanges alumine/silice ou alumine/silice/zirconium. Le diamètre moyen des fibres est compris entre 1 et 5 µm. Lorsqu’elles sont chauffées à des températures supérieures à 1 000° C, les fibres de céramique réfractaire peuvent se transformer en cristobalite (silice cristalline).
La diversité des diamètres et des compositions chimiques des FAV explique qu’elles soient utilisées dans plus de 35 000 applications. La laine de verre est employée pour l’isolation acoustique et thermique des bâtiments, ainsi que dans les systèmes de conditionnement d’air et de climatisation. Les fils de verre continus servent à fabriquer des tissus et comme agents de renforcement des plastiques, en particulier dans l’industrie automobile. Les fibres de verre à usage spécifique ont des applications particulières, par exemple dans l’industrie aéronautique qui exige des propriétés d’isolation (thermique et acoustique) de très haute qualité. La laine de roche et la laine de laitier sans liant sont utilisées pour le flocage et pour l’isolation des toits. Liées à des résines phénoliques, elles servent à la fabrication de matériaux d’isolation, comme les garnitures calorifuges et les matelas d’isolation. La fibre céramique réfractaire constitue 1 à 2% de la production mondiale des FAV. Elle est employée dans certaines installations industrielles comme les hauts fourneaux. La laine de verre, les fils de verre continus et la laine minérale sont les FAV dont la production est la plus importante.
On pense que les FAV ont moins d’effets indésirables que les silicates fibreux naturels (comme l’amiante) en raison de leur état non cristallin et de leur propension à se briser en fibres plus courtes. D’après les données actuelles, la laine de verre est la FAV la plus utilisée et celle qui a le moins de risque d’effets nocifs; elle est suivie par la laine de roche et la laine de laitier, puis par la fibre de verre à usage spécifique et durabilité élevée et, enfin, par la fibre céramique réfractaire. Dans les deux derniers cas, les fibres mesurent généralement moins de 3 µm de diamètre et présentent dès lors un risque élevé pour l’appareil respiratoire. La fibre de verre à usage spécifique (à forte teneur en stabilisants) telles l’alumine et la fibre céramique réfractaire a elle aussi une forte tendance à demeurer dans les liquides physiologiques. En revanche, les fils de verre continus n’ont pas une taille respirable et ne représentent donc aucun risque pour les poumons.
Les données dont on dispose actuellement proviennent de tests d’inhalation réalisés chez l’animal et d’études de morbidité et de mortalité conduites parmi des travailleurs employés à la fabrication des FAV. D’après des études chez le rat, l’exposition à deux matériaux d’isolation à base de laine de verre dont les fibres mesuraient en moyenne 1 µm de diamètre et 20 µm de longueur provoque une réponse cellulaire pulmonaire discrète qui cède partiellement à l’arrêt de l’exposition. Des résultats comparables ont été trouvés dans une autre étude d’inhalation réalisée chez l’animal avec un type particulier de laine de laitier. L’exposition par inhalation à la laine de roche provoque une fibrose minime chez l’animal, alors que les fibres céramiques réfractaires provoquent des cancers pulmonaires, des mésothéliomes, des fibroses pleurales et pulmonaires chez le rat ainsi que des mésothéliomes et des fibroses pleurales et pulmonaires chez le hamster à la concentration maximale admissible de 250 f/ml. A 75 f/ml et 120 f/ml, un mésothéliome et une fibrose minimale ont été mis en évidence chez le rat, tandis qu’à 25 f/ml on enregistrait une réponse cellulaire au niveau des poumons (Bunn et coll., 1993).
Une irritation de la peau, des yeux et des voies respiratoires supérieures et inférieures peut se produire; elle dépend des niveaux d’exposition et des activités exercées. L’irritation de la peau est l’un des effets les plus courants et nécessite un reclassement rapide chez 5% des travailleurs. Cette irritation est due au traumatisme mécanique de la peau engendré lorsque les fibres mesurent plus de 4 à 5 µm de diamètre. Elle peut être évitée grâce à des mesures de contrôle appropriées, permettant en particulier d’éviter que la peau ne soit en contact direct avec les fibres, et, cela, grâce au port de vêtements amples et à manches longues et au lavage séparé des vêtements de travail. Des symptômes des voies respiratoires supérieures et inférieures peuvent apparaître si l’environnement est particulièrement empoussiéré, c’est-à-dire lors de la fabrication des produits à base de FAV et de leur utilisation, ainsi que dans les bâtiments résidentiels lorsque ces produits ne sont pas manipulés, mis en place ou enlevés correctement.
Lorsqu’on étudie la morbidité respiratoire dans des usines de fabrication, on ne trouve généralement pas d’effets indésirables si l’on se réfère à la symptomatologie, aux radiographies pulmonaires et aux épreuves fonctionnelles respiratoires. Toutefois, une étude entreprise chez les travailleurs d’une usine de fabrication de fibres céramiques réfractaires a révélé une augmentation de la prévalence des plaques pleurales (Lemasters et coll., 1994). En règle générale, les études effectuées parmi les travailleurs des secteurs de production secondaire et les utilisateurs de FAV sont limitées et difficiles à interpréter en raison des possibilités d’exposition antérieure à l’amiante.
Des études de mortalité réalisées dans des usines de fabrication de fibres de verre et de laine minérale sont en cours en Europe et aux Etats-Unis. Les résultats de l’étude européenne ont déjà révélé une augmentation globale de la mortalité due au cancer du poumon par rapport aux taux de mortalité nationaux (mais non locaux). Dans les cohortes de travailleurs de l’industrie de la fibre de verre et de la laine minérale, la tendance au cancer du poumon augmente en fonction du temps écoulé depuis l’embauche initiale, mais non en fonction de la durée du travail effectué. Si l’on se réfère aux taux de mortalité locaux, on observe une augmentation de la mortalité liée au cancer du poumon dans la phase précoce de la production de laine minérale (Simonato, Fletcher et Cherrie, 1987; Boffetta et coll., 1992). L’étude menée aux Etats-Unis montre une augmentation statistiquement significative du risque de cancer respiratoire, sans qu’il soit possible de la corréler avec divers indices d’exposition (Marsh et coll., 1990). Ces résultats corroborent ceux d’autres études cas-témoins réalisées dans des usines de fabrication de laine de laitier et de fibres de verre qui ont révélé une augmentation des risques de cancer du poumon corrélés avec le tabagisme, mais non avec l’importance de l’exposition aux FAV (Wong, Foliart et Trent, 1991; Chiazze, Watkins et Fryar, 1992). En revanche, le risque de mortalité n’est pas augmenté dans le secteur des fils de verre continus (Shannon et coll., 1990). Une autre étude en cours concerne la production de fibres de céramique réfractaire aux Etats-Unis. Enfin, on peut noter que les études de mortalité concernant les travailleurs engagés dans la fabrication des produits et les applications des FAV sont très peu nombreuses.
En 1987, le Centre international de recherche sur le cancer (CIRC) a classé la laine de verre, la laine de roche, la laine de laitier et les fibres céramiques dans le groupe des cancérogènes humains possibles (groupe 2B). Les études effectuées à l’heure actuelle chez l’animal et les études de morbidité et de mortalité menées chez les travailleurs employés à la fabrication des FAV et dans leurs utilisations vont permettre de mieux définir les risques potentiels pour la santé humaine. D’après les données dont on dispose, le risque lié à l’exposition aux FAV est sensiblement plus faible qu’avec l’amiante, qu’il s’agisse de morbidité ou de mortalité. La majorité des études réalisées chez l’humain concerne toutefois les usines de fabrication des FAV, où les niveaux d’exposition ne dépassent généralement pas 0,5-1 f/ml pour une journée de travail de huit heures. Dans le domaine de la production secondaire et des applications des FVA, vu que l’on dispose de peu de données de morbidité et de mortalité, on préconise de maintenir l’exposition aux fibres respirables à des niveaux inférieurs ou égaux à ces valeurs, et, cela, grâce à l’adoption de mesures de prévention technique, au respect des bonnes pratiques de travail, à la formation des travailleurs et à des programmes de protection respiratoire individuelle. Cela vaut tout particulièrement pour les fibres céramiques réfractaires à longévité élevée, de même que pour les fibres de verre à usage spécifique et toutes les autres fibres artificielles respirables dont la biopersistance est longue dans les milieux biologiques et qui peuvent, par conséquent, former des dépôts durables dans le parenchyme pulmonaire.
Le cancer du poumon est le cancer le plus répandu au monde. En 1985, on estimait qu’il existait 676 500 cas de cancer du poumon chez l’homme et 219 300 cas chez la femme, représentant 11,8% de tous les cancers d’apparition récente et ce chiffre augmente à un taux d’environ 0,5% par an (Parkin, Pisani et Ferlay, 1993). Environ 60% de ces cas sont recensés dans les pays industriels, où généralement le cancer du poumon est la première cause de décès chez l’homme. Dans les pays industriels et en développement, l’incidence est toujours plus élevée chez l’homme que chez la femme, avec un rapport compris entre 2 et 10. Ces différences et leurs variations sont dues au tabagisme, dont l’importance varie d’un pays à l’autre.
Le risque de cancer du poumon est plus important dans les zones urbaines que dans les régions rurales. Dans les pays industriels, il existe une relation inverse évidente chez l’homme entre la fréquence du cancer du poumon et la mortalité par classe sociale; ce tableau semble être moins clair chez la femme. Chez l’homme, les différences constatées sont imputables au profil tabagique. Toutefois, dans les pays en développement, les risques semblent plus élevés chez les hommes des classes socioprofessionnelles supérieures, probablement en raison de l’adoption plus précoce des habitudes occidentales par les groupes plus favorisés de la population.
Les données du programme SEER de l’Institut national du cancer (National Cancer Institute) aux Etats-Unis pour la période 1980-1986 indiquent que, comme pour les années précédentes, l’incidence est plus élevée chez les hommes de race noire que chez les hommes de race blanche, différence raciale qui n’est pas observée chez les femmes. Ces disparités selon les groupes ethniques aux Etats-Unis semblent pouvoir être attribuées aux différences socio-économiques entre Noirs et Blancs (Baquet et coll., 1991).
L’incidence du cancer du poumon augmente avec l’âge de façon presque linéaire selon une échelle bilogarithmique; seuls les groupes les plus âgés peuvent présenter une courbe descendante. L’incidence du cancer du poumon et la mortalité qu’il entraîne ont augmenté rapidement au cours de ce siècle et continuent à progresser dans la plupart des pays.
Il existe quatre types histologiques principaux de cancer du poumon: le carcinome épidermoïde, l’adénocarcinome, le cancer anaplasique à grandes cellules et le cancer à petites cellules; les trois premiers sont également appelés cancers pulmonaires autres qu’à petites cellules. Les proportions de chaque type histologique varient selon le sexe et l’âge.
Le carcinome épidermoïde bronchique est très fortement associé au tabagisme et représente le type le plus courant de cancer du poumon dans de nombreuses populations. Il apparaît le plus souvent dans les bronches proximales.
L’adénocarcinome est moins fortement corrélé au tabagisme. Cette tumeur est périphérique à l’origine et peut se manifester sous forme d’un nodule périphérique solitaire, d’une maladie multifocale ou d’une pneumonie rapidement évolutive se propageant de lobe en lobe.
Le cancer à grandes cellules représente une plus faible proportion des cancers du poumon et se comporte de la même façon que l’adénocarcinome.
Le cancer à petites cellules ne représente que 10 à 15% de tous les cancers pulmonaires. Il apparaît généralement en situation endobronchique centrale et a tendance à métastaser rapidement.
Les signes et les symptômes du cancer du poumon dépendent de la localisation de la tumeur, de son extension et de ses métastases. De nombreux patients consultent pour une lésion asymptomatique découverte de façon fortuite à la radiographie. Parmi les patients souffrant d’un cancer autre qu’à petites cellules, il est fréquent d’observer de la fatigue, une diminution de l’activité, une toux persistante, une dyspnée, une diminution de l’appétit et une perte de poids. Aux stades avancés, des sifflements ou un stridor peuvent apparaître. La poursuite de l’évolution peut provoquer une atélectasie, une pneumonie et la formation d’un abcès. Chez les patients atteints d’un cancer à petites cellules, les signes cliniques sont moins prononcés et sont généralement liés à la localisation endobronchique de la tumeur.
Le cancer du poumon peut métastaser dans théoriquement n’importe quel organe. Cependant, les sites privilégiés des métastases sont la plèvre, les ganglions lymphatiques, l’os, le cerveau, les glandes surrénales, le péricarde et le foie. Au moment où le diagnostic est posé, la majorité des patients présentant un cancer du poumon ont déjà des métastases.
Le pronostic varie selon le stade de la maladie. La survie globale à cinq ans pour le cancer du poumon en Europe (en 1983-1985) était comprise entre 7 et 9% (Berrino et coll., 1995).
Il n’existe actuellement aucune méthode de dépistage systématique du cancer du poumon dans l’ensemble de la population.
Le cancer nasopharyngé est rare dans la plupart des populations, mais fréquent chez l’homme et la femme dans certaines régions géographiques comme l’Asie du Sud-Est, la Chine du Sud et l’Afrique du Nord. Ce risque reste élevé chez les personnes émigrant de Chine australe, mais diminue de plus de moitié dans les deuxième et troisième générations d’émigrants installés aux Etats-Unis.
Les cancers du nasopharynx sont généralement d’origine épithéliale malphigienne. L’OMS classe ces tumeurs de la façon suivante: type 1, épithélioma épidermoïde kératinisant; type 2, cancer non kératinisant; type 3, cancer indifférencié (qui est le type histologique le plus fréquent). Le type 1 présente une prolifération locale non contrôlée et des métastases chez 60% environ des patients. Les types 2 et 3 métastasent chez 80 à 90% des patients.
La présence d’une masse au niveau du cou est notée chez environ 90% des sujets présentant un cancer nasopharyngé. On observe également parfois des troubles de l’audition, une otite moyenne séreuse, des acouphènes, une obstruction nasale, des douleurs et des symptômes en rapport avec la prolifération de la tumeur dans les structures anatomiques adjacentes.
En Europe, entre 1983 et 1985, la survie globale à cinq ans pour le cancer nasopharyngé était d’environ 35% et variait selon le stade de la tumeur et sa localisation (Berrino et coll., 1995).
La consommation de poissons salés à la chinoise constitue un facteur de risque de cancer nasopharyngé; le rôle des autres facteurs nutritionnels et des virus, en particulier le virus d’Epstein-Barr, bien que suspecté, n’a pas été confirmé. Aucun facteur professionnel n’est connu actuellement. Il n’existe aucune mesure préventive (Higginson, Muir et Muñoz, 1992).
Les cancers du nez et des cavités nasales sont relativement rares. Ils représentent ensemble — si l’on inclut les sinus maxillaires, éthmoïdiens, sphénoïdiens et frontaux — moins de 1% de tous les cancers. Dans la plupart des cas, ces tumeurs sont classées comme des cancers épidermoïdes. Dans les pays occidentaux, les cancers du nez sont plus fréquents que les cancers des sinus (Higginson, Muir et Muñoz, 1992).
Ces cancers apparaissent plus fréquemment chez l’homme et dans les populations de race noire. La fréquence la plus élevée est observée en Inde, au Koweït et en Martinique. Le pic de développement de la maladie apparaît vers la soixantaine. La cause principale connue est l’exposition à la poussière de bois, en particulier les bois durs. Ce type de cancer ne semble pas corrélé au tabagisme.
La plupart des tumeurs des fosses nasales et des sinus de la face sont bien différenciées et ont une croissance lente. Elles peuvent se manifester par une ulcération qui ne cicatrise pas, des saignements, une obstruction nasale et des symptômes en rapport avec la prolifération dans la cavité buccale, l’orbite et la fosse ptérygoïdienne. La maladie est généralement à un stade avancé au moment du diagnostic.
En Europe, entre 1983 et 1985, la survie globale à cinq ans pour le cancer du nez et des sinus de la face était d’environ 35% et variait selon la taille de la lésion au moment du diagnostic (Berrino et coll., 1995).
L’incidence la plus élevée de cancers laryngés a été relevée en Navarre (Espagne), à São Paulo (Brésil) et à Varèse (Italie). Une mortalité importante est également décrite en Afrique du Nord, au Moyen-Orient, à Cuba, en France, en Hongrie, en Uruguay et en Yougoslavie. Le cancer laryngé prédomine chez l’homme: on estime que 120 500 cas sont apparus chez l’homme en 1985, contre 20 700 chez la femme (Parkin, Pisani et Ferlay, 1993). De façon générale, son incidence est plus élevée dans les populations noires que dans les populations blanches et plus importante dans les zones urbaines que dans les zones rurales.
Presque tous les cancers du larynx sont des épithéliomas épidermoïdes. Ils sont situés pour la plupart au niveau de la glotte, mais peuvent également se développer dans la région subglottique, ou plus rarement, sous-glottique.
Ce cancer est peu ou pas symptomatique. Une douleur, une sensation d’irritation locale, une modification de la tolérance aux aliments chauds ou froids, une tendance à faire des fausses routes, une altération des voies aériennes et une légère modification de la voix pendant plusieurs semaines, ainsi qu’une adénopathie cervicale peuvent être présentes selon la localisation et le stade de la lésion.
La plupart des cancers laryngés sont visibles par une inspection laryngée ou une endoscopie. Les lésions prénéoplasiques peuvent être identifiées dans le larynx des fumeurs (Higginson, Muir et Muñoz, 1992).
En Europe, entre 1983 et 1985, la survie globale à cinq ans pour le cancer laryngé était d’environ 55% (Berrino et coll., 1995).
Les mésothéliomes peuvent apparaître au niveau de la plèvre, du péritoine et du péricarde. Le mésothéliome malin représente la tumeur pleurale la plus importante: il apparaît principalement entre 50 et 70 ans.
Le mésothéliome pleural était autrefois une tumeur rare. Il le reste chez la plupart des femmes tandis que chez l’homme, il a augmenté de 5 à 10% par an dans les pays industriels au cours des dernières années. De façon générale, les hommes sont atteints cinq fois plus que les femmes. Des estimations précises concernant l’incidence et la mortalité sont difficiles à établir en raison des difficultés de diagnostic histologique et des modifications apportées à la Classification internationale des maladies (CIM) (Higginson, Muir et Muñoz, 1992). Toutefois, l’incidence semble présenter des variations locales très importantes et peut être très élevée dans les régions où il existe des mines d’amiante (comme la région nord-ouest de la province du Cap en Afrique du Sud), des chantiers navals et dans celles où l’on note une contamination environnementale importante par les fibres, comme dans le centre de la Turquie.
Les patients peuvent être soit asymptomatiques — et leur maladie sera alors diagnostiquée de façon fortuite sur la radiographie thoracique — , soit présenter une dyspnée et des douleurs thoraciques.
Les mésothéliomes ont tendance à être invasifs. La survie médiane est de quatre à dix-huit mois dans diverses séries.
A part la fumée de tabac, quatorze agents ou mélanges complexes et dix activités industrielles (voir tableau 10.24) sont incriminés dans la genèse des cancers respiratoires, selon le Centre international de recherche sur le cancer (CIRC). En outre, six agents ou mélanges complexes et deux activités industrielles sont probablement cancérogènes pour un organe au moins de l’appareil respiratoire (voir tableau 10.25). Tous ces produits — sauf l’azathioprine, médicament immunosuppresseur — représentent des expositions professionnelles (CIRC, 1971-1994).
|
Agents |
Organes cibles |
|
Substances |
|
|
Amiante |
Poumon, larynx, plèvre |
|
Mélanges complexes |
|
|
Goudrons de houille |
Poumon |
|
Activités industrielles |
|
|
Production d�aluminium |
Poumon |
Source: CIRC, 1971-1994.
|
Agents |
Organes cibles suspectés |
|
Substances |
|
|
Acrylonitrile |
Poumon |
|
Mélanges complexes |
|
|
Gaz d�échappement des moteurs diesel |
Poumon |
|
Activités industrielles |
|
|
Industrie du caoutchouc |
Poumon |
Source: CIRC, 1971-1994.
Les catégories professionnelles présentant un risque accru de cancer du poumon par exposition à des produits arsenicaux sont les ouvriers des fonderies de métaux non ferreux, les travailleurs de la fourrure, les fabricants de produits antiparasitaires et les travailleurs viticoles (CIRC, 1987).
De nombreuses études épidémiologiques ont été réalisées sur l’association entre les composés du chrome (hexavalent) et l’apparition d’un cancer du poumon ou d’un cancer du nez ou des fosses nasales dans les opérations mettant en œuvre des chromates ou des pigments chromiques et dans les ateliers de chromage (CIRC, 1990). Les résultats de ces études ont démontré le potentiel cancérogène du chrome hexavalent et de ses composés.
Dans de nombreux pays, les personnes travaillant dans les raffineries de nickel présentent un risque plus élevé de cancer du poumon et de cancer nasal. Les autres catégories professionnelles exposées au nickel, et chez lesquelles un risque accru de cancer du poumon a été mis en évidence, sont les mineurs de sulfure de nickel et les travailleurs employés à la fabrication d’alliages à haute teneur en nickel (CIRC, 1990).
Les travailleurs exposés au béryllium encourent eux aussi un risque accru de cancer du poumon (CIRC, 1994). Les données les plus intéressantes proviennent du registre des cas de bérylliose établi aux Etats-Unis, dans lequel toutes les observations de pathologies pulmonaires en rapport avec le béryllium recueillies dans différents secteurs industriels ont été consignées.
Une augmentation des cas de cancer du poumon a été constatée dans des cohortes de travailleurs des fonderies de cadmium et de la fabrication de piles nickel-cadmium (CIRC, 1994); elle ne peut être expliquée par l’exposition simultanée aux produits arsenicaux chez les premiers ou au nickel chez les seconds.
L’amiante constitue un cancérogène professionnel majeur. Les principaux cancers dus à l’amiante sont le cancer du poumon et le mésothéliome, mais d’autres sites peuvent être touchés, comme l’appareil digestif, le larynx et les reins. Toutes les formes d’amiante ont été incriminées dans la pathogenèse du cancer du poumon et du mésothéliome. En outre, les fibres asbestiformes contenant du talc se sont révélées cancérogènes pour le poumon humain (CIRC, 1987). Une caractéristique spécifique au cancer du poumon dû à l’amiante est sa relation synergique avec le tabagisme.
De nombreuses études réalisées chez les mineurs ou les travailleurs des carrières, des fonderies, de la céramique et du granit et chez les tailleurs de pierre ont montré que le risque de cancer du poumon est plus élevé chez les sujets présentant une silicose due à l’exposition à des poussières de silice cristalline (CIRC, 1987).
Les hydrocarbures aromatiques polycycliques (HAP) résultent principalement de processus pyrolitiques, notamment de la combustion incomplète de matières organiques. L’être humain est exposé exclusivement à des mélanges d’HAP tels que les suies, les goudrons et les brais de houille. Des études de mortalité réalisées sur des cohortes de ramoneurs ont montré une augmentation du risque de cancer pulmonaire attribuée à l’exposition à la suie. Plusieurs études épidémiologiques ont mis en évidence une hausse du nombre des cancers respiratoires chez les travailleurs exposés aux fumées de brai lors de la production de l’aluminium ou du carbure de calcium et dans les travaux de couverture. Ces activités comportent également des risques d’exposition aux goudrons, notamment au goudron de houille. D’autres industries pour lesquelles l’augmentation des cancers respiratoires est due à l’exposition aux fumées de goudron de houille sont la gazéification de la houille et la production de coke (CIRC, 1987). On a essayé d’analyser les effets de l’exposition aux gaz d’échappement des moteurs diesel séparément des autres produits de combustion; certaines études, mais non toutes, ont relevé un risque accru de cancer respiratoire, surtout pulmonaire. Les catégories professionnelles étudiées comprenaient les cheminots, les dockers, les personnes employées dans les garages d’autobus, les employés des compagnies d’autobus et les chauffeurs professionnels (CIRC, 1989a). Parmi les autres mélanges d’HAP dont le potentiel cancérogène a été étudié chez l’humain, on peut citer le noir de carbone, les gaz d’échappement des moteurs à essence, les huiles minérales, les huiles de schiste et les bitumes. Les huiles de schiste et les huiles minérales faiblement ou non traitées sont cancérogènes pour l’humain, tandis que les gaz d’échappement des moteurs à essence peuvent être cancérogènes sans que cela soit certain. En ce qui concerne les huiles minérales très raffinées, les bitumes et le noir de carbone, on ne saurait les classer par rapport à leur pouvoir cancérogène pour l’humain (CIRC, 1987, 1989a). Bien que ces mélanges contiennent des HAP, aucun effet cancérogène n’a été mis en évidence sur le poumon, quel que soit le produit considéré; les preuves de la cancérogénicité des huiles minérales faiblement ou non traitées et des huiles de schiste reposent sur le risque accru de cancers autres que respiratoires (principalement de la peau et du scrotum) chez les travailleurs exposés.
Le sulfure de bis(2-chloroéthyle), connu sous le nom d’ypérite ou de gaz moutarde, a été largement utilisé au cours de la première guerre mondiale. Les études portant sur les soldats exposés à ce gaz et les travailleurs employés à sa fabrication ont révélé des cas de cancer du poumon et de cancer nasal (CIRC, 1987).
De nombreuses études épidémiologiques ont démontré que les travailleurs exposés au chlorométhylméthyléther ou au bis(chlorométhyl)éther ont un risque plus élevé de cancer pulmonaire, surtout à petites cellules (CIRC, 1987).
Selon certaines études réalisées dans la fabrication des fibres textiles synthétiques, la polymérisation de l’acrylonitrile et l’industrie du caoutchouc (CIRC 1987), l’acrylonitrile est associée à un risque accru de cancer du poumon.
Le risque de cancer est également supérieur à la normale chez les travailleurs exposés au formaldéhyde dans les industries de la chimie et du bois et dans la production et les applications de ce composé (CIRC, 1987). Il s’agit essentiellement du cancer nasal et nasopharyngé: plusieurs études relèvent un gradient dose-réponse, bien que le nombre des cas exposés soit souvent faible. Les autres cancers cités sont les cancers du poumon et du cerveau et les leucémies.
Plusieurs études ont mis en évidence une augmentation du risque de cancer laryngé chez les travailleurs exposés aux brouillards et fumées d’acide sulfurique et d’autres acides inorganiques forts, utilisés, par exemple, dans le décapage de l’acier, la fabrication du savon et l’industrie pétrochimique (CIRC, 1992). Un risque accru de cancer du poumon est également relevé dans certaines de ces études. On a également trouvé davantage de cancers du nez et des sinus dans une cohorte de travailleurs d’une manufacture d’isopropanol utilisant le procédé à l’acide fort.
Les travailleurs du bois présentent eux aussi un risque plus élevé de cancer nasal, en particulier d’adénocarcinome (CIRC, 1987). Le risque est confirmé chez les travailleurs de l’industrie du meuble et les ébénistes. Les études réalisées chez les charpentiers et les menuisiers suggèrent également une augmentation de ce risque, mais certains travaux ont donné des résultats négatifs. Pour d’autres industries du bois, comme les scieries et les usines à papier, le risque cancérogène n’est pas classifiable. Même si la cancérogénicité des poussières de bois n’a pas été évaluée par le CIRC, il est vraisemblable que ces poussières sont responsables, au moins en partie, du risque accru d’adénocarcinome nasal chez les travailleurs du bois. En revanche, il ne semble pas y avoir une augmentation du risque d’atteinte cancéreuse d’autres organes respiratoires.
L’adénocarcinome nasal a également été mis en évidence dans la fabrication et la réparation des chaussures (CIRC, 1987). Aucune donnée n’a permis de démontrer que le risque de cancer respiratoire était plus important chez les travailleurs employés au tannage, au traitement du cuir et à la fabrication d’articles en cuir. A l’heure actuelle, on ignore encore si le risque accru d’adénocarcinome nasal dans l’industrie de la chaussure est dû aux poussières de cuir ou à d’autres agents. La cancérogénicité des poussières de cuir n’a pas été évaluée par le CIRC.
Le cancer du poumon est assez répandu chez les mineurs d’uranium et les travailleurs employés à l’extraction souterraine d’hématite et dans plusieurs autres catégories de mineurs du métal (CIRC, 1988; Committee on the Biological Effects of Ionizing Radiation, BEIR IV, 1988). Un facteur commun à ces catégories professionnelles est l’exposition aux rayonnements alpha émis par les particules de radon inhalées. La principale source de données concernant l’apparition d’un cancer après une exposition à des rayonnements ionisants provient du suivi réalisé chez les survivants de la bombe atomique (Preston et coll., 1986; Shimizu et coll., 1987). Le risque de cancer du poumon est plus élevé chez ces personnes, ainsi que chez celles ayant bénéficié d’une radiothérapie (Smith et Doll, 1982). Toutefois, aucune donnée ne permet actuellement d’établir que le risque de cancer du poumon est plus important chez les travailleurs exposés à de faibles niveaux de rayonnements ionisants, comme c’est le cas dans l’industrie nucléaire (Béral et coll., 1987; Committee on the Biological Effects of Ionizing Radiation, BEIR V, 1990). La cancérogénicité des rayonnements ionisants n’a pas été évaluée par le CIRC.
Un risque accru de cancer pulmonaire a été observé chez les peintres dans trois études de cohortes importantes et dans huit études de petites cohortes, ainsi que dans onze études cas-témoins dans plusieurs pays. En revanche, il ne semble pas que le risque soit supérieur parmi les travailleurs employés à la fabrication de peintures (CIRC, 1989c).
D’autres substances chimiques, professions et industries présentant des risques de cancérogénicité pour l’humain d’après le CIRC (groupe 1) n’ont pas le poumon comme organe cible primaire. Néanmoins, la possibilité d’un risque accru de cancer du poumon a été soulevée pour certaines de ces substances, comme le chlorure de vinyle (CIRC, 1987) et dans certaines activités comme la pulvérisation d’insecticides (CIRC, 1991b), mais les données recueillies ne sont pas concluantes.
En outre, plusieurs agents ayant le poumon comme cible principale ont été considérés comme pouvant être cancérogènes pour l’humain (CIRC, groupe 2B) sur la base de leur activité cancérogène en expérimentation animale ou de données épidémiologiques limitées. Ces agents incluent les composés inorganiques du plomb (CIRC, 1987), le cobalt (CIRC, 1991a), les fibres vitreuses artificielles (laine de roche, laine de laitier et laine de verre) (CIRC, 1988), ainsi que les fumées de soudage (CIRC, 1990).
Bien que les études épidémiologiques concernant les pneumonies d’origine professionnelle (POP) soient limitées, on pense que ces affections diminuent dans le monde. En revanche, dans les pays développés, les POP ont tendance à augmenter dans les professions de santé et la recherche biomédicale. Les germes responsables des POP contractées à l’hôpital sont souvent les mêmes que ceux qui prédominent à l’extérieur, mais la réémergence de la tuberculose, de la rougeole et de la coqueluche dans les établissements de soins représente un risque supplémentaire pour les professionnels de la santé. Dans les pays en développement et dans certaines professions spécifiques des pays industriels, de nombreux cas de POP sont dus à des agents pathogènes infectieux très particuliers qui ne circulent habituellement pas dans la population.
Il est difficile d’attribuer l’infection à une cause professionnelle plutôt qu’à l’environnement général, notamment chez le personnel hospitalier. Jusqu’à présent, le risque professionnel était établi avec certitude seulement dans les cas d’infection par des agents présents dans le milieu du travail mais absents dans la collectivité. Désormais, l’utilisation de techniques moléculaires pour retrouver les clones microbiens spécifiques dans les milieux professionnels et les collectivités faciliteront l’établissement des risques.
Comme les pneumonies communautaires, les POP proviennent de micro-aspirations de bactéries qui colonisent l’oropharynx, d’inhalation de particules infectieuses respirables ou d’ensemencement hématogène des poumons. La plupart des pneumonies communautaires proviennent de micro-aspirations, tandis que les POP sont généralement dues à l’inhalation de particules infectieuses de 0,5 à 10 µm en suspension dans l’air dans le milieu de travail. Les particules plus grosses n’arrivent pas à atteindre les alvéoles en raison de leur enclavement à la suite d’un impact ou de leur sédimentation sur les parois des grosses voies aériennes et de leur élimination ultérieure. Quant aux particules plus petites, elles restent suspendues au cours des mouvements inspiratoires et expiratoires et se déposent rarement dans les alvéoles. Dans certaines maladies comme la fièvre hémorragique avec syndrome rénal, due à un hantavirus, le mode principal de transmission est l’inhalation, mais le foyer primaire de la maladie n’est pas toujours le poumon. Les agents pathogènes professionnels qui ne sont pas transmis par inhalation peuvent secondairement intéresser les poumons, mais ne feront pas l’objet d’une discussion ici.
Le présent article examine brièvement quelques agents pathogènes professionnels particulièrement importants. Une liste plus exhaustive des pathologies pulmonaires d’origine professionnelle, classées par étiologie spécifique, est présentée dans le tableau 10.26.
|
Maladie/agent pathogène |
Réservoir |
Populations à risque |
|
Bactéries, chlamydiae, mycoplasmes et rickettsies |
||
|
Brucellose (Brucella spp.) |
Bétail (bovins, caprins, porcs) |
Personnel vétérinaire, ouvriers agricoles, personnel de laboratoire, personnel des abattoirs |
|
Infection charbonneuse (Bacillus anthracis) |
Produits animaux (laines, peaux) |
Ouvriers agricoles, tanneurs, personnel des abattoirs, ouvriers du textile, personnel de laboratoire |
|
Peste pneumonique (Yersinia pestis) |
Rongeurs sauvages |
Personnel vétérinaire, chasseurs, trappeurs, personnel de laboratoire |
|
Coqueluche (Bordetella pertussis) |
Humains |
Personnel des foyers pour personnes âgées, personnel de santé |
|
Maladie des légionnaires (Legionella spp.) |
Sources d�eau contaminée (tours de refroidissement, condenseurs à évaporation forcée, par exemple) |
Personnel de santé, personnel de laboratoire, excavateurs de puits d�eau |
|
Mélioïdose (Pseudomonas pseudomallei) |
Sol, eau stagnante, rizières |
Personnel militaire, ouvriers agricoles |
|
Streptococcus pneumoniae |
Humains |
Personnel de santé, ouvriers agricoles, mineurs de gisements souterrains |
|
Neisseria meningitidis |
Humains |
Personnel de santé, personnel de laboratoire, personnel militaire |
|
Pasteurellose (Pasteurella multocida) |
Divers animaux domestiques (chats, chiens) ou sauvages |
Ouvriers agricoles, personnel vétérinaire |
|
Tularémie respiratoire (Francisella tularensis) |
Rongeurs sauvages et lapins |
Travailleurs manuels, personnel militaire, personnel de laboratoire, chasseurs, trappeurs, ouvriers agricoles |
|
Ornithose (Chlamydia psittaci) |
Oiseaux |
Personnel des commerces d�oiseaux, des usines de préparation de la volaille, des cliniques vétérinaires, des laboratoires |
|
Pneumonie à Chlamydia pneumoniae |
Humains |
Personnel de santé, personnel militaire |
|
Fièvre Q (Coxiella burnetii) |
Animaux domestiques (bovins, ovins, caprins) |
Personnel de laboratoire, ouvriers du textile, personnel des abattoirs, ouvriers |
|
Pneumonie atypique (mycoplasma pneumoniae) |
Humains |
Personnel militaire, personnel de santé, employés de collectivités |
|
Champignons/mycobactéries |
||
|
Histoplasmose (Histoplasma capsulatum) |
Sol, excréments d�oiseaux et de chauves-souris (endémique dans l�est de l�Amérique du Nord) |
Ouvriers agricoles, personnel de laboratoire, travailleurs manuels |
|
Coccidioïdomycose (Coccidioides immitis) |
Sol (endémique dans l�ouest de l�Amérique du Nord) |
Personnel militaire, ouvriers agricoles, travailleurs manuels, ouvriers du textile, personnel de laboratoire |
|
Blastomycose (Blastomyces dermatitidis) |
Sol (endémique dans l�est de l�Amérique du Nord) |
Personnel de laboratoire, ouvriers agricoles et forestiers, travailleurs manuels |
|
Paracoccidioïdomycose (Paracoccidioides brasiliensis) |
Sol (endémique au Venezuela, en Colombie, au Brésil) |
Ouvriers agricoles |
|
Sporotrichose (Sporothrix schenkii) |
Débris végétaux, écorces d�arbres et de plantes d�agrément |
Jardiniers, fleuristes, mineurs |
|
Tuberculose (Mycobacterium tuberculosis, M. bovis, M. africanum) |
Humains et autres primates, bovins |
Mineurs au rocher, travailleurs de fonderie, personnel de santé et de laboratoire, personnel des abattoirs, personnel vétérinaire, personnel militaire, personnes travaillant dans les tavernes |
|
Mycobactériose autre que la tuberculose (Mycobacterium spp.) |
Sol |
Travailleurs exposés à la silice, y compris les personnes chargées du décapage au jet de sable |
|
Virus |
||
|
Hantavirus |
Rongeurs |
Travailleurs agricoles, gardiens de troupeaux, personnel de dératisation |
|
Rougeole |
Humains |
Personnel de santé et de laboratoire |
|
Rubéole |
Humains |
Personnel de santé et de laboratoire |
|
Grippe |
Humains |
Personnel de santé et de laboratoire |
|
Varicelle |
Humains |
Personnel de santé et de laboratoire |
|
Virus syncytial respiratoire |
Humains |
Personnel de santé et de laboratoire |
|
Adénovirus |
Humains |
Personnel de santé et de laboratoire |
|
Virus parainfluenza |
Humains |
Personnel de santé et de laboratoire |
|
Virus de la chorioméningite lymphocytaire(arénavirus) |
Rongeurs |
Personnel de laboratoire, personnel vétérinaire |
|
Fièvre de Lassa (arénavirus) |
Rongeurs |
Personnel de santé |
|
Virus Marburg et Ebola (filovirus) |
Humains et autres primates, éventuellement chauves-souris |
Personnel de laboratoire, personnel vétérinaire, personnel de santé, travailleurs de l�industrie cotonnière |
Outre les gaz et les poussières organiques susceptibles d’irriter l’appareil respiratoire et de générer une symptomatologie pseudo-infectieuse, plusieurs agents responsables de zoonoses (pathogènes communs à l’humain et à l’animal) et autres agents infectieux associés aux travaux agricoles affectent spécifiquement cette catégorie de travailleurs. Les maladies considérées sont acquises par inhalation d’aérosols infectieux véhiculés par l’air et se transmettent rarement d’une personne à l’autre: il s’agit de l’infection charbonneuse, de la brucellose, de la fièvre Q, de l’ornithose, de la tuberculose et de la peste (voir tableau 10.26). Les agents pathogènes fongiques incluent l’histoplasmose, la blastomycose, la coccidioïdomycose, la paracoccidioïdomycose et la cryptococcose (voir tableau 10.26). En dehors des maladies à hantavirus, les maladies virales ne constituent pas une cause importante de maladies pulmonaires professionnelles chez les travailleurs agricoles.
Certaines des infections en question semblent plus répandues dans l’agriculture, mais leur fréquence est difficile à déterminer pour les raisons suivantes: 1) la plupart des cas sont infracliniques; 2) les manifestations cliniques sont bénignes ou difficiles à diagnostiquer en raison de symptômes non spécifiques; 3) la plupart des travailleurs agricoles n’ont pas accès aux services de médecine et de diagnostic; 4) il n’existe aucun système organisé de recensement de ces affections; 5) ces maladies sont souvent rares dans la collectivité et ne sont pas reconnues par le personnel médical. C’est ainsi que, bien que la néphrite épidémique due au virus Puumala (un hantavirus) soit rarement rapportée en Europe occidentale, des enquêtes sérologiques conduites chez des travailleurs agricoles ont montré une prévalence de 2 à 7% des anticorps antihantavirus.
Dans les pays en développement, les zoonoses sont en voie de régression en raison de la mise en œuvre de programmes de lutte active contre ces maladies; les efforts visent surtout les populations animales. Malgré ces mesures, les travailleurs agricoles et toutes les personnes participant, de près ou de loin, à une activité qui touche le milieu agricole (vétérinaires, personnes chargées de l’emballage de la viande ou de la transformation de la volaille, tanneurs) restent exposés à de nombreuses maladies.
L’infection à hantavirus se manifeste par une fièvre hémorragique avec syndrome rénal (FHSR) ou une néphrite épidémique (NE); elle a été décrite cliniquement depuis plus de cinquante ans dans les régions endémiques d’Asie et d’Europe et touche les travailleurs agricoles, le personnel militaire et les personnes travaillant en laboratoire. L’infection provient de l’inhalation d’aérosols infectieux libérés par l’urine, la salive ou les excréments de rongeurs infectés. En général, les hantaviroses se manifestent par des symptômes hémorragiques et une altération de la fonction rénale plutôt que par une pneumonie, mais on a également décrit des cas d’œdème pulmonaire dû à l’augmentation de la perméabilité vasculaire dans la FHSR et la NE. Les conséquences pulmonaires profondes des hantaviroses n’ont été complètement appréhendées qu’à la suite d’une épidémie récente de syndrome pulmonaire à hantavirus (SPH) due à un hantavirus récemment isolé et survenue dans l’ouest des Etats-Unis (virus Muerto Canyon, Four Corners ou Sin Nombre).
Les hantavirus font partie de la famille des Bunyaviridae, virus à ARN; cinq d’entre eux sont associés à des maladies humaines. La FHSR est liée au virus de Hantaan en Asie de l’Est, au virus de Dobrava dans les Balkans et au virus de Séoul, qui a une distribution mondiale. La NE, de son côté, est associée au virus Puumala en Europe occidentale. Quant au SPH, il est probablement dû à un hantavirus nouvellement isolé dans l’ouest des Etats-Unis. De 1951 à 1983, 12 000 cas de FHSR ont été rapportés en République de Corée. En Chine, l’incidence de la maladie semble augmenter avec les épidémies qui sévissent dans les centres ruraux et urbains; en 1980, 30 500 cas (dont 2 000 mortels) ont été attribués à la FHSR.
Avec les virus provoquant une FHSR ou une NE, l’infection se traduit généralement par le développement asymptomatique d’anticorps antihantavirus. Dans le cas contraire, les signes et les symptômes de la phase précoce ne sont pas spécifiques et l’infection à hantavirus ne peut être diagnostiquée que par une analyse sérologique. La guérison est généralement longue; quelques personnes évoluent vers une FHSR ou une NE et développent une protéinurie, une hématurie microscopique, une azotémie et une oligurie. En cas de FHSR, on observe également des hémorragies profondes en raison d’une coagulation intravasculaire disséminée, de l’augmentation de la perméabilité vasculaire et du choc. La mortalité observée chez les personnes présentant la forme complète de FHSR varie de 5 à 20%.
Le SPH se manifeste par des infiltrats pulmonaires interstitiels diffus et l’apparition brutale d’une insuffisance respiratoire aiguë et d’un choc. Une hyperleucocytose marquée peut apparaître en raison de l’augmentation des cytokines qui caractérisent la maladie. La mortalité du SPH peut être supérieure à 50%. L’incidence des infections asymptomatiques ou des cas de SPH non reconnus n’est pas totalement établie.
Le diagnostic s’établit par la démonstration de la présence d’immunoglobulines M ou d’une augmentation des titres d’immunoglobine G par une méthode d’immunofluorescence indirecte sensible et hautement spécifique et par analyse des anticorps neutralisants. Les autres méthodes diagnostiques sont les réactions PCR pour les acides ribonucléiques viraux et l’immunohistochimie pour les antigènes viraux.
L’infection provient de l’inhalation d’aérosols infectieux libérés par l’urine, la salive et les excréments de rongeurs infectés — lesquels ne présentent d’ailleurs aucun symptôme apparent de la maladie. La transmission peut se produire également par inoculation percutanée d’urine, de salive ou d’excréments de rongeurs infectés, mais il n’y a aucune évidence de transmission interhumaine.
Les enquêtes séro-épidémiologiques chez les humains et les rongeurs ont montré que les hantavirus sont endémiques, avec une répartition mondiale dans les zones urbaines aussi bien que rurales. Dans les zones endémiques rurales, les interactions humain-rongeur augmentent lorsque les rongeurs envahissent de façon saisonnière les habitations ou que l’activité humaine augmente dans les régions infestées de rongeurs. Le risque d’infection est plus important chez les personnes exerçant une profession rurale. Des enquêtes ont été réalisées dans les populations rurales asymptomatiques en Italie; elles ont montré que 4 à 7% des forestiers, éleveurs, chasseurs et agriculteurs présentent des anticorps antihantavirus, contre 0,7% seulement des soldats. Chez les travailleurs agricoles asymptomatiques, en Irlande et en République tchèque, la prévalence des anticorps antihantavirus atteint respectivement 1-2% et 20-30%. Toutes les activités agricoles et connexes (semis, récolte, battage du blé, gardiennage de troupeaux et activités forestières) constituent des facteurs de risque d’infections virales. Des enquêtes sérologiques sont en cours dans l’ouest des Etats-Unis pour déterminer le risque professionnel d’infections à hantavirus. Toutefois, une étude réalisée parmi le personnel de santé soignant des patients souffrant de SPH n’a permis de mettre en évidence aucun cas d’infection. D’après les résultats obtenus sur les 68 premières personnes présentant un SPH, il apparaît que les travaux agricoles effectués dans les habitats des rongeurs infectés (comme le labourage, le nettoyage des zones de stockage des aliments, les semis, le nettoyage des excréments animaux et le gardiennage des troupeaux) comportent des risques. Le principal réservoir de SPH est la souris, Peromyscus maniculatus.
Dans les agglomérations urbaines, le réservoir de rongeurs pour le virus de Séoul est le rat domestique. Les travailleurs employés sur les docks, dans les silos à grains et dans les zoos, de même que ceux chargés de la dératisation, courent plus de risques de contracter une infection à hantavirus. Les laboratoires de recherche qui utilisent des rongeurs comme matériel d’expérimentation ont parfois constitué des sources non suspectées d’infection. D’autres professions, comme le personnel militaire et les biologistes travaillant sur le terrain, présentent également un risque plus élevé.
La ribavirine a une activité in vitro contre plusieurs hantavirus; son efficacité clinique contre le virus Hantaan a été utilisée pour traiter les personnes présentant un SPH.
Il n’existe actuellement aucune protection vaccinale, malgré tous les efforts consacrés à la mise au point de vaccins atténués, inactivés ou tués. La prévention consiste à éviter tout contact entre l’humain et les rongeurs et à réduire les populations de rongeurs dans les zones habitées pour diminuer le risque de maladie. Dans les laboratoires de recherche sur les hantavirus, la mise en place de mesures de biosécurité très strictes limite le risque de propagation virale dans les cultures cellulaires ou lors des manipulations de matériaux à fortes concentrations de virus. Dans les autres laboratoires de recherche utilisant des rongeurs, une surveillance sérologique périodique de l’infection à hantavirus chez les colonies de rongeurs pourrait être envisagée.
Comme les infections à hantavirus, la CML est par nature une infection qui frappe les rongeurs sauvages et qui se propage occasionnellement à l’humain. Le virus CML est un arenavirus, mais sa transmission se fait généralement par l’intermédiaire d’aérosols. Les hôtes naturels incluent la souris sauvage; toutefois, l’infection persistante des hamsters domestiques de Syrie est bien connue. L’infection menace par conséquent la plupart des professions exposées aux aérosols libérés par l’urine de rongeurs. L’épidémie professionnelle la plus récente a touché des personnes travaillant en laboratoire, exposées à des souris nude athymiques déficientes en lymphocytes T et infectées de façon persistante en raison de l’inoculation de lignées cellulaires tumorales contaminées.
La plupart des cas de CML sont asymptomatiques ou associés à un syndrome pseudo-grippal non spécifique; ils ne sont par conséquent pas reconnus. L’appareil respiratoire est généralement le site d’entrée, mais les symptômes respiratoires ont tendance à être non spécifiques et spontanément résolutifs. Une méningite ou une méningo-encéphalite apparaît chez un petit pourcentage de patients et peut donner lieu à un diagnostic spécifique.
Le diagnostic s’établit généralement par voie sérologique, en présence d’une augmentation du titre des anticorps antiviraux et sur la base de signes cliniques donnés. On recourt parfois aussi à l’isolement du virus et à l’immunofluorescence tissulaire.
Environ 20% des souris sauvages sont infectées par ce virus. La transmission transplacentaire du virus chez des rongeurs sensibles provoque une tolérance des lymphocytes T et une infection congénitale des souris (ou des hamsters) qui persiste la vie durant. De même, les souris déficientes en lymphocytes T, comme les souris nude, peuvent être infectées de façon permanente. Les humains sont affectés par transmission aérienne. Les lignées cellulaires de rongeurs peuvent être contaminées par le virus et le propager. Les humains contractent généralement la maladie par l’intermédiaire d’aérosols, mais la transmission peut aussi être directe ou indirecte par l’intermédiaire d’insectes vecteurs.
Toute profession exposée à des poussières contaminées par des excréments de rongeurs sauvages comporte un risque d’infection CML. Les soigneurs des animaleries de laboratoire, les personnes employées dans les commerces d’animaux de compagnie et le personnel de laboratoire travaillant sur des lignées cellulaires de rongeurs peuvent être infectés.
La CML est généralement spontanément résolutive. Toutefois, un traitement de soutien peut être nécessaire dans les cas graves.
Il n’existe actuellement aucun vaccin. Le dépistage effectué chez les souris et les hamsters de laboratoire et les lignées cellulaires limite la plupart des infections acquises en laboratoire. En ce qui concerne les souris déficientes en lymphocytes T, l’analyse sérologique nécessite l’utilisation de souris sentinelles immunocompétentes. Le respect des précautions élémentaires de sécurité est également primordial, comme le port de gants, de protections oculaires et de blouses de laboratoire. Il est capital de lutter contre les rongeurs sauvages présents dans les régions habitées pour en réduire le nombre et combattre ainsi la CML, les hantavirus et la peste.
La chlamydiose respiratoire due à Chlamydia psittaci est la cause la plus fréquente de pneumonie d’origine professionnelle (POP) dans l’abattage des animaux (volailles) et la préparation de la viande. En général, ce type de maladie est dû au contact avec des animaux malades, contact qui constitue parfois le seul indice permettant de déterminer l’origine et le type de l’infection. La transformation des animaux infectés libère des aérosols qui peuvent infecter des personnes éloignées de la chaîne de transformation de la viande; le seul fait de travailler à proximité d’une usine de transformation de viande peut donc être un indice pour la détermination du type d’infection. La chlamydiose respiratoire peut également être causée par des perroquets ou des perruches (psittacose) ou d’autres oiseaux non psittacosiques (ornithose). En revanche, les sources non aviaires de Chlamydia psittaci ne sont généralement pas considérées comme des zoonoses potentielles; toutefois, des cas d’avortements spontanés et des conjonctivites ont été décrits chez l’humain en contact avec des ovins ou des caprins. Les pneumonies dues à C. pneumoniae constituent une cause courante, récemment décrite, de pneumonies communautaires distinctes des affections à C. psittaci. En raison de sa découverte récente, le rôle de C. pneumoniae dans les POP n’est pas encore complètement établi.
L’ornithose a une symptomatologie très variable: elle peut être soit bénigne et de type pseudo-grippal, soit sévère avec pneumonie et encéphalite qui, avant les antibiotiques, entraînait une mortalité supérieure à 20%. Les prodromes se caractérisent par de la fièvre, des frissons, des myalgies, des céphalées et une toux non productive qui peuvent durer trois semaines avant que ne soit établi le diagnostic de pneumonie. Les troubles neurologiques, hépatiques et rénaux sont courants. Les radiographies montrent une condensation du lobe inférieur et des adénopathies hilaires. Le diagnostic repose sur la mise en évidence de l’exposition aviaire, en rapport ou non avec la profession, car il n’existe aucune donnée pathognomonique.
L’ornithose se traduit généralement par un titre élevé d’anticorps de fixation du complément (FC), mais l’administration précoce de tétracyclines peut supprimer la formation de ces anticorps. La présence d’une augmentation isolée des anticorps FC supérieure à 1/16, compatible avec le tableau clinique, ou d’une multiplication par 4 du titre des anticorps FC, permet de porter un diagnostic. L’utilité diagnostique des analyses sérologiques est malheureusement souvent diminuée par la présence d’anticorps antichlamydia dans les groupes à risque et d’appariements inappropriés des échantillons.
C. psittaci est présent dans presque toutes les espèces aviaires; il est très répandu chez les mammifères. L’infection provient généralement d’une transmission zoonotique, mais une transmission interhumaine est aussi possible. L’infection est souvent asymptomatique; 11% des travailleurs agricoles sans antécédent présentent des anticorps dirigés contre C. psittaci. Les épidémies restent limitées et intermittentes, mais des pandémies dues au commerce d’oiseaux exotiques se sont produites en 1930. Aux Etats-Unis, 70 à 100 cas d’ornithose sont rapportés chaque année et près du tiers de ces cas intéressent le milieu professionnel. La plupart des infections surviennent chez des personnes travaillant dans les commerces d’animaux de compagnie ou les usines d’abattage de la volaille; elles sont liées à la formation d’aérosols infectieux libérés par des tissus ou des excréments d’oiseaux. Dans les pays où les oiseaux sont des animaux de compagnie et où les mesures de quarantaine sont laxistes, les épidémies sont plus fréquentes et ne concernent pas spécifiquement certaines catégories professionnelles.
La maladie apparaît le plus souvent dans les usines d’abattage de la volaille; toutefois, les personnes se livrant au commerce des oiseaux exotiques ou travaillant dans les établissements de quarantaine aviaire, les batteries d’élevage et les cliniques vétérinaires sont également exposées.
L’administration de tétracycline ou d’érythromycine pendant dix à quatorze jours constitue le traitement de choix; les récidives cliniques sont toutefois courantes lorsque la durée du traitement est insuffisante.
Aux Etats-Unis, les oiseaux exotiques sont mis en quarantaine et traités préventivement à la tétracycline. Des méthodes comparables sont appliquées dans d’autres pays où l’on fait commerce d’oiseaux exotiques. Aucun vaccin n’existe actuellement contre l’ornithose. Des mesures ont été prises pour augmenter la ventilation afin de réduire la concentration d’aérosols dangereux, diminuer l’inhalation des particules infectieuses ou traiter les oiseaux malades, mais leur efficacité n’a pas été démontrée.
Chaque année, environ 500 000 cas de brucellose se déclarent dans le monde et sont dus à différentes espèces de brucellas. La pathogenèse des infections à brucella dépend des espèces infectantes, qui ont tendance à avoir des hôtes réservoirs différents. En général, les réservoirs de Brucella abortus, B. suis, B. melitensis, B. ovis, B. canis et B. neotomae sont respectivement les bovins, les porcs, les caprins, les ovins, les chiens et les rats.
Différentes voies de transmission ont été mises en évidence, y compris l’inhalation d’aérosols. Toutefois, le mécanisme pathogène le plus souvent incriminé est l’ingestion de produits laitiers non pasteurisés fabriqués avec du lait de chèvre. La maladie systémique qui en résulte est due à B. melitensis, mais n’est pas associée à des professions spécifiques. Une pneumonie apparaît dans 1% des cas, tandis que la toux constitue une manifestation fréquente de la maladie.
Dans les pays développés, la brucellose professionnelle est généralement due à Brucella abortus et résulte de l’ingestion ou de l’inhalation d’aérosols infectieux provenant de placentas de truies ou de bovins. L’infection est souvent subclinique; 1% des travailleurs agricoles présentent des anticorps anti-B. abortus. La maladie se développe chez 10% environ des personnes infectées. A la différence de B. melitensis, la pathologie due à B. abortus s’acquiert généralement dans le milieu de travail et son tableau est moins sévère. La brucellose aiguë se manifeste par des pics fébriles élevés, des arthralgies et une hépatosplénomégalie. Les pneumonies primitives provoquent rarement des condensations pulmonaires et se manifestent par de l’enrouement, des sifflements, des adénopathies hilaires, des infiltrats péribronchiques, des nodules parenchymateux ou des symptômes similiaires. L’agent pathogène peut généralement être isolé dans la moelle osseuse (dans 90% des cas aigus) et dans le sang (dans 50 à 80% des cas). Un diagnostic sérologique peut être établi, car on dispose de multiples méthodes d’analyses des anticorps. Le traitement par tétracyclines devrait être administré pendant quatre à six semaines, complété éventuellement par la rifampicine en vue d’une action synergique. Les populations les plus exposées sont les éleveurs de bovins, de caprins, d’ovins et de porcs, le personnel des laiteries et des abattoirs, les vétérinaires et les bouchers. Le dépistage de brucella et les programmes d’éradication ont permis de réduire considérablement le nombre des animaux infectés et d’identifier les troupeaux à risque. En présence d’animaux infectés par brucella, les seules méthodes de prévention efficaces en milieu professionnel sont d’éviter tout contact ou de porter une protection individuelle, surtout après un avortement ou une mise bas.
L’infection charbonneuse existe partout dans le monde, mais est moins répandue que l’anthrax cutané. C’est une maladie systémique qui frappe plusieurs espèces animales et qui se transmet généralement à l’humain par voie cutanée ou par l’ingestion de viande contaminée. Elle est due à l’inhalation de spores de Bacillus anthracis provenant des os, des poils ou de la peau d’ovins, de caprins ou de bovins («maladie des trieurs de laine») ou, plus rarement, lors de la préparation de viandes infectées. Les spores sont phagocytées par les macrophages alvéolaires et transportées jusqu’aux ganglions lymphatiques médiastinaux où elles germent et provoquent une médiastinite hémorragique. La maladie se présente rarement comme une pneumonie primitive, mais se caractérise par un élargissement du médiastin, un œdème pulmonaire, un épanchement pleural, une splénomégalie et une évolution rapide vers l’insuffisance respiratoire. Le taux de mortalité est supérieur à 50% malgré l’antibiothérapie et la ventilation assistée. Les hémocultures sont souvent positives, mais on peut également recourir aux analyses sérologiques (méthodes immuno-enzymatique: immunoblot). Le traitement consiste à administrer de fortes doses de pénicilline ou de la ciprofloxacine par voie intraveineuse en cas d’allergie à la pénicilline. Les populations les plus exposées sont les éleveurs, les vétérinaires, les soigneurs, les personnes spécialisées dans le traitement de la fourrure et des peaux et les travailleurs des abattoirs. Une vaccination annuelle peut être proposée pour les animaux situés dans les régions endémiques et les êtres humains fortement exposés. Les mesures de contrôle spécifiques contre le charbon sont la décontamination au formaldéhyde, la stérilisation à la vapeur des peaux et des fourrures ou leur irradiation, l’interdiction d’importer des peaux en provenance des régions endémiques et la protection individuelle (port d’un masque) pour les travailleurs exposés.
La peste, due au bacille de Yersin (Yersinia pestis), est une maladie véhiculée par les puces, enzootique chez les rongeurs sauvages. La transmission à l’humain a généralement lieu par la piqûre d’une puce infectée; l’évolution vers une septicémie est fréquente. Aux Etats-Unis, de 1970 à 1988, environ 10% des personnes septicémiques ont développé une pneumonie secondaire. Les humains et les animaux atteints de la peste pneumonique produisent des aérosols infectieux. C’est par l’inhalation des aérosols infectieux émanant de cadavres d’animaux morts d’une pneumonie secondaire que la pneumonie primaire peut se produire chez l’humain. Malgré le potentiel de propagation pulmonaire, la transmission interhumaine est rare et ne s’est pas produite aux Etats-Unis depuis cinquante ans. La prévention inclut l’isolement des personnes infectées et le port de masques par le personnel de santé. Comme la transmission aérienne est possible, il convient d’envisager l’administration préventive de tétracyclines chez toute personne en contact avec des humains ou des animaux infectés. Les professions les plus exposées sont les professions biomédicales et le personnel hospitalier de laboratoire et, dans les régions endémiques, certaines professions rurales comme les vétérinaires, les travailleurs chargés de la lutte contre les rongeurs, les trappeurs, les chasseurs, les biologistes étudiant les mammifères et la faune sauvage, ainsi que les travailleurs agricoles. Une vaccination devrait être proposée à toutes ces catégories à risque.
Due à l’inhalation de Coxiella burnetii, la fièvre Q est une maladie systémique qui se manifeste par une pneumonie atypique chez 10 à 60% des personnes infectées. De nombreux isolats de C. burnetii sont pathogènes, et les théories affirmant une virulence plasmide-dépendante restent controversées. C. burnetii infecte de nombreux animaux domestiques (moutons, vaches, chèvres et chats) dans le monde entier; elle est transmise sous forme d’aérosols provenant de l’urine, des excréments, du lait, du placenta ou des tissus utérins d’animaux infectés. C. burnetii forme une endospore très résistante qui reste infectieuse pendant des années et qui est extrêmement virulente.
Après une période d’incubation de quatre à quarante jours, la fièvre Q aiguë se manifeste par un syndrome pseudo-grippal qui évolue vers une pneumonie atypique comparable à celle due à Mycoplasma. La phase aiguë dure généralement environ deux semaines, mais peut se prolonger jusqu’à neuf semaines. La maladie peut devenir chronique vingt ans après la phase aiguë et se manifester alors par une endocardite et une hépatite.
Il est rare d’isoler d’emblée C. burnetii, car cela nécessite une installation de haute sécurité. Le diagnostic est établi par sérologie, qui doit mettre en évidence des titres d’anticorps FC supérieurs à 1/8 corroborant le tableau clinique, ou la multiplication par 4 des taux d’anticorps préexistants.
Les populations les plus exposées sont les professions agricoles (secteurs du lait et de la laine en particulier), et les personnes travaillant dans les laboratoires hospitaliers et la recherche biomédicale.
Il n’existe aucun vaccin efficace contre C. burnetii. En général, la phase aiguë est traitée par administration de tétracyclines ou de ciprofloxacine pendant deux semaines.
En raison de la répartition géographique très étendue de la maladie, du nombre important de réservoirs animaux et de la résistance à l’inactivation, les seules mesures préventives efficaces sont la protection respiratoire individuelle et le respect de mesures mises en place pour empêcher la propagation des aérosols contaminés. Toutefois, ces méthodes de contrôle sont difficiles à mettre en œuvre dans les exploitations agricoles (élevage de moutons, de bovins, etc.). Il est donc primordial de bien informer les personnes à risque afin de faciliter un diagnostic précoce. A l’hôpital, l’isolement des malades permet de limiter la propagation de la pneumonie à fièvre Q et la contamination du personnel de santé.
Pseudomonas pseudomallei est l’agent pathogène de la mélioïdose. Ce micro-organisme se rencontre surtout en Asie du Sud-Est; il est présent dans les sols et chez les rongeurs. La maladie est due au contact avec la terre et peut avoir une assez longue période de latence. Pendant et après la guerre du Viet Nam, les principales victimes de la mélioïdose aux Etats-Unis étaient les militaires. La forme pulmonaire se caractérise par une pneumonie multifocale nodulaire suppurative ou granulomateuse.
Francisella tularensis — l’agent étiologique de la tularémie — est responsable d’une zoonose due aux rongeurs sauvages et aux lagomorphes. La tularémie constitue une maladie professionnelle potentielle chez les biologistes étudiant la faune sauvage ou les mammifères, le personnel chargé de la lutte contre les rongeurs, les chasseurs, les trappeurs et les vétérinaires. La maladie peut provenir d’une inhalation, d’une inoculation directe, d’un contact cutané ou d’une ingestion; elle peut aussi être véhiculée par un vecteur. La maladie pulmonaire est due soit à une inhalation directe, soit à une propagation hématogène de la maladie septicémique. Les lésions pulmonaires de la tularémie sont aiguës, multifocales, suppuratives et nécrosantes.
L’histoplasmose est due à Histoplasma capsulatum, micro-organisme fongique libre présent dans les sols ainsi que dans les excréments d’oiseaux ou de chauves-souris. L’histoplasmose est la cause la plus importante des pneumonies fongiques d’origine professionnelle chez les travailleurs agricoles; ces affections sont décrites plus loin.
La fréquence et la sévérité des crises d’histoplasmose varient selon l’agent pathogène infectant et les taux d’anticorps de l’hôte conférés par une infection antérieure. Après une exposition importante, 50% des sujets développent une pathologie respiratoire spontanément résolutive, alors que les autres sont asymptomatiques. Les syndromes symptomatiques les moins sévères se manifestent par des symptômes pseudo-grippaux, une toux non productive et des douleurs thoraciques. Un examen médical peut permettre de détecter un érythème noueux ou un érythème polymorphe. La radiographie pulmonaire montre la présence d’infiltrats en plaques segmentaires, mais aucune donnée radiographique ne permet de différencier spécifiquement l’histoplasmose des autres infections pulmonaires. La présence d’une adénopathie hilaire et médiastinale est courante à tous les stades de l’histoplasmose primitive.
L’histoplasmose à forme pneumonique primitive évolutive se caractérise par des symptômes systémiques plus importants, une toux productive avec expectoration purulente et une hémoptysie. On note également sur les radiographies l’apparition progressive de nodules multiples, d’une condensation lobaire et d’infiltrats interstitiels denses et multilobaires. La symptomatologie est d’autant plus sévère que l’exposition est importante; la maladie peut évoluer vers une insuffisance respiratoire sévère, un syndrome de dysfonction réactive des voies aériennes (RADS) ou une atélectasie due à l’obstruction médiastinale par des adénopathies.
Dans près de 20% des cas, l’histoplasmose se manifeste par d’autres types de syndromes idiosyncrasiques indépendants de l’importance de l’exposition ou de l’évolution de la maladie primitive. Il est donc parfois possible d’observer une association arthrite/érythème noueux, une péricardite ou une histoplasmose pulmonaire chronique (infiltrats fibrotiques de l’apex des poumons avec cavernes). Enfin, un faible pourcentage de patients, en particulier les immunodéprimés, développe une histoplasmose disséminée.
Le diagnostic définitif s’établit par l’isolement du micro-organisme ou sa mise en évidence histopathologique dans un échantillon clinique. Malheureusement, les concentrations présentes sont souvent faibles et ne peuvent être détectées par les méthodes actuelles, celles-ci n’étant pas assez sensibles. Un diagnostic d’histoplasmose peut être présumé d’après la situation géographique et sur la base de l’anamnèse, des signes radiologiques pulmonaires ou de la présence de calcifications dans la rate.
On retrouve H. capsulatum partout dans le monde dans certaines conditions géologiques spécifiques, mais la maladie a été signalée surtout dans les vallées de l’Ohio et du Mississippi, aux Etats-Unis. Les spores sont présentes en grandes quantités sur les perchoirs à oiseaux, dans les vieux bâtiments, les poulaillers, les cavernes et les cours de récréation, où elles sont libérées par les activités humaines. La concentration des microconidies est particulièrement élevée dans les espaces confinés et les chantiers de démolition; l’inoculation y est aussi plus forte que dans la plupart des sites ouverts à l’extérieur. Dans les zones endémiques, les personnes qui nettoient les perchoirs à oiseaux, démolissent les vieilles bâtisses contaminées ou creusent des tranchées pour la construction de routes ou de bâtiments sont plus exposées que la population générale. Aux Etats-Unis, l’histoplasmose est responsable de 15 000 à 20 000 hospitalisations par an; le taux de mortalité y est de 3%.
Il est difficile d’établir l’origine professionnelle des cas d’infection à Histoplasma, car ce micro-organisme est présent dans le sol sous forme libre et la concentration des spores transmises par voie aérienne est importante s’il y a du vent et beaucoup de poussière. L’infection est surtout liée à la situation géographique. Dans les zones endémiques, la prévalence des tests cutanés positifs aux antigènes H. capsulatum est de 60 à 80%, indépendamment de la profession du sujet. Les manifestations pathologiques résultent généralement d’une inoculation importante et intéressent donc principalement les catégories professionnelles impliquées dans des travaux de labourage des sols ou de démolition de bâtiments contaminés.
Le traitement de l’histoplasmose et des autres infections fongiques d’origine professionnelle ne justifie pas l’administration d’un antifongique en cas de pneumopathie aiguë spontanément résolutive. En revanche, l’amphotéricine B (dose totale de 30 à 35 mg/kg) ou le kétoconazole (400 mg/jour pendant six mois) sont indiqués en cas d’histoplasmose disséminée, d’histoplasmose pulmonaire chronique, d’histoplasmose pulmonaire aiguë avec RADS ou de granulome médiastinal avec obstruction symptomatique et peuvent être utiles en cas de prolongation d’une pathologie primitive de gravité modérée. La réponse au traitement est de 80 à 100%, mais les récidives sont courantes et peuvent atteindre 20% avec l’amphotéricine B et 50% avec le kétoconazole. L’efficacité des nouveaux médicaments azolés (itraconazole et fluconazole) n’a pas encore été établie.
Il n’existe actuellement aucun vaccin efficace contre l’histoplasmose. Certaines mesures sont susceptibles de réduire l’infection, comme la décontamination chimique avec du formaldéhyde à 3%, la préhumidification du sol ou des surfaces contaminées pour diminuer la formation d’aérosols infectieux et le port de masques de protection pour éviter l’inhalation des spores présentes dans l’air, mais leur efficacité n’a pas été démontrée.
Les pneumonies fongiques des travailleurs agricoles sont l’aspergillose, la blastomycose, la cryptococcose, la coccidioïdomycose et la paracoccidioïdomycose (voir tableau 10.26). Ces maladies sont dues respectivement à Aspergillus spp., Blastomyces dermatitidis, Cryptococcus neoformans, Coccidioides immitis et Paracoccidioides brasiliensis. Malgré la vaste distribution géographique de ces champignons, la maladie est généralement signalée dans des régions endémiques. Par rapport aux pneumonies virales ou bactériennes, les pneumonies fongiques sont rares et donc généralement mal diagnostiquées. Les déficits immunitaires (lymphocytes T) augmentent la sensibilité à l’histoplasmose, la blastomycose, la cryptococcose, la coccidioïdomycose et la paracoccidioïdomycose. Toutefois, si l’exposition initiale est très intense, la maladie peut se déclarer même chez des travailleurs immunocompétents. Les infections à Aspergillus et aux champignons apparentés ont tendance à se produire chez les patients accusant une neutropénie. L’aspergillose est plus souvent une POP de personnes immunodéprimées et sera abordée plus loin dans la section consacrée aux infections chez les travailleurs immunodéprimés.
Cr. neoformans, à l’instar de H. capsulatum, est souvent présent dans les sols contaminés par les excréments aviaires. L’exposition professionnelle aux poussières contaminées par Cr. neoformans peut déclencher la maladie. La blastomycose professionnelle est liée aux travaux effectués à l’extérieur, en particulier dans l’est et le centre des Etats-Unis. La coccidioïdomycose prédomine dans les régions endémiques du sud-ouest des Etats-Unis (d’où l’expression fièvre de la vallée de San Joaquin). En Amérique du Sud et en Amérique centrale, les expositions professionnelles aux poussières contaminées engendrent plutôt une paracoccidioïdomycose; dans ce cas, l’apparition des symptômes peut être très tardive en raison du temps de latence potentiellement long de cette affection.
Les tableaux cliniques de la coccidioïdomycose, de la blastomycose et de la paracoccidioïdomycose sont analogues à celui de l’histoplasmose. La contamination par voie aérienne peut produire une POP si l’inoculation initiale est assez forte. Toutefois, des facteurs dépendants de l’hôte (comme l’exposition antérieure) empêchent le développement de la maladie chez la plupart des individus. S’agissant de la coccidioïdomycose, seul un faible pourcentage de personnes infectées présente des signes pulmonaires et systémiques. La dissémination dans différents organes est rare en l’absence d’immunodépression. Bien que le poumon soit généralement la source d’infection, la blastomycose peut se manifester par une symptomatologie pulmonaire, cutanée ou systémique. Les manifestations cliniques les plus courantes sont la toux chronique et la pneumonie, indifférenciable de la tuberculose. Toutefois, dans la majorité des cas de blastomycose cliniquement apparente, il existe également des lésions extrapulmonaires qui intéressent la peau, les os ou l’appareil urogénital. La paracoccidioïdomycose est une maladie du Mexique, de l’Amérique centrale et de l’Amérique du Sud qui apparaît le plus souvent comme une réactivation d’une infection antérieure, après une période de latence longue, mais variable. La maladie peut être liée au vieillissement des individus infectés et une réactivation peut être induite par l’immunosuppression. Les manifestations pulmonaires sont comparables à celles des autres pneumonies fongiques, mais sont souvent accompagnées de symptômes extrapulmonaires intéressant notamment les muqueuses.
Le poumon est le site habituel de l’infection primitive par Cryptococcus neoformans. Comme dans le cas des autres infections fongiques, les infections pulmonaires à Cr. neoformans peuvent être asymptomatiques, spontanément résolutives ou progressives. Toutefois, le micro-organisme se dissémine parfois et gagne, en particulier, les méninges et le cerveau, sans entraîner de pathologie respiratoire symptomatique. La manifestation clinique la plus courante de l’infection à Cr. neoformans, bien que rare, reste la méningo-encéphalite cryptococcique sans signe de cryptococcose pulmonaire.
La démonstration directe de la présence du micro-organisme dans les tissus permet un diagnostic définitif à partir des biopsies et des préparations cytologiques. L’immunofluorescence peut être utile pour confirmer le diagnostic si les détails morphologiques sont insuffisants pour établir l’agent étiologique. Les micro-organismes peuvent également être mis en culture à partir de lésions suspectes. Le test d’agglutinines cryptococciques sur latex effectué sur des échantillons de liquide céphalorachidien permet d’orienter le diagnostic vers une méningo-encéphalite cryptococcique. Toutefois, la mise en évidence de ces micro-organismes n’est pas toujours suffisante; ainsi, une prolifération saprophyte de Cr. neoformans peut se produire dans les voies aériennes.
Les travailleurs les plus exposés sont ceux chargés d’isoler ces champignons en laboratoire.
Le traitement antifongique est comparable à celui de l’histoplasmose.
Le personnel des laboratoires devrait respecter strictement les consignes de sécurité. En outre, le port d’un masque pour tout travail au contact de sols fortement contaminés par des excréments aviaires permet de réduire l’exposition à Cr. neoformans.
L’inhalation d’aérosols infectieux est la source la plus courante d’infection chez les personnes travaillant en milieux de soins. De nombreux types de pneumonies virales ou bactériennes peuvent avoir une origine professionnelle (voir tableau 10.26). La majorité des infections sont virales et spontanément résolutives. Toutefois, on a recensé plusieurs épidémies potentiellement graves de tuberculose, de rougeole, de coqueluche et de pneumonies pneumococciques chez le personnel hospitalier. Les infections qui apparaissent chez le travailleur immunodéprimé seront abordées à la fin du présent chapitre.
Les personnes travaillant en laboratoire au contact d’agents pathogènes sont les plus exposées. En effet, la transmission se produit lorsque ces agents sont mis en suspension dans l’air pendant la phase de traitement initiale des échantillons cliniques provenant de patients potentiellement infectieux; elle reste souvent ignorée. Ainsi, lors d’une épidémie collective récente de brucellose, un tiers des techniciens de laboratoire exposés avaient contracté la maladie: leur activité professionnelle était le seul facteur de risque identifié. La transmission interhumaine entre collègues, la transmission par les aliments ou l’eau, le contact avec un échantillon clinique précis n’ont pu être reconnus comme étant des facteurs de risque avérés. Il en va de même pour la rubéole, la tuberculose, la varicelle et les pathologies dues au virus respiratoire syncytial, affections qui sont toutes des maladies professionnelles pouvant être contractées par les techniciens de laboratoire.
Dans le secteur de la recherche biomédicale, l’inhalation reste le principal mode de transmission des maladies infectieuses, malgré la rigueur des précautions vétérinaires, le respect des consignes de sécurité et l’utilisation d’animaux sains provenant d’élevages. Ces mesures de prévention peuvent d’ailleurs être déjouées suite à la découverte de nouveaux micro-organismes ou de réservoirs zoonotiques inconnus jusqu’ici.
Dans les pays développés, la rougeole, en tant que maladie professionnelle, est devenue un problème de plus en plus important pour les personnes travaillant en milieu hospitalier. Depuis 1989, cette maladie a refait son apparition aux Etats-Unis, car les recommandations en matière de protection vaccinale n’ont pas été suivies et parce que l’immunisation n’est pas toujours complète après une primo-vaccination. En raison de la morbidité élevée et de la mortalité potentielle chez les personnes sensibles, la rougeole devrait occuper une place particulière dans les programmes de santé au travail. De 1985 à 1989, plus de 350 cas de rougeole professionnelle ont été recensés aux Etats-Unis, représentant 1% de l’ensemble des cas déclarés. Environ 30% du personnel hospitalier ayant contracté la maladie sur le lieu de travail a dû être hospitalisé. Les catégories professionnelles les plus touchées étaient le personnel infirmier et médical; 90% d’entre eux avaient été contaminés par leurs patients. La moitié de ces personnes malades étaient éligibles pour la vaccination, mais aucune d’entre elles n’avait été vaccinée. L’augmentation de la morbidité et de la mortalité imputables à la rougeole chez l’adulte pose le problème de la contagion des patients et des collègues de travail par le personnel infecté.
En 1989, une commission consultative sur les pratiques vaccinales a recommandé qu’au moment de leur admission à un emploi dans un établissement de santé les nouveaux employés reçoivent deux doses de vaccin contre la rougeole dans les cas où une immunité acquise n’aurait pu être démontrée. Le statut sérologique et vaccinal des travailleurs devrait être noté. En outre, en cas de contact avec des patients ayant la rougeole, il est conseillé de procéder à une réévaluation du statut immunitaire du personnel médical et paramédical. Le respect de ces recommandations et l’isolement des malades ayant la rougeole (connue ou suspectée) devraient empêcher la transmission de la maladie dans les établissements de soins.
Outre les manifestations courantes observées chez les adultes non immunisés, la rougeole peut également présenter un tableau atypique et modifié qu’il convient de prendre en considération; en effet, de nombreux travailleurs hospitaliers ont déjà reçu des vaccins tués ou ont acquis une immunité partielle. La rougeole classique a une durée d’incubation de deux semaines et présente des symptômes bénins des voies aériennes supérieures. Au cours de cette période, le travailleur est virémique et contagieux. Ensuite, pendant sept à dix jours, la maladie se manifeste par de la toux, du coryza, de la conjonctivite et l’apparition d’une éruption morbiliforme et d’un signe de Koplik (points blancs saillants sur la muqueuse buccale) pathognomonique de la rougeole. On observe à la radiographie des infiltrats réticulonodulaires diffus et des adénopathies hilaires bilatérales, souvent en rapport avec une bronchopneumonie bactérienne. Ces signes apparaissent longtemps après une éventuelle contamination par le sujet infecté d’autres personnes sensibles. Chez l’adulte, les complications pulmonaires sont responsables de 90% des décès dus à la rougeole.
Aucun traitement antiviral spécifique n’est efficace, quelle que soit la forme de rougeole, bien que l’administration d’immunoglobulines antirougeole en forte concentration soit susceptible d’améliorer certains symptômes chez l’adulte.
Dans la rougeole atypique, spécifique aux personnes vaccinées avec un vaccin tué développé dans les années soixante, l’implication pulmonaire est souvent grave. L’éruption est atypique et le signe de Koplik rare. Dans la rougeole modifiée, spécifique aux personnes ayant reçu un vaccin vivant mais ayant développé une immunité partielle, les signes et les symptômes sont comparables à ceux de la rougeole classique, mais ils sont atténués et passent souvent inaperçus. Les personnes présentant une rougeole atypique ou modifiée sont virémiques et peuvent propager le virus.
Chez les travailleurs hospitaliers, la rougeole est souvent modifiée ou atypique et rarement suspectée. Le diagnostic devrait être évoqué chez toute personne présentant une éruption maculopapuleuse érythémateuse précédée d’un prodrome fébrile de trois à quatre jours. En cas de primo-infection et en l’absence d’immunisation antérieure, l’isolement viral ou la détection des antigènes est difficile, mais les analyses immuno-enzymatiques ou à anticorps fluorescents peuvent être utilisées pour un diagnostic rapide. En cas d’immunisation antérieure, l’interprétation de ces analyses est difficile; la coloration par anticorps immunofluorescents de cellules exfoliées peut être très utile.
Le personnel médical et infirmier ayant une sensibilité au virus a presque neuf fois plus de risques de contracter la rougeole que des personnes du même âge ne travaillant pas dans le secteur de la santé. La transmission interhumaine est due à l’inhalation d’aérosols infectieux présents dans l’air. Le personnel hospitalier peut être contaminé par les patients et des collègues qui, à leur tour, transmettent la rougeole à des patients, des collègues ou des membres de leur famille.
Des épidémies de rougeole ont été décrites parmi le personnel enseignant dans les pays développés ainsi que parmi les travailleurs agricoles vivant sur place dans des logements collectifs.
Les mesures stratégiques en matière de santé publique comprennent des campagnes de vaccination et des programmes de prévention permettant de détecter les nouveaux cas et de contrôler le statut immunitaire des travailleurs. En l’absence d’antécédents d’infection naturelle ou de vaccination appropriée (deux doses), des analyses sérologiques devraient être effectuées. La vaccination est contre-indiquée chez les femmes enceintes; par contre, celle des autres travailleurs à risque contribue fortement à la prévention de la maladie. La mise à l’écart pendant vingt et un jours des travailleurs sensibles qui ont été exposés au virus de la rougeole peut permettre de diminuer la propagation de la maladie. La limitation de l’activité professionnelle pendant les sept jours qui suivent l’apparition de l’éruption peut également permettre de freiner la transmission de l’affection. Malheureusement, les travailleurs vaccinés peuvent développer une rougeole, même si des taux d’anticorps protecteurs ont été mis en évidence avant les premières manifestations de la maladie. Il est donc recommandé de porter un masque de protection lors de tout contact avec des patients ayant la rougeole.
Plusieurs virus qui ne sont pas spécifiques au milieu professionnel hospitalier sont à l’origine des POP parmi le personnel de santé. Les agents étiologiques sont les mêmes que ceux présents dans la collectivité, c’est-à-dire les adénovirus, les cytomégalovirus, le virus influenza, le virus para-influenza et le virus respiratoire syncytial. Ces micro-organismes étant également présents dans la collectivité, il est difficile de leur attribuer l’origine d’une POP donnée. Toutefois, des études sérologiques suggèrent que le personnel de santé et le personnel des garderies ont un risque plus important d’exposition à ces agents pathogènes respiratoires. Ces virus sont également responsables d’épidémies dans les situations où les travailleurs sont réunis dans un espace confiné; ainsi, les épidémies d’infections à adénovirus sont courantes dans les casernes militaires.
La coqueluche, comme la rougeole, est en recrudescence chez le personnel hospitalier dans les pays développés. En 1993, près de 6 000 cas de coqueluche ont été recensés aux Etats-Unis, soit une augmentation de 80% par rapport à 1992. A la différence des années précédentes, 25% des cas déclarés visaient des sujets âgés de plus de dix ans. On ne connaît pas précisément le nombre des cas d’origine professionnelle pour le personnel hospitalier, mais il pourrait bien être sous-estimé dans les pays développés. Si l’on attache actuellement une importance toute particulière au diagnostic et à la surveillance de la coqueluche, c’est en raison de la décroissance de l’immunité chez l’adulte et du risque de transmission de l’infection aux enfants sensibles par le personnel hospitalier.
En l’absence de traitement, la coqueluche peut durer six à dix semaines. Pendant la première semaine — période la plus contagieuse — on note une toux sèche, un coryza, une conjonctivite et de la fièvre. Chez les adultes vaccinés, la toux productive et persistante peut durer plusieurs semaines et la coqueluche est rarement évoquée. Le diagnostic clinique est difficile, mais devrait être suspecté devant une toux de plus de sept jours. Une numération leucocytaire supérieure à 20 000 avec prédominance de lymphocytes peut constituer la seule anomalie biologique, mais elle est rarement notée chez l’adulte. Les radiographies thoraciques montrent une bronchopneumonie confluante dans les lobes inférieurs, qui irradie depuis le cœur pour donner le signe caractéristique du «cœur en porc-épic»; une atélectasie est présente dans 50% des cas. Le pouvoir infectieux extrêmement puissant de l’agent pathogène rend indispensable un isolement respiratoire strict jusqu’à ce qu’un traitement par érythromycine ou triméthoprime/sulphaméthoxazole ait été administré pendant cinq jours. Tout contact étroit entre une personne infectée et une personne employée à l’hôpital sans avoir respecté les précautions imposées exige l’administration d’une antibiothérapie prophylactique pendant quatorze jours, et, cela, quel que soit son statut immunitaire.
L’isolement de Bordetella pertussis, la coloration par immunofluorescence directe des sécrétions nasales ou la production d’anticorps anti-B. pertussis contribuent à l’établissement du diagnostic définitif.
B. pertussis est un virus puissant qui se transmet d’une personne à l’autre par inhalation d’aérosols infectieux; son taux d’attaque est de 70 à 100%. Autrefois, la coqueluche n’était pas une maladie d’adultes et n’était pas considérée comme une POP. Lors d’une flambée collective de coqueluche dans l’Ouest des Etats-Unis, de nombreuses personnes travaillant dans les hôpitaux ont été exposées sur place et ont contracté une coqueluche malgré une antibiothérapie prophylactique. La décroissance des taux d’anticorps protecteurs observés chez les adultes n’ayant jamais eu de signe clinique de la maladie, mais ayant reçu un vaccin anticoquelucheux préparé sur cellules après 1940, est responsable d’une augmentation de la population sensible à l’agent de la coqueluche parmi le personnel hospitalier des pays développés.
L’identification, l’isolement et le traitement des personnes atteintes sont les principales stratégies de lutte contre la maladie dans les hôpitaux. L’utilité du vaccin anticoquelucheux acellulaire pour le personnel hospitalier ayant un titre insuffisant d’anticorps protecteurs n’a pas été démontrée. Lors de la flambée qui a eu lieu dans l’Ouest des Etats-Unis, un tiers du personnel hospitalier vacciné a signalé des effets secondaires du vaccin, discrets ou modérés, mais 1% seulement a présenté des symptômes systémiques «sévères». Bien que ce petit groupe de personnes ait dû interrompre son travail, aucun symptôme neurologique n’a été rapporté.
Au cours des années cinquante, il était admis que le personnel de santé des pays développés était plus exposé à la tuberculose (TB — maladie granulomateuse due à Mycobacterium tuberculosis ou à un micro-organisme apparenté M. bovis) que la population générale. De 1970 à 1980, les enquêtes ont suggéré que ce risque n’était en réalité que faiblement accru. A la fin des années quatre-vingt, en revanche, on a constaté une augmentation importante du nombre des cas de TB admis dans les hôpitaux américains, ce qui s’est traduit par une transmission insoupçonnée de M. tuberculosis au personnel hospitalier. La prévalence élevée de tests tuberculiniques positifs dans certaines catégories socio-économiques ou émigrantes dont est issue une grande partie du personnel hospitalier et la faible association entre le virage du test cutané et l’exposition professionnelle à la TB rendent difficile toute quantification du risque de transmission professionnelle de cette maladie aux travailleurs. En 1993, aux Etats-Unis, on estimait que le personnel de santé représentait 3,2% des personnes tuberculeuses. Malgré la difficulté à définir le risque, une infection ayant un rapport avec le milieu professionnel devrait toujours être évoquée lorsque des personnes travaillant à l’hôpital développent une tuberculose ou que leur test tuberculinique devient positif.
M. tuberculosis se transmet presque exclusivement d’une personne à l’autre par l’intermédiaire de particules infectieuses de 1 à 5 µm de diamètre projetées dans l’air quand le sujet malade tousse, parle ou éternue. Le risque d’infection est fonction de l’intensité de l’exposition aux aérosols infectieux; les facteurs suivants jouent un rôle important: espaces communs confinés, concentration élevée et élimination insuffisante des particules infectieuses, remise en circulation d’air chargé de particules infectieuses et contact prolongé avec de l’air vicié. Dans les établissements de soins, des techniques telles que la bronchoscopie, l’intubation intratrachéale et l’aérosolthérapie augmentent la concentration d’aérosols infectieux. Près de 30% des personnes partageant un espace commun avec une personne infectée deviennent elles-mêmes infectées et ont des tests tuberculiniques positifs. Parmi elles, 3 à 10% développeront une TB dans les douze mois (primo-infection), tandis que 5 à 10% feront une tuberculose au cours de leur vie (réactivation). Les pourcentages les plus élevés se rencontrent surtout dans les pays en développement et dans les régions où la malnutrition est la plus répandue. Chez les sujets infectés par le VIH, on trouve un taux de réactivation de la tuberculose plus élevé que dans la population générale, soit environ 3 à 8% par an. Le taux de CFR («case-fatality rate») varie: dans les pays développés, il est compris entre 5 et 10%, alors que dans les pays en développement, il atteint 15 à 40%.
Avant l’épidémie de sida, la tuberculose était pulmonaire dans 85 à 90% des cas. Toux chronique, expectoration, fièvre et perte de poids restent les symptômes les plus fréquents dans ce type de tuberculose. L’examen clinique n’est pas d’une grande utilité, sauf dans de rares cas de respiration amphorique ou de râles crépitants post-tussifs au niveau des lobes supérieurs. Une radiographie thoracique anormale est trouvée dans presque tous les cas et constitue généralement le premier signe évoquant une tuberculose. Dans la primo-infection tuberculeuse, il est fréquent d’observer un infiltrat au niveau des lobes inférieurs ou moyens avec une adénopathie hilaire homolatérale et une atélectasie. Une réactivation de la tuberculose se traduit généralement par un infiltrat et l’apparition de cavernes dans les lobes supérieurs des poumons. Bien que sensible, la radiographie thoracique manque de spécificité et ne permet pas d’établir un diagnostic définitif.
Le diagnostic définitif de tuberculose pulmonaire ne peut être établi que par l’isolement de M. tuberculosis dans les expectorations ou à partir d’une biopsie pulmonaire, bien qu’un diagnostic de présomption soit possible si des bacilles acido-résistants sont mis en évidence dans les crachats de sujets présentant un tableau clinique en rapport avec une tuberculose. Le diagnostic de tuberculose devrait être évoqué sur la base des signes cliniques et des symptômes. En cas de suspicion, l’isolement et le traitement des sujets devraient être entrepris sans attendre le résultat du test tuberculinique. Dans les pays en développement où les possibilités de procéder à des tests tuberculiniques et à des radiographies thoraciques sont réduites, l’OMS suggère de rechercher une tuberculose chez toute personne présentant un symptôme respiratoire quelconque depuis plus de trois semaines, une hémoptysie quelle que soit sa durée ou une perte de poids significative. Ces personnes devraient bénéficier d’un examen microscopique de leurs expectorations à la recherche de bacilles acido-résistants.
La transmission de M. tuberculosis par voie aérienne de travailleur à travailleur ou de client à travailleur par voie aérienne a été décrite chez le personnel hospitalier, le personnel navigant, les mineurs, le personnel pénitentiaire, les soigneurs d’animaux, les travailleurs des chantiers navals, le personnel scolaire et les personnes travaillant dans des usines de fabrication de contreplaqué. Une attention particulière devrait être portée à certaines professions comme les travailleurs agricoles, les soigneurs d’animaux, les travailleurs manuels, le personnel de maison, les concierges et les personnels de cuisine, même si une grande partie du risque est imputable aux conditions socio-économiques ou au statut d’immigré de bon nombre de ces travailleurs.
Il convient aussi d’être particulièrement vigilant chez les mineurs et les autres travailleurs exposés à la silice. Outre un risque plus important de primo-infection dû au contact avec leurs collègues de travail, les personnes silicotiques sont plus susceptibles d’évoluer vers une tuberculose et ont une mortalité spécifique par tuberculose plus importante que les travailleurs non silicotiques. Chez le silicotique, comme chez la plupart des gens, M. tuberculosis est réactivé après une primo-infection ancienne qui, chez le silicotique, est antérieure à l’exposition à la silice. Dans les modèles expérimentaux, l’exposition à la silice aggrave l’évolution de la maladie selon un mode dose-dépendant, mais on ne sait pas vraiment si les travailleurs exposées à la silice, mais non silicotiques, courent un risque plus grand de contracter une tuberculose. Les travailleurs des fonderies exposés aux poussières siliceuses, mais sans signe radiographique de silicose, ont un risque de mortalité spécifique par tuberculose trois fois plus élevé que leurs homologues non exposés à la silice. Aucune autre exposition professionnelle à des poussières n’est associée à un risque accru de tuberculose.
Les travailleurs agricoles migrants ont davantage de risque de réactiver une tuberculose que la population générale. Les estimations de tests tuberculiniques positifs chez cette catégorie professionnelle sont de 45% pour les personnes de quinze à trente-quatre ans, et de 70% pour celles de plus de trente-quatre ans.
Les personnes travaillant dans des laboratoires d’analyses ont un risque plus important de contracter une tuberculose d’origine professionnelle, acquise par transmission aérienne. Dans une enquête récente portant sur dix ans, effectuée dans des hôpitaux du Japon, 0,8% des laborantins présentaient une tuberculose. Aucune source collective n’a pu être identifiée et une exposition professionnelle n’a pu être mise en évidence que dans 20% des cas. La plupart de ces cas concernaient des personnes travaillant dans des laboratoires d’anatomopathologie ou de bactériologie ou dans les salles d’autopsie.
Plusieurs protocoles thérapeutiques ont montré leur efficacité dans différents établissements de soins ambulatoires. Dans les pays développés, le protocole standard consiste dans l’administration de doses journalières d’une quadrithérapie (incluant l’isoniazine et la rifampicine) pendant deux mois, puis de doses journalières d’isoniazide et de rifampicine pendant les quatre mois suivants. Chez les malades qui supportent mal ce traitement, l’administration des mêmes médicaments deux fois par semaine, mais sous surveillance, reste une possibilité. Dans les pays en développement et dans les situations où les traitements antituberculeux ne sont pas facilement disponibles, on a généralement recours à l’administration journalière d’isoniazide et de rifampicine pendant neuf à douze mois. Le protocole thérapeutique devrait être cohérent avec la politique nationale et prendre en considération la sensibilité du micro-organisme au traitement antituberculeux standard disponible sur place et à la durée du traitement. En raison des ressources limitées permettant de lutter contre la tuberculose dans les pays en développement, les efforts devraient se concentrer sur les sources primitives d’infection, c’est-à-dire les patients dont les crachats contiennent des bacilles acido-résistants.
Dans les établissements de soins, un arrêt de travail est indiqué chez le personnel présentant une tuberculose pulmonaire. Dans les autres établissements, il suffit d’isoler les sujets infectés de leurs collègues. De façon générale, on considère que les personnes cessent d’être infectieuses si, après deux semaines de traitement antituberculeux adapté, on constate une amélioration symptomatique et une diminution du nombre de bacilles acido-résistants sur les lames des expectorations.
Les principales mesures de prévention concernant la transmission professionnelle ou collective de la tuberculose restent l’identification, l’isolement et le traitement des personnes atteintes de tuberculose pulmonaire. Là où les risques de transmission sont exceptionnellement élevés, on pourra recourir à une ventilation efficace pour diluer les aérosols infectés présents dans l’air, au filtrage de l’air et à des lampes à rayons ultraviolets, ou encore au port de masques respiratoires; l’efficacité de ces méthodes n’est toutefois pas établie. L’utilité du BCG pour protéger les travailleurs exposés reste controversée.
Les infections bactériennes courantes du poumon peuvent être transmises par des patients ou acquises au sein de la collectivité. En milieu de travail, le risque de transmission aérienne de bactéries pathogènes comme Streptococcus pneumoniae, Haemophilus influenza, Neisseria meningitidis, Mycoplasma pneumoniae et Legionella spp. existe (voir tableau 10.26); les pathologies résultantes sont incluses dans de nombreux programmes de surveillance hospitaliers. Les infections bactériennes des voies respiratoires d’origine professionnelle ne sont pas limitées au personnel de santé; ainsi, les infections par Streptococcus spp. sont une cause bien connue d’épidémie dans les casernes militaires. Toutefois, pour un travailleur donné, la prévalence de ces pathologies en dehors du milieu de travail complique la distinction entre infection professionnelle et infection acquise dans la collectivité. Le tableau clinique, les tests diagnostiques, l’épidémiologie et le traitement de ces pathologies sont décrits dans les traités médicaux classiques.
Les travailleurs immunodéprimés encourent un plus grand risque de contracter une POP. Par ailleurs, de nombreux micro-organismes qui ne sont pas pathogènes chez des individus normaux le seront chez des sujets immunodéprimés. Le type d’immunosuppression influera également sur la sensibilité à la maladie. Ainsi, l’aspergillose pulmonaire invasive est une complication plus fréquente de la chimiothérapie que du sida.
L’aspergillose pulmonaire invasive s’observe généralement chez les immunodéprimés, principalement chez ceux qui présentent une neutropénie. Toutefois, cette pathologie est décrite parfois chez des sujets sans prédisposition apparente à la maladie. L’aspergillose pulmonaire invasive se manifeste normalement par une pneumonie nécrosante grave avec ou sans atteinte systémique chez un patient neutropénique. Alors que l’aspergillose invasive est une infection nosocomiale fréquemment observée chez les patients soumis à une chimiothérapie, elle entraîne une mortalité élevée chez les travailleurs neutropéniques. Les techniques permettant de lutter contre l’aspergillose nosocomiale peuvent également protéger les travailleurs plus sensibles.
Divers agents pathogènes pour l’animal occasionnent des zoonoses potentielles uniquement chez les sujets immunodéprimés. Les zoonoses transmises par l’exposition aux aérosols, observées uniquement chez l’immunodéprimé, incluent l’encéphalitozoonose (due à Encephalitozoon cuniculi), la tuberculose aviaire (due à Mycobacterium avium) et les infections à Rhodococcus equi. Ces affections se rencontrent surtout en milieu agricole. Les méthodes de protection des travailleurs immunodéprimés n’ont pas fait jusqu’ici l’objet d’une étude exhaustive.
Chez le travailleur immunodéprimé, de nombreux agents pathogènes potentiels peuvent provoquer des maladies graves et invasives que l’on ne rencontre pas chez les patients normaux. Par exemple, des infections sévères par Candida albicans ou Pneumocystis carinii sont les manifestations classiques du sida. Chez le travailleur immunodéprimé, le spectre des agents pathogènes d’origine professionnelle peut donc englober des pathologies généralement absentes chez les sujets normaux. Les maladies des sujets immunodéprimés ont été étudiées de façon approfondie et ne seront pas examinées ici plus en détail.
Les POP surviennent de façon prédominante chez cinq groupes de travailleurs: les personnels hospitaliers, les travailleurs agricoles, les personnes employées dans la filière viande, les personnels militaires et les personnes employées dans des laboratoires biomédicaux (voir tableau 10.26). La façon la plus efficace de réduire l’infection consiste dans la plupart des situations à éviter les aérosols infectieux, mais cette mesure est difficile à mettre en œuvre. Ainsi, Coxiella burnetii, agent étiologique de la fièvre Q, peut être présent dans n’importe quel type d’environnement déjà contaminé par des liquides biologiques d’animaux infectés; il est pratiquement impossible cependant d’éviter tous les aérosols potentiellement infectés dans de nombreuses situations à faible risque, comme le gardiennage des troupeaux de moutons ou les rodéos. La prévention des maladies concomitantes permet de réduire le risque de POP. La silicose, par exemple, augmente le risque de réactivation d’une tuberculose, et la diminution de l’exposition à la silice peut réduire par conséquent le risque de tuberculose chez les mineurs. Pour les POP ayant une mortalité et une morbidité significatives dans la population générale, l’immunisation peut constituer la mesure de santé publique la plus importante. En outre, l’éducation des travailleurs quant aux risques de POP contribue à leur participation active aux programmes de lutte contre les maladies professionnelles et favorise le diagnostic précoce de ces maladies.
Chez le personnel hospitalier et militaire, la transmission interindividuelle constitue généralement le principal mode d’infection. L’immunisation des travailleurs peut empêcher la maladie et peut être utile pour contrôler les agents hautement pathogènes ou à mortalité élevée. Les risques étant plus élevés chez les personnes qui ne sont pas correctement immunisées, l’identification, l’isolement et le traitement des sujets malades revêtent toute leur importance dans la lutte contre les maladies. En cas d’échec des mesures d’immunisation et d’isolement, et dans les cas où la morbidité et la mortalité associées à la maladie sont inacceptables, il convient de recourir à une protection respiratoire individuelle ou à des mesures de prévention technique permettant de réduire la concentration ou le potentiel infectieux des aérosols présents dans l’atmosphère.
Chez les travailleurs agricoles et les personnes employées dans l’industrie de la viande ou dans les laboratoires biomédicaux, la transmission de l’animal à l’humain est courante. Outre l’immunisation des personnes sensibles lorsqu’elle est possible, les autres stratégies de lutte contre la maladie sont la vaccination des animaux, l’antibiothérapie prophylactique sous contrôle vétérinaire des animaux apparemment sains, la mise en quarantaine de tout animal nouvellement arrivé, l’isolement et le traitement des animaux malades et l’achat d’animaux sains. Lorsque ces méthodes ont échoué et que les risques de morbidité et de mortalité sont élevés, le recours à une protection individuelle ou à des mesures de prévention technique devrait être envisagé.
La transmission de l’environnement à l’humain des agents infectieux est également courante parmi les travailleurs agricoles. Leur immunisation est possible lorqu’on dispose d’un vaccin mais, pour bon nombre de ces agents pathogènes, l’incidence de la maladie dans la population générale est faible et la préparation des vaccins est rarement faisable. Dans les établissements agricoles, par ailleurs, les sources d’infection sont multiples et les mesures de prévention technique qui permettraient de réduire la concentration ou le potentiel infectieux des aérosols pathogènes sont difficilement praticables. Il convient alors de recourir à des agents mouillants ou à d’autres méthodes pour réduire la quantité de poussières, ainsi qu’à des agents de décontamination et à une protection respiratoire individuelle. Etant donné que le contrôle des POP chez les travailleurs agricoles est souvent malaisé et que ces maladies sont rarement décelées par le personnel médical, l’éducation des travailleurs, ainsi qu’une meilleure communication entre les travailleurs et le personnel médical demeurent essentielles.